Rolul proteinelor în promovarea hipertrofiei musculare

1. Introducere
Menținerea masei musculare scheletice pe toată durata vieții este esențială pentru păstrarea sănătății metabolice și a locomoției independente. Deși este esențial pentru producerea forței contractile, mușchiul scheletic servește de asemenea, ca loc principal de eliminare postprandială a glucozei și este cel mai mare contributor la cheltuiala de energie în repaus. Pe lângă importanța centrată pe sănătate a menținerii mușchiului scheletic, există de asemenea, un mare interes, în special în cadrul comunității atletice, pentru îmbunătățirea răspunsului adaptativ al mușchilor scheletici la antrenament (adică, producție îmbunătățită de forță și creșterea dimensiunii musculare: hipertrofie) cu scopul de a maximiza performanța fizică în evenimentele competitive. Astfel, strategiile de creștere a hipertrofiei mușchilor scheletici și de promovare a remodelării și recondiționării optime a mușchilor scheletici în urma antrenamentului este un domeniu intens de cercetare științifică, cu ramificații atât în mediul clinic, cât și în cel atletic.
Există acum o mulțime de studii care au caracterizat răspunsul mușchilor scheletici la modificări ale stimulilor nutriționali și contractili. Ceea ce au arătat aceste studii este că dimensiunea mușchiului scheletic depinde de procesele cinetice ale sintezei proteinelor musculare (MPS) și de descompunere a proteinelor musculare (MPB), diferența algebrică (MPS minus MPB) între care dictează echilibrul proteic net (NPB) . Când fluctuațiile diurne ale MPS sunt egale cu cele ale MPB, masa musculară este menținută. Acumularea proteinelor musculare care duce la creșterea dimensiunii fibrelor musculare este realizată numai atunci când ratele nete de MPS depășesc MPB și NPB este pozitivă. Alternativ, catabolismul muscular net (atrofia) care duce la pierderea proteinelor musculare, apare atunci când MPB depășește MPS și NPB este negativ. Încărcarea crescută a mușchilor scheletici și hiperaminoacidemia în urma aportului de proteine din dietă, exercită independent și sinergic o influență pozitivă asupra NPB prin modularea echilibrului relativ dintre MPS și MPB. Într-adevăr, în starea postabsorbtivă, o criză acută de exercițiu de rezistență stimulează MPS cu peste 100% peste nivelurile bazale; cu toate acestea, NPB rămâne negativă datorită activării concomitente a MPB. Numai atunci când proteinele sunt ingerate în urma unui exercițiu de rezistență, există un impact sinergic asupra MPS, rezultând o stare prelungită de NPB pozitiv. Sesiunile repetitive de exerciții de rezistență în combinație cu aportul de proteine cresc NPB și promovează acumularea de proteine mușchilor în timp.
În această scurtă trecere în revistă, ne concentrăm asupra modului în care proteinele dietetice sunt utilizate în sprijinul remodelării proteinelor musculare scheletice și modul în care proteinele pot facilita creșterea MPS post-exercițiu și în cele din urmă pot afecta hipertrofia. Pentru a obține o înțelegere mai profundă a acestui concept, ne referim la capacitatea umană de a digera proteinele și o contrastăm cu capacitatea mușchilor scheletici de a utiliza aminoacizii disponibili pentru MPS. În plus, discutăm problema cantității de proteine pe masă, care stimulează optim MPS zilnic și speculăm de ce o strategie axată pe suprimarea persistentă a MPB poate fi nepotrivită obiectivului de a promova hipertrofia musculară cu antrenament de rezistență. Folosind dimensiuni mari de eșantion din meta-analize recente, încercăm să oferim o rețetă „optimă” pentru aportul de proteine pentru a maximiza remodelarea proteinelor și hipertrofia după exercițiul de rezistență. În cele din urmă, oferim o scurtă discuție a descoperirilor recente cu privire la strategiile de menținere sau chiar de creștere a masei musculare scheletice în perioadele de restricție energetică.
2. Înțelegerea limitelor sintezei proteinelor musculare: Câtă proteină pot folosi muschii?
Capacitatea de a digera și absorbi proteinele dietetice și aminoacidemia ulterioară depășește cu mult capacitatea mușchiului scheletic de a utiliza aminoacizii constituenți în scopul anabolismului muscular. După ingestia orală, digestia proteinelor este inițiată în stomac de pepsină în prezența acidului clorhidric și continuă în duoden prin secreția de proteaze pancreatice și proteaze enterocite. Produsele finale includ fragmente de peptide și aminoacizi liberi care sunt absorbiți aproape exclusiv în intestinul subțire. Intestinul este un organ extrem de activ din punct de vedere metabolic și extrage ~40%-50% din aminoacizii disponibili din masa proteică ingerată în primul rând în scopul producerii de energie și pentru sinteza locală a proteinelor. Restul (~50%) de aminoacizi este eliberat în vena portă hepatică înainte de a fi absorbite de ficat. La fel ca intestinul, ficatul folosește aminoacizi pentru metabolismul local, dar mai degrabă decât aminoacizii oxidanți, o proporție semnificativă de aminoacizi sunt utilizati în schimb pentru sinteza proteinelor din sângele hepatic și derivate din ficat. Aminoacizii care au fost sechestrați de țesuturile splanhnice și de ficat sunt „eliminați prin prima trecere” și prin urmare, nu sunt disponibili pentru metabolismul periferic. Este interesant de observat că aminoacizii cu lanț ramificat (BCAA), care sunt implicați în anabolismul mușchilor scheletici, sunt catabolizați într-o măsură relativ mică de ficat datorită conținutului scăzut de enzimă aminotransferază cu lanț ramificat din hepatocitele umane.
O cantitate disproporționată (față de compoziția proteinei ingerate) de aminoacizi eliberați din patul splanhnic în vena hepatică sunt prin urmare, BCAA. În general, ~50% din aminoacizii dintr-o masă care conține proteine sunt extrași de țesuturile splanhnice, în timp ce restul sunt eliberați în circulația plasmatică pentru utilizare extra-splanhnic. Deși mușchiul scheletic este un depozit mare pentru reținerea aminoacizilor, nu toți aminoacizii eliberați în plasmă sunt destinați să fie încorporați în noul țesut muscular scheletic. Într-un studiu recent care folosește o abordare a trasorului etichetat intrinsec, Groen și colegii săi au demonstrat că numai ~ 2,2 g sau 11% din aminoacizii furnizați bărbaților tineri într-un bolus de 20 g de cazeină au fost utilizați pentru sinteza proteinelor de novo, în ciuda ~55. % disponibilitate in circulatia periferica in urma extractiei splanhnice. Aminoacizii rămași sunt catabolizați și servesc drept substrat pentru o serie de procese metabolice de la producerea de energie și sinteza ureei și într-o măsură foarte mică, producția de neurotransmițători (a se vedea Figura 1 pentru o prezentare generală). Cu toate acestea, este important să recunoaștem că stările de boală, precum și vârsta pot modifica cinetica metabolismului aminoacizilor după ingestia de proteine. Cercetările viitoare ar trebui să se concentreze pe determinarea modului în care factori precum tipul proteinei, vârsta și eventual, microbiota intestinală interacționează pentru a influența împărțirea aminoacizilor și în special modul în care acești factori se schimbă în contextul exercițiului de rezistență.
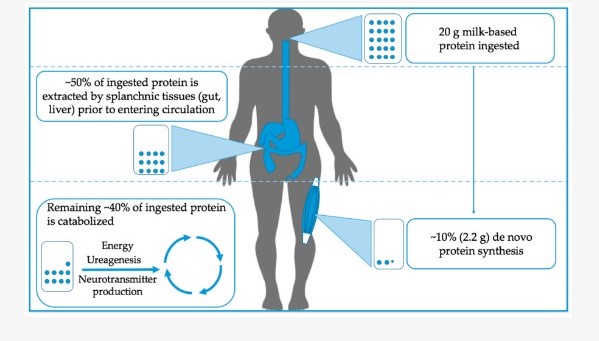
Figura 1. Prezentare generală simplificată a utilizării proteinelor orale în întregul corp în repaus. Din proteina ingerată, aproximativ 50% este extrasă de țesuturile splanhnice înainte de a intra în circulația periferică. Interesant este că doar ~ 10% din proteina ingerată este utilizată pentru sinteza proteinelor musculare scheletice, în timp ce restul este catabolizat.
Proteinele de calitate inferioară, cum ar fi proteinele din soia sau din grâu, din care lipsesc sau au un conținut scăzut de unul sau mai mulți aminoacizi esențiali, nu reușesc să stimuleze MPS în aceeași măsură ca sursele de calitate superioară, iar aminoacizii constituenți ar putea deveni, probabil mai puțin îmbogățiți în țesutul muscular la aceeași doză relativă. Indiferent de sursa de proteine, creșterea indusă de hrănire a concentrațiilor plasmatice de aminoacizi determină absorbția prin membrana musculară. Unele dovezi sugerează că ingestia de proteine induce expresia genică a mai multor proteine de transport de aminoacizi care pot crește influxul de aminoacizi în mușchiul scheletic. După o hiperaminoacidemie substanțială, există o întârziere de ~ 30 de minute în stimularea MPS înainte de a atinge vârful la 2 ore. Este important că activarea MPS indusă de aminoacidemie este tranzitorie și MPS revine la nivelurile bazale după ~2-3 ore, în ciuda hiperaminoacidemiei continue. Acest fenomen, care a fost coraborat în studiile care utilizează atât perfuzia de aminoacizi, cât și ingestia orală de proteine în bolus, a fost inventat efectul „plin de mușchi” și explică de ce pur și simplu consumul de proteine în absența activității contractile nu reușește să induce retenția de proteine și hipertrofie musculară. Stimularea MPS ca răspuns la hiperaminoacidemie pare a fi condusă în întregime de aminoacizii esențiali conținuti în proteine, iar dintre acești aminoacizi, leucina este agonistul principal al aminoacizilor. Deși este adevărat că leucina este capabilă să stimuleze MPS în absența altor aminoacizi, trebuie subliniat că sinteza proteinelor va deveni în cele din urmă limitată de disponibilitatea altor aminoacizi esențiali.
Cu toate acestea, îmbogățirea unei proteine de calitate inferioară cu leucină, cu condiția să fie prezentă și o completare de aminoacizi esențiali, poate induce o stimulare comparabilă a MPS cu cea observată în sursa de calitate superioară. Indiferent, faptul că platourile MPS în ciuda hiperaminoacidemiei susținute sugerează că MPS este un proces saturabil și că aminoacizii peste anumite cantități nu oferă nicio stimulare suplimentară. În acest sens, Moore și colab. a arătat că 0,24 g/kg (±0,06 g/kg; 95% interval de încredere (IC)) masa corporală de proteine a stimulat ratele maxime de MPS la bărbații mai tineri, dar ~0,40 g/kg (±0,19 g/kg; 95% CI; ) masa corporală de proteine este necesară la adulții în vârstă pentru a obține o stimulare comparabilă a MPS: 0,056%/h față de 0,058%/h la adulții mai în vârstă și respectiv mai tineri. Astfel, se recomandă ca dozele pe masă să fie cu ~68% mai mari la persoanele în vârstă pentru a atinge niveluri similare de MPS.
Știm că exercițiile fizice sensibilizează mușchiul la hiperaminoacidemie, ceea ce sugerează că exercițiile fizice obișnuite ar deplasa curba doză-răspuns la stânga și ar fi necesare aporturi mai mici de proteine pentru a stimula MPS; cu toate acestea, se poate ca exercițiul să mărească și capacitatea de utilizare a aminoacizilor, astfel încât câștigul maxim în MPS poate necesita aporturi mai mari de proteine. În ceea ce privește recuperarea după exercițiu, Witard și colegii au folosit un model de exercițiu unilateral pentru a cerceta diferențele dintre ratele MPS în odihnă și stimulate de efort și au făcut observații similare ca Moore și colab. la măsurarea sintezei proteinelor specifice miofibrilare la bărbați tineri li s-au administrat doze titrabile de proteină din zer (vezi Figura 2 pentru creșterea relativă a MPS la fiecare doză de proteină). Foarte important, Moore și Witard au observat că dozele de proteine peste ~ 20 g (echivalent cu ~ 0,24 g/kg de masă corporală per masă) au dus la o stimulare suplimentară neglijabilă a MPS, astfel încât 40 g de proteine nu au furnizat o îmbunătățire semnificativă statistic a ratelor de MPS fie în repaus, fie după exerciții de rezistență. În schimb, așa cum ar fi de așteptat oxidarea leucinei a crescut atunci când doza de proteine a depășit 20 g sau a existat o conversie îmbunătățită a fenilalaninei în tirozină, o creștere a producției și concentrației de uree în plasmă.
Este important de remarcat faptul că punctele de timp pentru achiziția biopsiei din investigațiile menționate mai sus au permis doar măsurători MPS pe o perioadă de ~4 ore după exercițiu; totuși, MPS cumulativ pe parcursul unei zile influențează de asemenea, acumularea proteinei miofibrilare. Prin urmare, poate fi mai important să se ia în considerare strategia de dozare a proteinelor care maximizează MPS în timpul orelor de veghe, mai degrabă decât la o singură masă. Areta și colegii săi au demonstrat că aportul de 20 g de proteine din zer administrat la fiecare ~3 ore a fost mai eficient în stimularea MPS pe o perioadă de 12 ore după exercițiul bilateral al picioarelor decât dozele echivalente cu proteine administrate ca pulsuri mai mici și mai frecvente (10 g la fiecare 1,5 ore). ), sau bolusuri mai mari consumate mai rar (40 g la 6 ore). Având în vedere că studiile menționate mai sus au măsurat MPS folosind perfuzii cu izotopi stabili într-un cadru controlat de laborator, cercetările viitoare ar trebui să reproducă aceste studii în condiții de viață liberă folosind oxid de deuteriu pentru a surprinde influența tiparelor normale de alimentație zilnică asupra MPS. Cumulativ, aceste constatări sugerează că ~ 20 g de proteine de înaltă calitate (sau ~ 0,3 g/kg/masă) sunt suficiente pentru a stimula maxim MPS după o singură masă și atunci când sunt administrate în mod repetat la 3 ore distanță, pentru a optimiza MPS pe parcursul zilei.
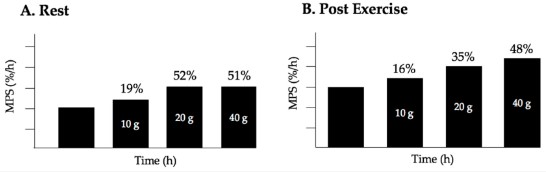
Figura 2. Creșterea MPS indusă de ingestia de proteine din zer la bărbați tineri, modificare procentuală de la 0 g. (A) În repaus, consumul a 10 g sau 20 g de proteine are ca rezultat o creștere de 19% și, respectiv, 52% de la 0g. Consumul a 40 g de proteine din zer nu are ca rezultat stimularea superioară a MPS dincolo de consumul de 20 g; (B) În urma exercițiilor de rezistență, consumul de 20 g de proteine crește MPS aproape de două ori mai mult decât consumul de 10 g, în timp ce consumul de 40 g de proteine din zer are ca rezultat o mică stimulare a MPS peste cea observată la 20 g, ceea ce indică faptul că există sunt randamente descrescătoare în ceea ce privește stimularea MPS peste 20 g. Date retrase de la Witard și colab., cu toate acestea, date similare sunt raportate de MacNaughton și colab. și Moore și colab.
Un studiu recent cu două doze, realizat de MacNaughton și colegii săi, a detectat o stimulare semnificativă statistic cu 19% mai mare a MPS în urma exercițiilor de rezistență a întregului corp la bărbații tineri care consumă 40 g de proteine, comparativ cu cei care consumă 20 g. Pentru a plasa această constatare în context, stimularea adăugată observată la ingerarea a 40 g în comparație cu 20 g de proteine de către Moore și Witard (care au măsurat, de asemenea, răspunsurile la proteine mai mici și zero) a fost de 11%, respectiv 13%. Având în vedere că singura diferență semnificativă între designul experimental folosit de MacNaughton și cele utilizate de Moore și Witard a fost protocolul de exerciții (corp întreg vs. unilateral), aceste date sugerează că bărbații tineri care efectuează exerciții de rezistență pentru întregul corp pot opta pentru a ingera cantități mai mari de proteine decât cei care efectuează exerciții pentru a maximiza anabolismul muscular. Cu toate acestea, creșterea progresivă în masă musculară ar părea a fi marginală și probabil să nu aibă o relevanță mare pentru persoanele care fac exerciții recreaționale. În cele din urmă, deoarece MacNaughton și colab. au testat doar două aporturi de proteine (20 g și 40 g), nu se știe dacă un aport între aceste două niveluri (de exemplu, 30 g) ar fi putut duce la o stimulare similară a MPS. În plus, nu a fost posibil în acest studiu să se determine un răspuns real la doză și astfel să se determine robustețea diferenței mici dintre MPS la 20 g și 40 g de proteină. Aporturile zilnice de proteine recomandate sunt specifice masei corporale, iar sportivii mai grei vor avea nevoie cantitativ de mai multe proteine decât sportivii mai ușori la fiecare masă pentru a-și îndeplini cerințele zilnice. Cu toate acestea, chiar și un atlet de 100 kg își poate satisface necesarul zilnic de proteine consumând ~ 30 g de proteine la fiecare masă, ceea ce se aliniază cu recomandările per masă de 0,24–0,30 g/kg (inclusiv intervalul de încredere superior al 95-lea) susținute de Moore. et al. Astfel, este important să se ia în considerare variabile contextuale, cum ar fi masa corporală și modalitatea de exercițiu atunci când se optează pentru strategii de dozare a proteinelor.
Mai recent, ingerarea de proteine înainte de somn a strâns un interes semnificativ, deoarece este legată de recuperarea după etape succesive de exerciții de rezistență. Adulții cu vârsta cuprinsă între 18 și 64 de ani dorm în medie aproximativ 7 ore în fiecare noapte, ceea ce face ca perioada de peste noapte să fie cea mai lungă perioadă postabsorbtivă a zilei dacă se consideră că ultima masă poate fi consumată cu 3-4 ore înainte de somn. Până de curând s-a acordat puțină atenție perioadei de somn de peste noapte; cu toate acestea, în contextul stimulării MPS, o rețetă optimă pentru ingestia de proteine ar include ceva care ar putea compensa NPB negativ după postul de peste noapte. Într-un studiu de demonstrare a principiului, Groen și colab. a demonstrat că administrarea nazogastrică a 40 g de proteină(cazeină) a stimulat eficient MPS și a îmbunătățit echilibrul proteic al întregului corp pe parcursul unui somn peste noapte de 7 ore. Această constatare este deosebit de relevantă în cazul sportivilor și adulților activi din punct de vedere recreațional care pot face exerciții fizice în timpul serii și prin urmare, pot consuma suplimente de proteine imediat înainte de a dormi. Dovezi limitate au arătat că ingestia de ~ 20 g de proteine, care maximizează MPS la fiecare masă în timpul orelor de veghe, poate fi incapabilă să îmbunătățească anabolismul proteinelor musculare peste noapte într-o măsură semnificativă. Cu toate acestea, este posibil ca lipsa efectului proteinei asupra anabolismului muscular peste noapte observată de Beelen și colegii să se fi datorat unei eliminări din perioada lungă de încorporare a trasorului (9 ore).
Același grup a demonstrat mai târziu o creștere semnificativă cu 22% a MPS mixte peste noapte la bărbații tineri care au ingerat 40 g de cazeină imediat înainte de culcare. De asemenea, s-a demonstrat recent că aceeași doză consumată după exercițiu stimulează MPS peste noapte cu 30% mai mult decât aceeași doză de proteine consumată fără efectuarea anterioară a exercițiilor de rezistență. Această constatare sugerează că sensibilizarea mușchilor scheletici la aportul de aminoacizi indusă de efort se extinde în perioada de recuperare peste noapte. Examinat pe o perioadă cronică, ingestia înainte de somn a 27,5 g de proteină cazeină (ca un amestec de proteine intact cu hidrolizat) a crescut câștigurile în aria secțiunii transversale a cvadricepsului, aria secțiunii transversale a fibrelor de tip II și suma mai multor evaluări 1-RM comparate celor care participă la același protocol de exerciții fără ingerare de proteine înainte de somn. Este important de remarcat faptul că deși Snijders și colegii au ajuns la concluzia că suplimentarea cu proteine înainte de somn a îmbunătățit creșterea zonei transversale a cvadricepsului în comparație cu aportul placebo, nu a existat nicio diferență în acumularea masei corporale slabe între grupurile cu antrenament de rezistență. În mod cumulativ, aceste date sugerează că proteina cazeină consumată înainte de somn reprezintă o strategie eficientă pentru a promova anabolismul mușchilor scheletici, dar că dozele de proteine înainte de somn ar putea trebui să fie ceva mai mari decât cele recomandate în timpul zilei, pare a fi în intervalul de ~30-40 g.
O meta-analiză și o meta-regresie recentă efectuate de laboratorul nostru au demonstrat că suplimentarea cu proteine este suficientă pentru a optimiza câștigurile induse de antrenamentul de rezistență în masă fără grăsimi. Într-adevăr, Morton și colab. a demonstrat că suplimentarea cu proteine în timpul antrenamentului de rezistență pentru ≥6 săptămâni a crescut acumularea de masă slabă cu 27% (~0,3 kg) în medie, ceea ce este similar cu o meta-analiză efectuată anterior (de exemplu, ~0,7 kg; ). Într-o analiză a punctului de pauză, am demonstrat, de asemenea, că dincolo de un aport zilnic de proteine de 1,6 g/kg/zi (1,0–2,2; 95% CI), suplimentarea cu proteine nu a reușit să sporească hipertrofia musculară indusă de efortul de rezistență. Deși momentul, doza și sursa pot influența eficacitatea suplimentării cu proteine asupra MPS, meta-analiza noastră a arătat că aceste variabile nu se traduc neapărat într-o creștere musculară îmbunătățită într-un cadru de exerciții cronice. Mai degrabă, un aport zilnic de proteine de ~1,6 g/kg/zi sau până la 2,2 g/kg/zi pare a fi factorul cel mai influent de luat în considerare atunci când obiectivul este optimizarea creșterii masei musculare cu exerciții de rezistență. Acest aport zilnic de proteine ar putea fi realizat prin încorporarea de surse de proteine de înaltă calitate la fiecare masă pe parcursul zilei și dacă este necesar, prin completarea dietei cu suplimente proteice de înaltă calitate (adică zer sau cazeină).
3. Inhibarea proteolizei indusă de proteine: un lucru bun pentru creșterea acreției musculare de proteine?
Exercițiul de rezistență are ca rezultat leziuni ale mușchilor scheletici care compromit integritatea arhitecturală a miofibrilei. Daunele pot fi induse mecanic, așa cum se evidențiază prin z-disk streaming, sau se pot manifesta ca carbonilare crescută a proteinelor, indicând stresul oxidativ indus de efort. Este probabil ca deteriorarea musculară indusă de efort să stimuleze o creștere a MPB care este observată în urma exercițiilor de rezistență. Din punct de vedere fiziologic, este necesară o creștere acută a MPB pentru a demonta și a repara proteinele deteriorate și pentru a ajuta la restabilirea funcției musculare. În starea postabsorbtivă, proteoliza musculară are ca rezultat eliberarea de aminoacizi în rezervorul liber intramuscular pentru utilizare ulterioară de către mașina de sinteză a proteinelor (adică, reciclarea intracelulară), susținând astfel MPS în absența aportului de proteine exogene. Teoretic, acest răspuns de remodelare după sesiuni succesive de exerciții de rezistență servește ca un mecanism eficient pentru a reduce daunele ulterioare induse de efort. Un studiu recent realizat de Damas și colegii săi a arătat că o perioadă neobișnuită(noutate) de exerciții de rezistență la bărbații tineri a dus la fluxul de disc z și edem indus de umflături, indicând prezența leziunilor musculare. Mai mult decât atât, ratele MPS s-au dovedit a fi cele mai mari în urma cursului inițial al unui antrenament neobișnuit decât după finalizarea aceluiași ciclu de exerciții, după 3 și 10 săptămâni de antrenament cu exerciții de rezistență. Important, atunci când răspunsul MPS acut a fost normalizat la magnitudinea fluxului de disc z la fiecare fază relativă a studiului, nu au existat diferențe detectabile în MPS. Această descoperire sugerează că în timpul perioadei timpurii de antrenament de rezistență, MPS este puternic stimulat pentru a facilita repararea și remodelarea daunelor proteice induse de efort. Pe măsură ce are loc tranziția țesutului muscular de la exercițiu simplu la „antrenat de rezistență”, MPS a fost redus adaptiv și direcționat mai degrabă către remodelarea miofibrilară decât către o remodelare globală a tuturor fracțiilor de proteine musculare. În consecință, antrenamentul atenuează răspunsul MPS la exercițiul de rezistență. Laboratorul nostru a arătat, de asemenea, că bărbații tineri care au efectuat antrenament de rezistență unilateral timp de 8 săptămâni au avut o stimulare mai pronunțată a MPS în membrul lor antrenat față de membrul lor neantrenat la 4 ore după terminarea exercițiului; totuși, MPS a revenit la nivelurile bazale la 28 de ore după exercițiu numai în membrul antrenat.
Propunem ca MPB să urmeze un declin adaptativ similar cu antrenamentul de rezistență caracterizat printr-o stimulare robustă în urma primei perioade de exerciții neobișnuite pentru a iniția remodelarea globală, urmată de o scădere adaptativă cu antrenament. În mod analog, conținutul de enzime antioxidante crește dintr-o stare neantrenată în urma antrenamentului de rezistență, care la rândul său, poate reduce daunele oxidative induse de efort. Luate împreună, creșterea turnover-ului proteic pare să fie necesară, mai ales în perioada timpurie de antrenament de rezistență, pentru a facilita remodelarea mușchilor scheletici și pentru a pune bazele pentru acumularea ulterioară a proteinelor musculare cu antrenament progresiv. Impactul suprimării acestei creșteri normale a MPB nu este cunoscut, totuși pare puțin probabil, în estimarea noastră, să se traducă într-un beneficiu fiziologic. Două intervenții nutriționale capabile să suprime MPB, îmbunătățind astfel echilibrul net proteic, includ creșterea concentrațiilor sistemice de insulină prin ingestia de carbohidrați și/sau prin suplimentarea cu doze mai mari de proteine (decât sunt necesare pentru a stimula maxim MPS).
În modelele preclinice de rozătoare, insulina stimulează MPS, cu toate acestea, la om, concentrațiile de insulină peste ~5 UI/ml nu par să stimuleze MPS. Într-o meta-analiză recentă, s-a concluzionat că insulina este doar permisivă pentru stimularea MPS și reglează predominant anabolismul muscular prin influența sa inhibitoare asupra MPB. Chiar și creșteri moderate ale insulinei plasmatice care pot fi realizate prin consumul unei mese mixte sau a unei băuturi proteice sunt suficiente pentru a reduce MPB cu ~50%, fără suprimare suplimentară la concentrații de insulină peste ~30 mU/L. Prin urmare, nu este surprinzător faptul că investigațiile care au asociat aportul de carbohidrați și proteine după exercițiu nu au reușit să observe un răspuns anabolic superior în comparație cu ingestia de proteine în monoterapie. Trivialitatea carbohidraților în creșterea anabolismului muscular a fost demonstrată de Staples și colab. , care nu a reușit să detecteze o stimulare mai mare a MPS sau o suprimare mai mare a MPB atunci când 50 g de carbohidrați au fost adăugate la o doză de 25 g de proteină din zer atunci când au fost evaluate doar față de 25 g de proteine, în ciuda semnalizării anabolice îmbunătățite și al insulinemiei substanțial mai mare. Astfel, coingestia de carbohidrați cu proteine nu sporește efectul anabolic al proteinelor și nu contribuie la un potențial hipertrofic mai mare în urma exercițiilor de rezistență. Cu toate acestea, având în vedere că proteinele sunt în mod obișnuit ingerate ca o masă mixtă, este prudent să menționăm că carbohidrații nu afectează răspunsul anabolic la proteine, în ciuda creșterii retenției splanhnice a aminoacizilor și a încetinirii ratei cu care aceștia intră în circulația sistemică. Mai mult decât atât, ingerarea carbohidraților restabilește glicogenul muscular în urma exercițiilor fizice exhaustive și prin urmare, poate fi importantă pentru recuperarea performanței într-un cadru atletic.
Aportul de aminoacizi la niveluri suficient de ridicate (~70 g) pare, de asemenea, să inhibe proteoliza într-o manieră independentă de insulină. Teoretic, continuând să ingereze aminoacizi dincolo de punctul în care MPS este stimulat maxim (adică, 20–30 g la adulții tineri sănătoși), concentrațiile intracelulare de aminoacizi cresc și inhibă MPB mai degrabă decât stimularea în continuare MPS și prin extensie, promovează un NPB mai mare. Kim şi colab. au sugerat că concentrarea exclusivă pe MPS pentru a genera recomandări cu privire la doza de proteine necesară pentru a optimiza răspunsul anabolic la o masă neglijează contribuția pe care ar avea-o suprimarea proteolizei la promovarea unui NPB mai pozitiv. Ei susțin că, în timp ce datele generate din laboratorul lor coroborează constatarea că ~25 g de proteine de înaltă calitate maximizează răspunsul MPS în repaus sau după exerciții fizice, cantități mai mari de proteine promovează o NPB progresiv mai mare a întregului corp, în primul rând prin suprimarea întregului corp (notă: MPB nu a fost măsurat) prin degradarea proteinelor. Pentru a oferi dovezi experimentale care să susțină teza lor, Kim și colab. a comparat recent răspunsul anabolic de 40 g față de 70 g de proteine, sub formă de chifle de vită, fie în repaus, fie în urma unui exercițiu de rezistență exhaustiv pe NPB. În timp ce sinteza proteinelor specifice mușchilor a fost crescută într-o măsură similară în ambele grupuri, NPB a fost mai pozitivă în grupul cu proteine mai multe datorită unei suprimări mai mari a defalcării proteinelor întregului corp și unei creșteri mai mici, deși semnificative, a sintezei proteinelor în întregul corp. Având în vedere că mușchiul scheletic poate constitui ~ 25% din proteoliza întregului corp, este posibil ca 70 g de proteină să suprima MPB, totuși, o astfel de speculație necesită investigații suplimentare. Într-un alt studiu, efectuat de același grup, s-a demonstrat că a existat o relație liniară pozitivă între aportul de proteine din ce în ce mai mare (de la ~6 g la 92 g) și NPB pentru întregul corp, ceea ce i-a determinat pe autori să concluzioneze că nu există o limită superioară practică în ceea ce privește cantitatea de proteine care ar putea maximiza anabolismul muscular; cu toate acestea, încă o dată răspunsurile măsurate nu au fost specifice mușchilor.
În timp ce consumul de cantități mai mari de proteine pe masă decât ceea ce recomandăm aici (adică, ~20–30 g/masă) poate suprima proteoliza, vedem puține dovezi care să susțină strategiile care urmăresc să suprime în mod specific MPB după exercițiul de rezistență datorită rolului. MPB ar juca în remodelarea proteinelor în timpul recuperării după exerciții fizice și din cauza lipsei relative de înțelegere a potențialelor consecințe ale acestui lucru. Într-adevăr, datele despre rozătoare oferă o lentilă utilă prin care să vizualizați potențialele consecințe fiziologice ale inhibării proteolizei. Cele două sisteme predominante responsabile de degradarea specifică a proteinei și macromoleculară sunt sistemele ubiquitin-proteazomal (UPS) și respectiv, autofagic-lizozomal. Eliminarea Atg7 la rozătoare, o genă critică a autofagiei, are ca rezultat o scădere cu 40% a dimensiunii miofibrelor în comparație cu tovarășii de tip sălbatic. În plus, șoarecii nuli Atg7 au o forță musculară specifică foarte afectată, probabil ca rezultat al nealinierii discului z care acționează în confluență cu carbonilarea crescută a proteinelor. Deficiențe similare au fost observate la șoarecii cărora li s-a eliminat TSC1, ducând, în consecință, la activarea susținută a mTORC1 și o inhibare cronică a Ulk-1, un activator în amonte al autofagiei. În cele din urmă, rozătoarele cu gena Rpt3 (o subunitate esențială în miezul 19S al proteazomului 26S) au fost eliminate în mod condiționat, au prezentat o durată de viață redusă, o miofibră CSA mai mică și o rezistență de prindere grav afectată. Luate împreună, munca pe animale în combinație cu datele umane existente implică puternic un rol important pentru ratele bazale de descompunere a proteinelor mediată de autofagie și UPS în menținerea viabilității mușchilor scheletici. Desigur, suprimarea MPB prin mijloace nutriționale nu este sinonimă cu suprimarea MPB de la eliminarea factorilor proteolitici cheie și este improbabil ca consecințele suprimării MPB să fie de la distanță caracteristice ablației genetice. Cu toate acestea, există dovezi transversale care sugerează că chiar și diferențele moderate în reglarea proteolizei sunt legate de calitatea slabă a mușchilor și fragilitatea. De exemplu, o expresie mai scăzută a genelor implicate în autofagie, mitofagie și UPS s-a dovedit a fi asociată cu sarcopenie și funcția fizică afectată, așa cum este indicat de o masă slabă mai mică și o distanță redusă de călătorie în timpul unui test de mers de 6 minute la femeile în vârstă. Teza din spatele acestor date este că există o scădere a clearance-ului proteinelor pliate greșit și/sau agregate la indivizii cu flux de autofagie mai scăzut, ceea ce duce la o cantitate și o calitate mai scăzută a mușchilor.
În contextul exercițiului de rezistență, rolul jucat de factorii proteolitici nu este la fel de clar. Un studiu realizat de Leger et al. a demonstrat o creștere de 10 ori și de 2,5 ori a ARNm MuRF1 și respectiv, atrogin1, în urma unui studiu de antrenament de rezistență de 8 săptămâni. Foarte important, conținutul de proteină atrogin1 a crescut cu ~40%, în ciuda faptului că participanții au înregistrat o creștere de 10% în dimensiunea mușchilor cvadriceps. Probabil, conținutul crescut de proteine atrogin1 constituie una din o serie de adaptări care apar pentru a modula descompunerea proteinelor musculare scheletice în prezența unui conținut crescut de proteine contractile și structurale, mai degrabă decât să fie implicat în atrofia musculară. Nu este clar ce efect ar avea asupra integrității mușchiului scheletic încercarea de a suprima, prin diete sau alte mijloace, această creștere indusă de exerciții fizice a conținutului de proteine atrogin1 sau o activare acută a MPB în general, asupra integrității mușchilor scheletici, dar dacă munca la rozătoare este orice indicație, degradarea proteinelor bazale este necesară pentru a asigura funcționarea optimă a mușchilor scheletici. Mai mult decât atât, suprimarea defalcării proteinelor întregului corp în urma exercițiilor fizice poate duce la acumularea tranzitorie de țesut de organ (o componentă a masei corporale slabe) mai degrabă decât hipertrofia musculară în sine, care nu poate fi ușor de deslușit din modificările masei corporale slabe derivate de DXA. Acum este nevoie de mai multe cercetări pentru a caracteriza impactul suprimării ușoare a defalcării proteinelor, atât la nivelul întregului corp, cât și la nivelul mușchilor scheletici, asupra adaptărilor fenotipice la exercițiul de rezistență. Cu toate acestea, în opinia noastră, sportivii și persoanele active din punct de vedere recreațional ar trebui să se concentreze pe practicile de maximizare a MPS mai degrabă decât a suprima MPB, ceea ce pare a fi important din punct de vedere fiziologic pentru remodelarea mușchilor scheletici în urma exercițiilor dăunătoare.
4. Aportul de proteine în timpul restricției energetice
Atunci când aportul de energie nu este suficient pentru a echilibra cheltuielile energetice, are loc o scădere a masei corporale totale. Aceste perioade de restricție energetică pot fi invocate în mod voluntar, așa cum este cazul sportivilor care concurează în evenimente și competiții cu restricție de masă corporală care se concentrează pe estetica musculară (adică, culturism), sau pot fi de natură involuntară, cum ar fi în timpul operațiunilor militare. În general, un deficit energetic poate fi atins fie prin restricție calorică, fie printr-o combinație între acestea, sau o creștere cronică a nivelurilor de activitate fizică (fără o creștere compensatorie a aportului de energie). La persoanele supraponderale și obeze, pierderea de masă corporală care urmează după un deficit energetic prelungit conferă, în general, beneficii fizice și metabolice pentru sănătate, cum ar fi o sensibilitate îmbunătățită la insulină a mușchilor scheletici și hepatic, precum și îmbunătățiri ale funcției celulelor beta. Cu toate acestea, o consecință îngrijorătoare a restricției energetice este că greutatea pierdută este compusă, în general, dintr-o pierdere de 25% a masei corporale slabe (LBM), din care o proporție semnificativă este mușchiul scheletic. Această pierdere a masei musculare scheletice ar putea duce ulterior la reduceri ale performanței și la o susceptibilitate crescută la accidentări. Astfel, indiferent de cauza precedentă a deficitului energetic, poate fi important pentru sportivi să se depună eforturi pentru a asigura menținerea LBM.
Sunt tot mai multe dovezi care sugerează că o reducere a MPS postabsorbtivă și postprandială contribuie și poate fi principalul mecanism de adaptare care conduce la pierderea LBM în timpul restricției energetice. În urma unui deficit energetic de ~20%, ratele postabsorbtive ale MPS au fost reduse cu ~19% în comparație cu măsurătorile efectuate în timpul menținerii masei corporale. Această scădere a MPS a fost probabil precipitată de o semnalizare anabolică intramusculară redusă, așa cum demonstrează o fosforilare cu ~35% și 30% mai mică a AktSer473 și respectiv 4E-BP1Thr37/46. Având în vedere că MPS este un proces care necesită energie, scăderile observate în timpul restricției calorice reprezintă probabil un mecanism orientat spre conservare pentru a evita utilizarea ineficientă a ATP pentru procesele de promovare a creșterii atunci când disponibilitatea alimentelor este scăzută. În conformitate cu această teză, reducerile MPS apar rapid după debutul privării alimentare. De exemplu, Areta et al. a observat o reducere de ~27% a sintezei proteinelor miofibrilare după doar 5 zile de restricție energetică la bărbați și femei. Pe măsură ce restricția energetică este prelungită, modificările MPS par să se stabilizeze la un nivel adecvat abundenței de nutrienți predominanti.
Modul exact în care ratele MPB se schimbă ca răspuns la restricția energetică este mai puțin caracterizat, în special din cauza dificultății de a aplica metodele disponibile în prezent pentru cuantificarea MPB. Carbone și colegii săi au investigat modificările markerilor moleculari ai MPB pentru a deduce dinamica proteolizei musculare ca răspuns la o dietă cu restricții energetice de ~ 40%. Ei nu au reușit să demonstreze nicio modificare în activitatea proteolitică proteozomală 26S, dar au observat o creștere de 1,2 și 1,3 ori a MuRF1 și respectiv ARNm atrogin1. Aceste observații i-au determinat pe autori să speculeze că MPB este crescut ca răspuns la restricția energetică. Mai târziu, același grup a arătat că rata de defalcare fracțională a fost crescută cu ~60% peste nivelurile bazale după 10 zile de deficit energetic, cu o mică creștere concomitentă a caspazei-3 într-un grup de cicliști foarte activi. Aceste constatări sunt în contradicție cu constatările din laboratorul nostru ca răspuns la o intervenție alimentară comparabilă. Hector și colab. au expus 24 de participanți supraponderali la o perioadă de 10 zile de restricție calorică de 40% (în raport cu cerințele energetice) și nu au găsit modificări semnificative în MPB sau vreun marker static al proteolizei musculare. Observațiile disparate ale lui Carbone și colab. şi Hector şi colab. care prezintă o rată ridicată și o rată neschimbată a MPB sunt greu de reconciliat; cu toate acestea, acestea se pot datora diferitelor populații de studiu (adulți activi în Carbone și colab. și adulți supraponderali în Hector și colab.). Cu toate acestea, susținem că există o scădere compensatorie a proceselor consumatoare de energie în perioadele de restricție calorică. Proteoliza musculară, care se realizează în primul rând prin degradarea mediată de UPS, depinde în mare măsură de ATP pentru a alimenta conjugarea și legarea moleculelor de ubiquitină pe un substrat țintă. În plus, capacul strâns 19S al complexului proteazomal 26S interzice proteinelor pliate să intre în miezul catalitic 20S. Prin urmare, fiecare etapă ulterioară de descompunere a proteinelor depinde de suficientă energie. Autofagia joacă, de asemenea, un rol cheie în defalcarea macromoleculară în condiții de privare de energie, cu toate acestea, domeniul de aplicare al revizuirii actuale exclude o discuție detaliată în acest sens. Având în vedere costul ridicat al energiei MPB, propunem că este puțin probabil ca restricția energetică să crească MPB în măsura observată de Carbone și colab. Luate împreună, eforturile de combatere a pierderii LBM în perioadele de restricție energetică ar fi cele mai fructuoase prin folosirea strategiilor care minimizează scăderile MPS.
Strategiile care s-au dovedit eficiente în menținerea sau chiar creșterea LBM în perioadele de restricție energetică includ practicarea exercițiilor de încărcare și într-o măsură mai mică, creșterea aportului zilnic de proteine. În timpul echilibrului energetic, așa cum am discutat mai sus, aportul zilnic de proteine de 1,6 g/kg/zi maximizează potențialul hipertrofic al mușchilor scheletici în urma unei intervenții de antrenament de rezistență. În condiții de restricție energetică, totuși, o proporție relativă mai mare de aminoacizi sunt catabolizați pentru producerea de energie, rezultând mai puțini aminoacizi disponibili pentru anabolismul muscular. S-ar putea susține că prin creșterea aportului de proteine în perioadele cu restricții calorice, producția de energie poate fi susținută păstrând în același timp MPS. Într-adevăr, Pasiakos și colab. a măsurat MPS ca răspuns la o masă bogată în proteine înainte și după 21 de zile cu un deficit de energie de 40%, obținut printr-o restricție calorică de 30% în combinație cu o creștere cu 10% a exercițiilor aerobe. Autorii au demonstrat că doar participanții care consumau 1,6 g/kg/zi (de două ori doza alimentară recomandată pentru proteine-DZR) și 2,4 g/kg/zi (de 3 ori RDA) și-au păstrat sensibilitatea anabolică la proteine. În schimb, grupul care consuma RDA (0,8 g/kg/zi) pentru proteine a avut un răspuns MPS suprimat la ingestia de proteine după ce a fost într-un deficit energetic. Grupul care consumă RDA a pierdut, de asemenea, substanțial mai multă masă totală ca masă fără grăsimi, în comparație cu cei care consumă de 2 sau 3 ori RDA pentru proteine. În ciuda păstrării sensibilității anabolice la o masă care conținea proteine, chiar și participanții care consumau proteine la niveluri mai mari decât RDA pentru proteine au experimentat pierderi semnificative de LBM. Luate împreună, aceste date sugerează că doar aportul de proteine este insuficient pentru a menține LBM în timpul restricției energetice.
Angajarea în exerciții de rezistență în timpul unui deficit de energie are un efect economisitor asupra LBM. Într-adevăr, LBM a fost menținut după o dietă cu restricții energetice de 4 săptămâni la indivizii care s-au antrenat 6 zile pe săptămână și au consumat 1,2 g/kg/zi de proteine, un aport zilnic de proteine care sa presupus a fi insuficient pentru a preveni scăderea LBM în absența exercițiului fizic. Mai mult, participanții care au consumat 2,4 g/kg/zi de proteine (de 3 ori RDA) împreună cu același regim de exerciții de 6 zile/săptămână și-au crescut LBM în perioada de 4 săptămâni. Areta și colab. au raportat că exercițiul de rezistență a restabilit scăderea de ~27% observată în MPS postabsorbtiv în timpul restricției energetice și atunci când este asociat cu ingestia de proteine, a îmbunătățit semnificativ MPS peste valorile obținute în balanța energetică. Folosind ingestia de oxid de deuteriu, am demonstrat, de asemenea, o conservare a sintezei integrate a proteinelor miofibrilare, care a fost observată doar la participanții care consumau 2,4 g/kg/zi de proteine. Este important de remarcat faptul că am studiat o populație supraponderală și prin urmare, aceste constatări pot să nu fie aplicabile subiecților mai slabi care trec prin perioade de restricție energetică și care în ciuda aportului mai mare de proteine, pot fi în imposibilitatea de a reține LBM. O meta-analiză a demonstrat că subiecții mai slabi cu experiență de antrenament de rezistență au fost mai vulnerabili la pierderi în LBM decât indivizii neadaptati la exerciții fizice cu un procent mai mare de grăsime corporală. Astfel, sportivilor care tind să fie mai slabi decât populația generală și care au mai multă experiență de antrenament, li s-a recomandat să consume aporturi de proteine de peste ~3 g/kg/zi în încercarea de a preveni pierderile de LBM în timpul restricției de energie. Este important de remarcat, totuși, că aportul de proteine necesar pentru a compensa reducerile LBM depinde probabil mai mult de severitatea restricției energetice și de cantitatea de exerciții de rezistență efectuate în mod obișnuit. Cu toate acestea, exercițiul de rezistență atunci când este efectuat împreună cu consumul unui aport mai mare de proteine este eficient pentru atenuarea pierderilor și pentru a conduce la menținerea sau pentru a permite acumularea LBM, în timpul restricției de energie.
Pe lângă necesarul de proteine, este important să se ia în considerare și efectul de sațietate al proteinelor. Mulți sportivi care concurează în sporturi înclinate din punct de vedere estetic (adică, culturism) încep să țină dietă agresiv cu 8-16 săptămâni înainte de competiție. Aceste perioade sunt adesea caracterizate de deficite calorice pronunțate care vizează reducerea grăsimii corporale la niveluri foarte scăzute, păstrând în același timp cea mai mare proporție de masă musculară posibilă. Succesul unui atlet în această perioadă se bazează pe capacitatea sa de a adera în mod cronic la o dietă cu restricții calorice. Astfel, maximizarea efectului de sațietate al fiecărei mese este primordială în aceste perioade prelungite de restricție energetică. Proteina este cel mai satios macronutrient si prin urmare, ar trebui sa fie piatra de temelie a oricarui plan de slabire; cu toate acestea, nu toate sursele de proteine modulează nivelul de foame și de sațietate în același grad. În situații acute, în care un mic dejun compus în principal din proteine din zer a fost comparat cu proteina cazeină, foamea a fost suprimată într-o măsură mai mare la participanții care consumau proteine din zer.
Acest efect se poate datora parțial eficacității proteinei din zer de a stimula o secreție mai pronunțată a hormonului care induce sațietatea peptidei asemănătoare glucagonului-1 (GLP-1) în comparație cu cazeina. Interesant, acest efect poate fi determinat de rolul inhibitor pe care îl are proteina din zer asupra dipeptidil peptidazei IV, enzima responsabilă pentru degradarea GLP-1 activ. Prin prevenirea degradării GLP-1 sistemic, mai mult GLP-1 rămâne activ în circulație și are un efect mai prelungit asupra sațietății. Hall şi colab. a demonstrat, de asemenea, creșteri plasmatice mai mari ale colecistokininei (CCK), un alt hormon inductor de sațietate secretat de intestin, după consumul de proteine din zer. Un CCK circulant crescut cu consumul de proteină din zer se poate datora prezenței glicomacropeptidei (GMP) care promovează secreția de CCK. În sprijinul capacității unice a GMP de a stimula eliberarea sistemică de CCK, Veldhorst și colegii săi au demonstrat un aport de energie crescut la prânz, după consumul unei mese care conține proteine din zer sărăcite în GMP, în comparație cu o proteină din zer „repletă cu GMP”.
Când perioadele de măsurare sunt prelungite și aportul alimentar ad libitum este evaluat după câteva ore, cazeina pare să fie ușor mai bună decât proteina din zer pentru suprimarea apetitului. Într-adevăr, suplimentarea cu cazeină a fost demonstrată într-un studiu că reduce aportul de energie în comparație cu suplimentarea cu zer pe parcursul unui studiu de suplimentare de șapte zile. Important este că efectele surselor individuale de proteine asupra sațietății pot fi echivalente dacă aportul de proteine este suficient de mare. Veldhorst și colab. a constatat că un mic dejun care conține proteine din zer, care oferă 10% proteine, 55% carbohidrați și 30% grăsimi, a suprimat mai eficient aportul de energie la prânz în comparație cu un mic dejun care conține proteine cazeină cu același profil de macronutrienți. Când procentul de proteine derivate din masă a fost crescut la 25% (cu o reducere corespunzătoare a grăsimilor), nu au existat diferențe observabile în aportul de energie din masa de prânz între grupele de cazeină și proteine din zer. Având în vedere că sportivii și adulții activi în recreere au nevoie de cantități mai mari de proteine pentru a menține LBM în timpul restricției energetice, diferențele observate între zer și cazeină la doze relative mai mici vor fi probabil diluate atunci când aportul de proteine este crescut. Prin urmare, asemănător sportivilor în echilibrul energetic, sportivii supuși dietelor cu restricții energetice ar trebui să se concentreze în primul rând pe îndeplinirea cerințelor zilnice de proteine (1,6–2,4 g/kg/zi) și abia apoi să se concentreze pe alte variabile relevante ale suplimentării proteice (adică, sursa de proteine și sincronizare).
5. Recomandări practice
5.1. Persoane aflate în Echilibrul Energetic
-Consumați ~0,4 g/kg de masă corporală (proteine adăugate pentru a lua în considerare influența altor macronutrienți în mese și calitatea proteinelor), pentru a stimula maxim MPS după o perioadă de repaus sau exercițiu de rezistență exhaustiv.
– Distanțarea meselor care conțin proteine ~3-4 ore pe parcursul zilei maximizează ratele MPS pe parcursul unei perioade de 12 ore (de la trezire).
– Practicați ingestia de proteine înainte de somn (1-3 ore înainte de somn) pentru a compensa scăderea MPS care ar avea loc în timpul unei perioade de post peste noapte.
-Pentru a maximiza acumularea de proteine musculare cu exerciții de rezistență, aportul zilnic de proteine ar trebui să fie de ~1,6 g/kg/zi și de până la 2,2 g/kg/zi. Acest aport poate fi realizat prin ingerarea a 3-4 mese.
5.2. Persoane în Restricție Energetică
– Necesarul zilnic de proteine este mai mare decât în perioada de echilibru energetic pentru a promova menținerea sau creșterea masei corporale slabe.
– Exercițiile de rezistență trebuie efectuate în timpul restricției energetice pentru a promova (dacă se dorește) menținerea masei corporale slabe.
-Pentru sportivii care fac „definirea” masei musculare pe o perioadă lungă de timp, ar trebui alese surse de proteine de înaltă calitate, cum ar fi zerul și cazeina sau un amestec din fiecare, pentru a optimiza controlul apetitului și pentru a asigura respectarea dietei.
-Pentru a promova menținerea masei corporale slabe în timpul pierderii în greutate, sunt susținute aporturi de proteine de ~2,3–3,1 g/kg/zi. Adulții neadaptati la exerciții fizice care au un procent mai mare de grăsime corporală ar trebui să urmărească atingerea limitei inferioare a acestui interval, în timp ce persoanele mai slabe cu experiență de antrenament de rezistență, care sunt mai vulnerabile la pierderea masei corporale slabe în timpul restricției energetice, ar putea viza nivelul superior al acestui interval.
6. Rezumat și concluzii
Corpul uman este capabil să digere cantități mari de proteine din dietă. Cu toate acestea, nu toți aminoacizii constituenți sunt utilizați de mașina de translație pentru a sintetiza noi proteine. Odată cu consumul unei surse izolate de proteine, dincolo de un aport de proteine de ~0,3 g/kg de masă corporală (adică, 0,24 plus limita superioară a IC de 95%), MPS este saturată, rata de catabolism a aminoacizilor prin oxidare si producția de uree crește și astfel sunt disponibili mai puțini aminoacizi pentru sinteza proteinelor. Persoanele care efectuează exerciții de rezistență pentru întregul corp pot necesita doze mai mari de proteine pentru a maximiza efectele anabolice ale proteinei, dar aceste efecte sunt doar marginal mai mari decât ceea ce se observă la 20 g de proteine. Având în vedere că mușchiul devine refractar la prezența aminoacizilor, astfel încât MPS revine la nivelurile bazale după ~ 3 ore în ciuda hiperaminoacidemiei susținute, mesele proteice ar trebui distantate la ~ 3-5 ore pentru a maximiza MPS în timpul perioadei de veghe. În timp ce aceste strategii s-au dovedit a fi cele mai eficiente în situații acute (adică, pe o perioadă de captură de 12 ore), cea mai importantă variabilă care determină eficacitatea suplimentării cu proteine asupra creșterii dimensiunii mușchilor în timpul antrenamentului de rezistență este încă aportul zilnic total de proteine.
Într-o mare meta-analiză, s-a demonstrat că aportul de proteine promovează câștiguri suplimentare în masa corporală slabă dincolo de cele observate doar cu exercițiile de rezistență; cu toate acestea, dincolo de un aport zilnic de 1,6 g/kg masă corporală pe zi (până la 2,2 g/kg/zi), efectele suplimentare ale proteinelor sunt mult diminuate. În loc să stimuleze în continuare MPS, aporturile mari de proteine dincolo de ceea ce recomandăm pot modula anabolismul prin suprimarea proteolizei; totuși, ne lipsesc dovezile experimentale pentru acest lucru în mușchi. Avertizăm împotriva strategiilor care se concentrează pe suprimarea MPB, deoarece susținem că îndepărtarea eficientă a proteinelor deteriorate ar necesita un răspuns proteolitic robust și complet funcțional. Nu suntem conștienți de eventuale îmbunătățiri în ceea ce privește hipertrofia mușchilor scheletici prin strategii care suprimă MPB. Astfel, sportivii din echilibrul energetic care caută să optimizeze potențialul de adaptare al programelor lor de antrenament de rezistență sunt sfătuiți să se asigure mai întâi că consumă aproximativ 1,6 g/kg masă corporală pe zi de proteine și să își adapteze strategiile de dozare pentru a îndeplini acest obiectiv general.
Perioadele de restricție energetică au ca rezultat reduceri semnificative ale masei corporale slabe. Persoanele slabe și cei cu mai multă experiență de antrenament par a fi mai susceptibili la reduceri ale dimensiunii mușchilor scheletici în comparație cu indivizii mai grei, neadaptati la antrenament. Reducerile LBM sunt determinate în primul rând de reducerile ratelor postabsorbtive ale MPS și de o sensibilitate redusă la prezența unui bolus proteic. Pentru a preveni eficient aceste scăderi ale MPS atât în perioada postabsorbtivă, cât și în perioada postprandială, s-a recomandat creșterea aportului zilnic de proteine la ~2,3–3,1 g/kg/zi, iar sportivii mai slabi ar putea dori să vizeze aportul la capătul superior al acestui interval. Participarea la exerciții de rezistență este suficientă pentru a contracara scăderile observate în MPS după o perioadă acută de restricție energetică și atunci când este asociată cu un aport suficient de proteine, poate duce la câștiguri în LBM. Astfel, această combinație de aport suficient de proteine și efectuarea regulată a exercițiilor de rezistență ar trebui să formeze piatra de temelie a oricărei diete de slăbire. Sportivii care încearcă să reducă masa corporală pentru o competiție cu câteva săptămâni înainte pot spori efectele de sațietate ale fiecărei mese și prin urmare, respectarea dietei, asigurându-se că sunt ingerate proteine de înaltă calitate. În perioadele acute, proteina din zer are efecte de suprimare a poftei de mâncare mai mari decât proteina cazeină, însă situația se inversează atunci când măsurătorile sunt obținute la câteva ore după aportul alimentar. Astfel, un atlet poate dori să consume un amestec de proteine în plus față de alte surse de alimente integrale pentru a obține o sațietate mai bună. Cu toate acestea, o astfel de strategie poate fi inutilă dacă aportul de proteine se apropie de cele necesare pentru menținerea masei musculare scheletice în perioadele de restricție energetică.
By. Bitanu-Alexandru
Referințe:
1. Thiebaud, D.; Jacot, E.; DeFronzo, R.A.; Maeder, E.; Jequier, E.; Felber, J.P. The effect of graded doses of
insulin on total glucose uptake, glucose oxidation, and glucose storage in man. Diabetes 1982, 31, 957–963.
[CrossRef] [PubMed]
2. Wang, Z.; Ying, Z.; Bosy-Westphal, A.; Zhang, J.; Schautz, B.; Later,W.; Heymsfield, S.B.; Muller, M.J. Specific
metabolic rates of major organs and tissues across adulthood: Evaluation by mechanistic model of resting
energy expenditure. Am. J. Clin. Nutr. 2010, 92, 1369–1377. [CrossRef] [PubMed]
3. Morton, R.W.; McGlory, C.; Phillips, S.M. Nutritional interventions to augment resistance training-induced
skeletal muscle hypertrophy. Front. Physiol. 2015, 6, 245. [CrossRef] [PubMed]
4. Phillips, S.M. A brief review of critical processes in exercise-induced muscular hypertrophy. Sports Med.
2014, 44, S71–S77. [CrossRef] [PubMed]
5. Phillips, S.M.; Tipton, K.D.; Aarsland, A.; Wolf, S.E.; Wolfe, R.R. Mixed muscle protein synthesis and
breakdown after resistance exercise in humans. Am. J. Physiol. 1997, 273, E99–E107. [CrossRef] [PubMed]
6. Biolo, G.; Tipton, K.D.; Klein, S.; Wolfe, R.R. An abundant supply of amino acids enhances the metabolic
effect of exercise on muscle protein. Am. J. Physiol. 1997, 273, E122–E129. [CrossRef] [PubMed]
7. McNurlan, M.A.; Garlick, P.J. Contribution of rat liver and gastrointestinal tract to whole-body protein
synthesis in the rat. Biochem. J. 1980, 186, 381–383. [CrossRef] [PubMed]
8. Nakshabendi, I.M.; McKee, R.; Downie, S.; Russell, R.I.; Rennie, M.J. Rates of small intestinal mucosal protein
synthesis in human jejunum and ileum. Am. J. Physiol. 1999, 277, E1028–E1031. [CrossRef] [PubMed]
9. Stoll, B.; Henry, J.; Reeds, P.J.; Yu, H.; Jahoor, F.; Burrin, D.G. Catabolism dominates the first-pass intestinal
metabolism of dietary essential amino acids in milk protein-fed piglets. J. Nutr. 1998, 128, 606–614. [PubMed]
10. Stoll, B.; Burrin, D.G.; Henry, J.; Yu, H.; Jahoor, F.; Reeds, P.J. Dietary amino acids are the preferential source
of hepatic protein synthesis in piglets. J. Nutr. 1998, 128, 1517–1524. [PubMed]
11. Jackman, S.R.; Witard, O.C.; Philp, A.; Wallis, G.A.; Baar, K.; Tipton, K.D. Branched-chain amino
acid ingestion stimulates muscle myofibrillar protein synthesis following resistance exercise in humans.
Front. Physiol. 2017, 8, 390. [CrossRef] [PubMed]
12. Hutson, S.M. Subcellular distribution of branched-chain aminotransferase activity in rat tissues. J. Nutr.
1988, 118, 1475–1481. [CrossRef] [PubMed]
13. Suryawan, A.; Hawes, J.W.; Harris, R.A.; Shimomura, Y.; Jenkins, A.E.; Hutson, S.M. A molecular model of
human branched-chain amino acid metabolism. Am. J. Clin. Nutr. 1998, 68, 72–81. [CrossRef] [PubMed]
14. Wahren, J.; Felig, P.; Hagenfeldt, L. Effect of protein ingestion on splanchnic and leg metabolism in normal
man and in patients with diabetes mellitus. J. Clin. Investig. 1976, 57, 987–999. [CrossRef] [PubMed]
15. Groen, B.B.; Horstman, A.M.; Hamer, H.M.; de Haan, M.; van Kranenburg, J.; Bierau, J.; Poeze, M.;
Wodzig, W.K.; Rasmussen, B.B.; van Loon, L.J. Post-prandial protein handling: You are what you just
ate. PLoS ONE 2015, 10, e0141582. [CrossRef] [PubMed]
16. Dangin, M.; Guillet, C.; Garcia-Rodenas, C.; Gachon, P.; Bouteloup-Demange, C.; Reiffers-Magnani, K.;
Fauquant, J.; Ballevre, O.; Beaufrere, B. The rate of protein digestion affects protein gain differently during
aging in humans. J. Physiol. 2003, 549, 635–644. [CrossRef] [PubMed]
17. Schadewaldt, P.; Wendel, U. Metabolism of branched-chain amino acids in maple syrup urine disease.
Eur. J. Pediatr. 1997, 156, S62–S66. [CrossRef] [PubMed]
18. Fouillet, H.; Mariotti, F.; Gaudichon, C.; Bos, C.; Tome, D. Peripheral and splanchnic metabolism of dietary
nitrogen are differently affected by the protein source in humans as assessed by compartmental modeling.
J. Nutr. 2002, 132, 125–133. [CrossRef] [PubMed]
Nutrients 2018, 10, 180 14 of 18
19. Devaraj, S.; Hemarajata, P.; Versalovic, J. The human gut microbiome and body metabolism: Implications for
obesity and diabetes. Clin. Chem. 2013, 59, 617–628. [CrossRef] [PubMed]
20. Tang, J.E.; Moore, D.R.; Kujbida, G.W.; Tarnopolsky, M.A.; Phillips, S.M. Ingestion of whey hydrolysate,
casein, or soy protein isolate: Effects on mixed muscle protein synthesis at rest and following resistance
exercise in young men. J. Appl. Physiol. 2009, 107, 987–992. [CrossRef] [PubMed]
21. Gorissen, S.H.; Horstman, A.M.; Franssen, R.; Crombag, J.J.; Langer, H.; Bierau, J.; Respondek, F.;
van Loon, L.J. Ingestion of wheat protein increases in vivo muscle protein synthesis rates in healthy older
men in a randomized trial. J. Nutr. 2016, 146, 1651–1659. [CrossRef] [PubMed]
22. Reidy, P.T.; Walker, D.K.; Dickinson, J.M.; Gundermann, D.M.; Drummond, M.J.; Timmerman, K.L.;
Cope, M.B.; Mukherjea, R.; Jennings, K.; Volpi, E.; et al. Soy-dairy protein blend and whey protein ingestion
after resistance exercise increases amino acid transport and transporter expression in human skeletal muscle.
J. Appl. Physiol. 2014, 116, 1353–1364. [CrossRef] [PubMed]
23. Drummond, M.J.; Fry, C.S.; Glynn, E.L.; Timmerman, K.L.; Dickinson, J.M.;Walker, D.K.; Gundermann, D.M.;
Volpi, E.; Rasmussen, B.B. Skeletal muscle amino acid transporter expression is increased in young and older
adults following resistance exercise. J. Appl. Physiol. 2011, 111, 135–142. [CrossRef] [PubMed]
24. Dreyer, H.C.; Drummond, M.J.; Pennings, B.; Fujita, S.; Glynn, E.L.; Chinkes, D.L.; Dhanani, S.; Volpi, E.;
Rasmussen, B.B. Leucine-enriched essential amino acid and carbohydrate ingestion following resistance
exercise enhances mtor signaling and protein synthesis in human muscle. Am. J. Physiol. Endocrinol. Metab.
2008, 294, E392–E400. [CrossRef] [PubMed]
25. Bohe, J.; Low, J.F.;Wolfe, R.R.; Rennie, M.J. Latency and duration of stimulation of human muscle protein
synthesis during continuous infusion of amino acids. J. Physiol. 2001, 532, 575–579. [CrossRef] [PubMed]
26. Bohe, J.; Low, A.;Wolfe, R.R.; Rennie, M.J. Human muscle protein synthesis is modulated by extracellular,
not intramuscular amino acid availability: A dose-response study. J. Physiol. 2003, 552, 315–324. [CrossRef]
[PubMed]
27. Atherton, P.J.; Etheridge, T.; Watt, P.W.; Wilkinson, D.; Selby, A.; Rankin, D.; Smith, K.; Rennie, M.J. Muscle
full effect after oral protein: Time-dependent concordance and discordance between human muscle protein
synthesis and mtorc1 signaling. Am. J. Clin. Nutr. 2010, 92, 1080–1088. [CrossRef] [PubMed]
28. Volpi, E.; Kobayashi, H.; Sheffield-Moore, M.; Mittendorfer, B.;Wolfe, R.R. Essential amino acids are primarily
responsible for the amino acid stimulation of muscle protein anabolism in healthy elderly adults. Am. J.
Clin. Nutr. 2003, 78, 250–258. [CrossRef] [PubMed]
29. Anthony, J.C.; Lang, C.H.; Crozier, S.J.; Anthony, T.G.; MacLean, D.A.; Kimball, S.R.; Jefferson, L.S.
Contribution of insulin to the translational control of protein synthesis in skeletal muscle by leucine. Am. J.
Physiol. Endocrinol. Metab. 2002, 282, E1092–E1101. [CrossRef] [PubMed]
30. Crozier, S.J.; Kimball, S.R.; Emmert, S.W.; Anthony, J.C.; Jefferson, L.S. Oral leucine administration stimulates
protein synthesis in rat skeletal muscle. J. Nutr. 2005, 135, 376–382. [CrossRef] [PubMed]
31. Norton, L.E.; Layman, D.K.; Bunpo, P.; Anthony, T.G.; Brana, D.V.; Garlick, P.J. The leucine content of a
complete meal directs peak activation but not duration of skeletal muscle protein synthesis and mammalian
target of rapamycin signaling in rats. J. Nutr. 2009, 139, 1103–1109. [CrossRef] [PubMed]
32. Churchward-Venne, T.A.; Breen, L.; Di Donato, D.M.; Hector, A.J.; Mitchell, C.J.; Moore, D.R.; Stellingwerff, T.;
Breuille, D.; Offord, E.A.; Baker, S.K.; et al. Leucine supplementation of a low-protein mixed macronutrient
beverage enhances myofibrillar protein synthesis in young men: A double-blind, randomized trial. Am. J.
Clin. Nutr. 2014, 99, 276–286. [CrossRef] [PubMed]
33. Moore, D.R.; Churchward-Venne, T.A.; Witard, O.; Breen, L.; Burd, N.A.; Tipton, K.D.; Phillips, S.M. Protein
ingestion to stimulate myofibrillar protein synthesis requires greater relative protein intakes in healthy older
versus younger men. J. Gerontol. A Biol. Sci. Med. Sci. 2015, 70, 57–62. [CrossRef] [PubMed]
34. Churchward-Venne, T.A.; Burd, N.A.; Phillips, S.M. Nutritional regulation of muscle protein synthesis with
resistance exercise: Strategies to enhance anabolism. Nutr. Metab. 2012, 9, 40. [CrossRef] [PubMed]
35. Witard, O.C.; Jackman, S.R.; Breen, L.; Smith, K.; Selby, A.; Tipton, K.D. Myofibrillar muscle protein synthesis
rates subsequent to a meal in response to increasing doses of whey protein at rest and after resistance exercise.
Am. J. Clin. Nutr. 2014, 99, 86–95. [CrossRef] [PubMed]
36. Moore, D.R.; Robinson, M.J.; Fry, J.L.; Tang, J.E.; Glover, E.I.;Wilkinson, S.B.; Prior, T.; Tarnopolsky, M.A.;
Phillips, S.M. Ingested protein dose response of muscle and albumin protein synthesis after resistance
exercise in young men. Am. J. Clin. Nutr. 2009, 89, 161–168. [CrossRef] [PubMed]
Nutrients 2018, 10, 180 15 of 18
37. Areta, J.L.; Burke, L.M.; Ross, M.L.; Camera, D.M.; West, D.W.; Broad, E.M.; Jeacocke, N.A.; Moore, D.R.;
Stellingwerff, T.; Phillips, S.M.; et al. Timing and distribution of protein ingestion during prolonged recovery
from resistance exercise alters myofibrillar protein synthesis. J. Physiol. 2013, 591, 2319–2331. [CrossRef]
[PubMed]
38. Macnaughton, L.S.;Wardle, S.L.;Witard, O.C.; McGlory, C.; Hamilton, D.L.; Jeromson, S.; Lawrence, C.E.;
Wallis, G.A.; Tipton, K.D. The response of muscle protein synthesis following whole-body resistance exercise
is greater following 40 g than 20 g of ingested whey protein. Physiol. Rep. 2016, 4, e128932. [CrossRef]
[PubMed]
39. Groen, B.B.; Res, P.T.; Pennings, B.; Hertle, E.; Senden, J.M.; Saris, W.H.; van Loon, L.J.
Intragastric protein administration stimulates overnight muscle protein synthesis in elderly men.
Am. J. Physiol. Endocrinol. Metab. 2012, 302, E52–E60. [CrossRef] [PubMed]
40. Beelen, M.; Tieland, M.; Gijsen, A.P.; Vandereyt, H.; Kies, A.K.; Kuipers, H.; Saris,W.H.; Koopman, R.; van
Loon, L.J. Coingestion of carbohydrate and protein hydrolysate stimulates muscle protein synthesis during
exercise in young men, with no further increase during subsequent overnight recovery. J. Nutr. 2008, 138,
2198–2204. [CrossRef] [PubMed]
41. Res, P.T.; Groen, B.; Pennings, B.; Beelen, M.; Wallis, G.A.; Gijsen, A.P.; Senden, J.M.G.; van Loon, L.J. Protein
ingestion before sleep improves postexercise overnight recovery. Med. Sci. Sports Exerc. 2012, 44, 1560–1569.
[CrossRef] [PubMed]
42. Holwerda, A.M.; Kouw, I.W.; Trommelen, J.; Halson, S.L.;Wodzig,W.K.; Verdijk, L.B.; van Loon, L.J. Physical
activity performed in the evening increases the overnight muscle protein synthetic response to presleep
protein ingestion in older men. J. Nutr. 2016, 146, 1307–1314. [CrossRef] [PubMed]
43. Trommelen, J.; Holwerda, A.M.; Kouw, I.W.; Langer, H.; Halson, S.L.; Rollo, I.; Verdijk, L.B.; van Loon, L.J.
Resistance exercise augments postprandial overnight muscle protein synthesis rates. Med. Sci. Sports Exerc.
2016, 48, 2517–2525. [CrossRef] [PubMed]
44. Snijders, T.; Res, P.T.; Smeets, J.S.; van Vliet, S.; van Kranenburg, J.; Maase, K.; Kies, A.K.; Verdijk, L.B.;
van Loon, L.J. Protein ingestion before sleep increases muscle mass and strength gains during prolonged
resistance-type exercise training in healthy young men. J. Nutr. 2015, 145, 1178–1184. [CrossRef] [PubMed]
45. Morton, R.W.; Murphy, K.T.; McKellar, S.R.; Schoenfeld, B.J.; Henselmans, M.; Helms, E.; Aragon, A.A.;
Devries, M.C.; Banfield, L.; Krieger, J.W.; et al. A systematic review, meta-analysis and meta-regression of
the effect of protein supplementation on resistance training-induced gains in muscle mass and strength in
healthy adults. Br. J. Sports Med. 2017. [CrossRef] [PubMed]
46. Cermak, N.M.; Res, P.T.; de Groot, L.C.; Saris,W.H.; van Loon, L.J. Protein supplementation augments the
adaptive response of skeletal muscle to resistance-type exercise training: A meta-analysis. Am. J. Clin. Nutr.
2012, 96, 1454–1464. [CrossRef] [PubMed]
47. Gibala, M.J.; MacDougall, J.D.; Tarnopolsky, M.A.; Stauber,W.T.; Elorriaga, A. Changes in human skeletal
muscle ultrastructure and force production after acute resistance exercise. J. Appl. Physiol. 1995, 78, 702–708.
[CrossRef] [PubMed]
48. Damas, F.; Phillips, S.M.; Libardi, C.A.; Vechin, F.C.; Lixandrao, M.E.; Jannig, P.R.; Costa, L.A.; Bacurau, A.V.;
Snijders, T.; Parise, G.; et al. Resistance training-induced changes in integrated myofibrillar protein synthesis
are related to hypertrophy only after attenuation of muscle damage. J. Physiol. 2016, 594, 5209–5222.
[CrossRef] [PubMed]
49. Hudson, M.B.; Hosick, P.A.; McCaulley, G.O.; Schrieber, L.; Wrieden, J.; McAnulty, S.R.; Triplett, N.T.;
McBride, J.M.; Quindry, J.C. The effect of resistance exercise on humoral markers of oxidative stress. Med. Sci.
Sports Exerc. 2008, 40, 542–548. [CrossRef] [PubMed]
50. Wolfe, R.R. Tracers in metabolic research: Radioisotope and stable isotope/mass spectrometry methods.
Lab. Res. Methods Biol. Med. 1984, 9, 1–287. [CrossRef] [PubMed]
51. Hartman, J.W.; Moore, D.R.; Phillips, S.M. Resistance training reduces whole-body protein turnover and
improves net protein retention in untrained young males. Appl. Physiol. Nutr. Metab. 2006, 31, 557–564.
[CrossRef] [PubMed]
52. Moore, D.R.; Del Bel, N.C.; Nizi, K.I.; Hartman, J.W.; Tang, J.E.; Armstrong, D.; Phillips, S.M. Resistance
training reduces fasted- and fed-state leucine turnover and increases dietary nitrogen retention in previously
untrained young men. J. Nutr. 2007, 137, 985–991. [CrossRef] [PubMed]
Nutrients 2018, 10, 180 16 of 18
53. Tang, J.E.; Perco, J.G.; Moore, D.R.;Wilkinson, S.B.; Phillips, S.M. Resistance training alters the response of
fed state mixed muscle protein synthesis in young men. Am. J. Physiol. Regul. Integr. Comp. Physiol. 2008,
294, R172–R178. [CrossRef] [PubMed]
54. Azizbeigi, K.; Azarbayjani, M.A.; Peeri, M.; Agha-alinejad, H.; Stannard, S. The effect of progressive resistance
training on oxidative stress and antioxidant enzyme activity in erythrocytes in untrained men. Int. J. Sport
Nutr. Exerc. Metab. 2013, 23, 230–238. [CrossRef] [PubMed]
55. Deutz, N.E.; Wolfe, R.R. Is there a maximal anabolic response to protein intake with a meal? Clin. Nutr. 2013,
32, 309–313. [CrossRef] [PubMed]
56. Kim, I.Y.; Deutz, N.E.P.; Wolfe, R.R. Update on maximal anabolic response to dietary protein. Clin. Nutr.
2017. [CrossRef] [PubMed]
57. Kimball, S.R.; Jurasinski, C.V.; Lawrence, J.C., Jr.; Jefferson, L.S. Insulin stimulates protein synthesis in
skeletal muscle by enhancing the association of eIF-4E and eIF-4G. Am. J. Physiol. 1997, 272, C754–C759.
[CrossRef] [PubMed]
58. Greenhaff, P.L.; Karagounis, L.G.; Peirce, N.; Simpson, E.J.; Hazell, M.; Layfield, R.;Wackerhage, H.; Smith, K.;
Atherton, P.; Selby, A.; et al. Disassociation between the effects of amino acids and insulin on signaling,
ubiquitin ligases, and protein turnover in human muscle. Am. J. Physiol. Endocrinol. Metab. 2008, 295,
E595–E604. [CrossRef] [PubMed]
59. Abdulla, H.; Smith, K.; Atherton, P.J.; Idris, I. Role of insulin in the regulation of human skeletal muscle
protein synthesis and breakdown: A systematic review and meta-analysis. Diabetologia 2016, 59, 44–55.
[CrossRef] [PubMed]
60. Wilkes, E.A.; Selby, A.L.; Atherton, P.J.; Patel, R.; Rankin, D.; Smith, K.; Rennie, M.J. Blunting of insulin
inhibition of proteolysis in legs of older subjects may contribute to age-related sarcopenia. Am. J. Clin. Nutr.
2009, 90, 1343–1350. [CrossRef] [PubMed]
61. Koopman, R.; Beelen, M.; Stellingwerff, T.; Pennings, B.; Saris,W.H.; Kies, A.K.; Kuipers, H.; van Loon, L.J.
Coingestion of carbohydrate with protein does not further augment postexercise muscle protein synthesis.
Am. J. Physiol. Endocrinol. Metab. 2007, 293, E833–E842. [CrossRef] [PubMed]
62. Staples, A.W.; Burd, N.A.;West, D.W.; Currie, K.D.; Atherton, P.J.; Moore, D.R.; Rennie, M.J.; Macdonald, M.J.;
Baker, S.K.; Phillips, S.M. Carbohydrate does not augment exercise-induced protein accretion versus protein
alone. Med. Sci. Sports Exerc. 2011, 43, 1154–1161. [CrossRef] [PubMed]
63. Glynn, E.L.; Fry, C.S.; Timmerman, K.L.; Drummond, M.J.; Volpi, E.; Rasmussen, B.B. Addition of
carbohydrate or alanine to an essential amino acid mixture does not enhance human skeletal muscle
protein anabolism. J. Nutr. 2013, 143, 307–314. [CrossRef] [PubMed]
64. Gorissen, S.H.; Burd, N.A.; Hamer, H.M.; Gijsen, A.P.; Groen, B.B.; van Loon, L.J. Carbohydrate coingestion
delays dietary protein digestion and absorption but does not modulate postprandial muscle protein accretion.
J. Clin. Endocrinol. Metab. 2014, 99, 2250–2258. [CrossRef] [PubMed]
65. Ivy, J.L.; Goforth, H.W., Jr.; Damon, B.M.; McCauley, T.R.; Parsons, E.C.; Price, T.B. Early postexercise muscle
glycogen recovery is enhanced with a carbohydrate-protein supplement. J. Appl. Physiol. 2002, 93, 1337–1344.
[CrossRef] [PubMed]
66. Berardi, J.M.; Price, T.B.; Noreen, E.E.; Lemon, P.W. Postexercise muscle glycogen recovery enhanced with a
carbohydrate-protein supplement. Med. Sci. Sports Exerc. 2006, 38, 1106–1113. [CrossRef] [PubMed]
67. Burke, L.M.; van Loon, L.J.C.; Hawley, J.A. Postexercise muscle glycogen resynthesis in humans.
J. Appl. Physiol. 2017, 122, 1055–1067. [CrossRef] [PubMed]
68. Kim, I.Y.; Schutzler, S.; Schrader, A.; Spencer, H.J.; Azhar, G.; Ferrando, A.A.; Wolfe, R.R. The anabolic
response to a meal containing different amounts of protein is not limited by the maximal stimulation of
protein synthesis in healthy young adults. Am. J. Physiol. Endocrinol. Metab. 2016, 310, E73–E80. [CrossRef]
[PubMed]
69. Symons, T.B.; Sheffield-Moore, M.; Wolfe, R.R.; Paddon-Jones, D. A moderate serving of high-quality protein
maximally stimulates skeletal muscle protein synthesis in young and elderly subjects. J. Am. Diet. Assoc.
2009, 109, 1582–1586. [CrossRef] [PubMed]
70. Long, C.L.; Birkhahn, R.H.; Geiger, J.W.; Blakemore, W.S. Contribution of skeletal muscle protein in elevated
rates of whole body protein catabolism in trauma patients. Am. J. Clin. Nutr. 1981, 34, 1087–1093. [CrossRef]
[PubMed]
71. Kim, I.Y.; Schutzler, S.; Schrader, A.; Spencer, H.; Kortebein, P.; Deutz, N.E.; Wolfe, R.R.; Ferrando, A.A.
Quantity of dietary protein intake, but not pattern of intake, affects net protein balance primarily through
differences in protein synthesis in older adults. Am. J. Physiol. Endocrinol. Metab. 2015, 308, E21–E28.
[CrossRef] [PubMed]
72. Masiero, E.; Agatea, L.; Mammucari, C.; Blaauw, B.; Loro, E.; Komatsu, M.; Metzger, D.; Reggiani, C.;
Schiaffino, S.; Sandri, M. Autophagy is required to maintain muscle mass. Cell Metab. 2009, 10, 507–515.
[CrossRef] [PubMed]
73. Castets, P.; Lin, S.; Rion, N.; Di Fulvio, S.; Romanino, K.; Guridi, M.; Frank, S.; Tintignac, L.A.; Sinnreich, M.;
Ruegg, M.A. Sustained activation of mTORC1 in skeletal muscle inhibits constitutive and starvation-induced
autophagy and causes a severe, late-onset myopathy. Cell Metab. 2013, 17, 731–744. [CrossRef] [PubMed]
74. Kitajima, Y.; Tashiro, Y.; Suzuki, N.;Warita, H.; Kato, M.; Tateyama, M.; Ando, R.; Izumi, R.; Yamazaki, M.;
Abe, M.; et al. Proteasome dysfunction induces muscle growth defects and protein aggregation. J. Cell Sci.
2014, 127, 5204–5217. [CrossRef] [PubMed]
75. Drummond, M.J.; Addison, O.; Brunker, L.; Hopkins, P.N.; McClain, D.A.; LaStayo, P.C.; Marcus, R.L.
Downregulation of E3 ubiquitin ligases and mitophagy-related genes in skeletal muscle of physically
inactive, frail older women: A cross-sectional comparison. J. Gerontol. A Biol. Sci. Med. Sci. 2014, 69,
1040–1048. [CrossRef] [PubMed]
76. Leger, B.; Cartoni, R.; Praz, M.; Lamon, S.; Deriaz, O.; Crettenand, A.; Gobelet, C.; Rohmer, P.;
Konzelmann, M.; Luthi, F.; et al. Akt signalling through GSK-3beta, mtor and foxo1 is involved in human
skeletal muscle hypertrophy and atrophy. J. Physiol. 2006, 576, 923–933. [CrossRef] [PubMed]
77. Dhurandhar, E.J.; Kaiser, K.A.; Dawson, J.A.; Alcorn, A.S.; Keating, K.D.; Allison, D.B. Predicting adult
weight change in the real world: A systematic review and meta-analysis accounting for compensatory
changes in energy intake or expenditure. Int. J. Obes. 2015, 39, 1181–1187. [CrossRef] [PubMed]
78. Magkos, F.; Fraterrigo, G.; Yoshino, J.; Luecking, C.; Kirbach, K.; Kelly, S.C.; de Las Fuentes, L.; He, S.;
Okunade, A.L.; Patterson, B.W.; et al. Effects of moderate and subsequent progressive weight loss on
metabolic function and adipose tissue biology in humans with obesity. Cell Metab. 2016, 23, 591–601.
[CrossRef] [PubMed]
79. Wolfe, R.R. The underappreciated role of muscle in health and disease. Am. J. Clin. Nutr. 2006, 84, 475–482.
[PubMed]
80. Pasiakos, S.M.; Vislocky, L.M.; Carbone, J.W.; Altieri, N.; Konopelski, K.; Freake, H.C.; Anderson, J.M.;
Ferrando, A.A.; Wolfe, R.R.; Rodriguez, N.R. Acute energy deprivation affects skeletal muscle protein
synthesis and associated intracellular signaling proteins in physically active adults. J. Nutr. 2010, 140,
745–751. [CrossRef] [PubMed]
81. Areta, J.L.; Burke, L.M.; Camera, D.M.;West, D.W.; Crawshay, S.; Moore, D.R.; Stellingwerff, T.; Phillips, S.M.;
Hawley, J.A.; Coffey, V.G. Reduced resting skeletal muscle protein synthesis is rescued by resistance exercise
and protein ingestion following short-term energy deficit. Am. J. Physiol. Endocrinol. Metab. 2014, 306,
E989–E997. [CrossRef] [PubMed]
82. Villareal, D.T.; Smith, G.I.; Shah, K.; Mittendorfer, B. Effect of weight loss on the rate of muscle protein
synthesis during fasted and fed conditions in obese older adults. Obesity (Silver Spring) 2012, 20, 1780–1786.
[CrossRef] [PubMed]
83. Carbone, J.W.; Margolis, L.M.; McClung, J.P.; Cao, J.J.; Murphy, N.E.; Sauter, E.R.; Combs, G.F., Jr.; Young, A.J.;
Pasiakos, S.M. Effects of energy deficit, dietary protein, and feeding on intracellular regulators of skeletal
muscle proteolysis. FASEB J. 2013, 27, 5104–5111. [CrossRef] [PubMed]
84. Carbone, J.W.; Pasiakos, S.M.; Vislocky, L.M.; Anderson, J.M.; Rodriguez, N.R. Effects of short-term
energy deficit on muscle protein breakdown and intramuscular proteolysis in normal-weight young adults.
Appl. Physiol. Nutr. Metab. 2014, 39, 960–968. [CrossRef] [PubMed]
85. Hector, A.J.; McGlory, C.; Damas, F.; Mazara, N.; Baker, S.K.; Phillips, S.M. Pronounced energy restriction
with elevated protein intake results in no change in proteolysis and reductions in skeletal muscle protein
synthesis that are mitigated by resistance exercise. FASEB J. 2017. [CrossRef] [PubMed]
86. Peth, A.; Nathan, J.A.; Goldberg, A.L. The atp costs and time required to degrade ubiquitinated proteins by
the 26 s proteasome. J. Biol. Chem. 2013, 288, 29215–29222. [CrossRef] [PubMed]
Nutrients 2018, 10, 180 18 of 18
87. Pasiakos, S.M.; Cao, J.J.; Margolis, L.M.; Sauter, E.R.; Whigham, L.D.; McClung, J.P.; Rood, J.C.; Carbone, J.W.;
Combs, G.F., Jr.; Young, A.J. Effects of high-protein diets on fat-free mass and muscle protein synthesis
following weight loss: A randomized controlled trial. FASEB J. 2013, 27, 3837–3847. [CrossRef] [PubMed]
88. Longland, T.M.; Oikawa, S.Y.; Mitchell, C.J.; Devries, M.C.; Phillips, S.M. Higher compared with lower
dietary protein during an energy deficit combined with intense exercise promotes greater lean mass gain
and fat mass loss: A randomized trial. Am. J. Clin. Nutr. 2016, 103, 738–746. [CrossRef] [PubMed]
89. Helms, E.R.; Zinn, C.; Rowlands, D.S.; Brown, S.R. A systematic review of dietary protein during caloric
restriction in resistance trained lean athletes: A case for higher intakes. Int. J. Sport Nutr. Exerc. Metab. 2014,
24, 127–138. [CrossRef] [PubMed]
90. Hector, A.; Phillips, S.M. Protein recommendations for weight loss in elite athletes: A focus on body
composition and performance. Int. J. Sport Nutr. Exerc. Metab. 2017. [CrossRef] [PubMed]
91. Helms, E.R.; Aragon, A.A.; Fitschen, P.J. Evidence-based recommendations for natural bodybuilding contest
preparation: Nutrition and supplementation. J. Int. Soc. Sports Nutr. 2014, 11, 20. [CrossRef] [PubMed]
92. Vandewater, K.; Vickers, Z. Higher-protein foods produce greater sensory-specific satiety. Physiol. Behav.
1996, 59, 579–583. [CrossRef]
93. Astrup, A. The satiating power of protein—A key to obesity prevention? Am. J. Clin. Nutr. 2005, 82, 1–2.
[PubMed]
94. Veldhorst, M.A.; Nieuwenhuizen, A.G.; Hochstenbach-Waelen, A.; van Vught, A.J.; Westerterp, K.R.;
Engelen, M.P.; Brummer, R.J.; Deutz, N.E.; Westerterp-Plantenga, M.S. Dose-dependent satiating effect
of whey relative to casein or soy. Physiol. Behav. 2009, 96, 675–682. [CrossRef] [PubMed]
95. Gunnarsson, P.T.; Winzell, M.S.; Deacon, C.F.; Larsen, M.O.; Jelic, K.; Carr, R.D.; Ahren, B. Glucose-induced
incretin hormone release and inactivation are differently modulated by oral fat and protein in mice.
Endocrinology 2006, 147, 3173–3180. [CrossRef] [PubMed]
96. Hall, W.L.; Millward, D.J.; Long, S.J.; Morgan, L.M. Casein and whey exert different effects on plasma amino
acid profiles, gastrointestinal hormone secretion and appetite. Br. J. Nutr. 2003, 89, 239–248. [CrossRef]
[PubMed]
97. Burton-Freeman, B.M. Glycomacropeptide (GMP) is not critical to whey-induced satiety, but may have a
unique role in energy intake regulation through cholecystokinin (CCK). Physiol. Behav. 2008, 93, 379–387.
[CrossRef] [PubMed]
98. Veldhorst, M.A.; Nieuwenhuizen, A.G.; Hochstenbach-Waelen, A.; Westerterp, K.R.; Engelen, M.P.;
Brummer, R.J.; Deutz, N.E.; Westerterp-Plantenga, M.S. Effects of complete whey-protein breakfasts versus
whey without GMP-breakfasts on energy intake and satiety. Appetite 2009, 52, 388–395. [CrossRef] [PubMed]
99. Acheson, K.J.; Blondel-Lubrano, A.; Oguey-Araymon, S.; Beaumont, M.; Emady-Azar, S.;
Ammon-Zufferey, C.; Monnard, I.; Pinaud, S.; Nielsen-Moennoz, C.; Bovetto, L. Protein choices
targeting thermogenesis and metabolism. Am. J. Clin. Nutr. 2011, 93, 525–534. [CrossRef] [PubMed]
100. Alfenas Rde, C.; Bressan, J.; Paiva, A.C. Effects of protein quality on appetite and energy metabolism in
normal weight subjects. Arq. Bras. Endocrinol. Metabol. 2010, 54, 45–51. [CrossRef] [PubMed]