Efectele Administrării Leucinei în Sarcopenie

1. Introducere
Sarcopenia se referă la pierderea masei musculare scheletice și a forței asociate îmbătrânirii și poate fi întâlnită în mai multe afecțiuni. Sarcopenia care apare odata cu inaintarea in varsta are o evolutie graduala si este larg asociata cu un risc crescut de rezultate adverse, cum ar fi dizabilitate fizica, calitate precara a vietii si mortalitate. Prevalența sa a fost estimată la 5%–13% la persoanele cu vârsta cuprinsă între 60–70 și până la 50% la cei peste 80 de ani. Mai multe rapoarte efectuate la populațiile mai în vârstă au arătat că indivizii prezintă un risc crescut de cădere, fragilitate, pierderea capacității de a desfășura activități de bază și diabet de tip II, toate acestea afectând calitatea vieții și determinând rate ridicate de morbiditate și mortalitate prematură.
Un studiu recent efectuat în SUA, bazat pe sondajul National Health and Nutrition Examination Survey (NHANES), a demonstrat că masa musculară este un predictor semnificativ al longevității pentru mortalitatea de orice cauză, luând în considerare bărbații și femeile cu vârsta de peste 55 sau 65 de ani. Una dintre principalele căi prin care pierderea masei musculare contribuie la apariția sau progresia altor boli este alterarea turnover-ului proteinelor și a metabolismului în țesutul muscular scheletic. În plus, alți factori, cum ar fi răspunsul anabolic redus la hrănirea cu proteine în timpul îmbătrânirii, contribuie la pierderea masei musculare la persoanele cu sarcopenie. Confirmând acest lucru, studiile metabolice au arătat că persoanele în vârstă, de 65 de ani și peste necesită aproximativ 2% mai mult aport de proteine pe masă pentru a maximiza sinteza proteinelor musculare. În plus, la nivel global, doar 40% dintre adulții în vârstă îndeplinesc aportul zilnic recomandat de proteine și 10% dintre femeile în vârstă nici măcar nu îndeplinesc necesarul mediu minim estimat.
Una dintre strategiile nutriționale care s-a dovedit a fi potențial utilă în creșterea sintezei proteinelor la nivel muscular este suplimentarea cu leucină, un aminoacid esențial cu lanț ramificat care are acțiuni reglatoare importante în mușchi care sunt mediati, cel puțin parțial, de ținta căii rapamicinei. Leucina modulează rata de turnover a proteinelor în mușchii scheletici prin scăderea proteolizei și creșterea sintezei proteinelor. Mai multe studii au arătat că administrarea de leucină poate îmbunătăți sinteza proteinelor în mușchi. Un studiu clinic recent a demonstrat că administrarea concomitentă a 1,5 g de leucină liberă pe cale orală cu un singur bolus de 15 g de proteine a crescut și mai mult rata proteinelor musculare în timpul recuperării după exercițiul fizic bazat pe rezistență la bărbații în vârstă, sugerând leucina- efectele sunt sinergice cu cele realizate prin exercițiul fizic cel puțin în unele condiții experimentale. În plus, leucina poate stimula, de asemenea, eliberarea de insulină de către celulele beta pancreatice și prin urmare, efectul său benefic poate îmbunătăți, de asemenea, absorbția de glucoză în mușchii scheletici, crescând semnalul anabolic în mușchii scheletici și contribuind pozitiv la menținerea masei musculare.
Având în vedere cele de mai sus, administrarea de suplimente care conțin leucină a fost propusă ca abordare promițătoare pentru tratarea sarcopeniei cel puțin la persoanele în vârstă. Cele mai multe studii randomizate controlate cu placebo (RCT) au inclus intervenții care utilizează proteine din zer ca supliment, deoarece acestea conțin cantități mari de leucină (aproximativ 13 g leucină/100 g proteină). Cu toate acestea, dovezile științifice cu privire la efectul leucinei în monoterapie în sarcopenie sunt foarte rare. Am efectuat un RCT pentru a stabili dacă administrarea de leucină în monoterapie este eficientă în tratamentul sarcopeniei și al funcției mușchilor respiratori la persoanele în vârstă instituționalizate, un subgrup de persoane în vârstă cu o cantitate uriașă de comorbiditate, care sunt rareori evaluate în RCT, care utilizează suplimente cu leucină.
Principalele obiective ale RCT au fost:
(1) să analizeze efectele administrării de leucină orală asupra criteriilor de sarcopenie, de exemplu, masa musculară, forța și activitatea funcțională la persoanele în vârstă;
(2) să evalueze efectele sale asupra funcției mușchilor respiratori folosind, ca indicatori, presiunile respiratorii statice maxime la nivelul cavității bucale, inspiratorii (MIP) și expiratorii (MEP) și debitul expirator de vârf (PEF);
(3) să investigheze efectele suplimentării cu leucină asupra altor rezultate secundare incluse în evaluarea psihogeriatrică integrativă, cum ar fi funcția cognitivă, capacitatea de a efectua activitățile de bază ale vieții și evaluarea nutrițională.
2. Materiale și metode
2.1. Studiul Populației
Participanții la RCT au fost bărbați și femei care locuiau în case de bătrâni (regiunea Valencia, Spania). Toți indivizii au îndeplinit criteriul de includere pentru a putea merge 6 m și aveau 65 de ani sau peste. Criteriile de excludere au fost afectarea cognitivă severă care împiedică înțelegerea întrebărilor incluse în chestionare, boli psihiatrice slab controlate, cum ar fi schizofrenia sau orbirea, infecțiile acute sau cancerul cunoscut. Mărimea eșantionului a fost estimată în funcție de diferențele dintre măsurătorile dintre grupurile care ar trebui detectate (=1 criteriu sarcopenie dintre cei șase parametri ai sarcopeniei, forța musculară, masa musculară, timpul de mers, maxim static inspirator (MIP) sau expirator ( MEP) presiunile la gură și debitul expirator de vârf (PEF), abaterea standard a acestor valori, valoarea p (0,05) și puterea (90%). La astfel de indivizi instituționalizați în vârstă precum cei înscriși în RCT (vârsta medie 79 de ani), experiența noastră a arătat că există un interval de variabilitate de 10%-30% a abandonului în studiile experimentale efectuate în casele de bătrâni. Din acest motiv, ne-am asumat o putere de 90% pentru a minimiza impactul unei eventuale rate ridicate de abandon în timpul studiului.
Ca rezultat, pentru a obține o putere de 90% cu un nivel de semnificație de 5% pe două părți și pentru a detecta o diferență minimă de un parametru de sarcopenie (am măsurat șase parametri de sarcopenie) între grupurile placebo și leucină, am calculat că o dimensiune a eșantionului dintr-un total de 44 de pacienți ar intra în acest studiu încrucișat cu două tratamente. Prin urmare, am planificat să recrutăm 50 de voluntari pentru a permite abandonul persoanelor care nu au putut finaliza investigația. Studiul a fost aprobat de Comitetul de etică al Universității din Valencia (Valencia, Spania) (H1524420647893 data de 5 iulie 2018). Consimțământul informat scris a fost obținut de la toți participanții. Studiul clinic a fost înregistrat pe ClinicalTrials.gov cu numărul de identificare NCT03831399.
2.2. Intervenţie
Compușii testați, L-leucina și placebo (lactoza), sub formă de pulbere, au fost întotdeauna păstrați în sticle și păstrați la temperatura camerei. Asistentele sau participanții înșiși sub supravegherea asistentei au dizolvat două linguri de L-leucină (6 g/zi) sau placebo (lactoză, 6 g/zi) într-un pahar cu apă sau suc și au fost administrate dimineața, la scurt timp după micul dejun ( 9–10 a.m.) (aproximativ 3 g) și după-amiaza la 4–5 p.m. (aproximativ 3 g). Participanții au fost instruiți să raporteze orice efecte secundare ale modificării gastrointestinale și să-și mențină obiceiurile alimentare obișnuite. Participanții au fost intervievați săptămânal cu privire la eventualele efecte adverse, inclusiv cele mai frecvente efecte secundare gastro-intestinale, cum ar fi dispepsia, flatulența și modificările caracteristicilor scaunului (consistență și frecvență). Conformitatea cu administrarea de leucină sau placebo a fost evaluată pe baza unui jurnal completat zilnic de asistentele care lucrează în casele de bătrâni. Asistentele au înregistrat dacă oamenii nu doreau să bea suplimentul sau dacă au existat probleme în momentul administrării, de exemplu, dacă persoanele au adormit în momentul administrării sau se aflau în afara azilului de bătrâni din orice motiv în momentul administrării. Conformitatea adecvată a fost definită ca fiind consumarea a 10 din cele 14 administrări posibile pe săptămână. Conformitatea procentuală a fost calculată prin determinarea numărului de unități de dozare consumate, împărțit la numărul estimat a fi luat și înmulțit cu 100. Dietele din casele de bătrâni sunt concepute și supravegheate constant de o echipă de nutriționiști/dieteticieni.
2.3. Măsurarea sarcopeniei
Sarcopenia a fost măsurată conform liniilor directoare ale Grupului de lucru european privind sarcopenia la persoanele în vârstă (EWGSOP) și poate fi evaluată prin intermediul unor măsuri indirecte ale funcției musculare și ale masei musculare, cum ar fi viteza scăzută de mers (≤0,8 m/s mers 4,6). m), rezistența(gripul) mânerului evaluată prin dinamometrie (bărbați ≤ 30 kg/m2 și femei ≤ 20 kg/m2) și pierderea de masă slabă calculată folosind ecuația formulată de Janssen pe baza valorilor de rezistență obținute în evaluarea bioimpedanței întregului corp (femei). ≤ 5,5 kg/m2 și bărbați ≤ 7,25 kg/m2). Aceste valori ale masei slabe pot fi ajustate la diferite populații, cu valori limită pentru populația spaniolă de 8,31 kg/m2 pentru bărbați și 6,68 kg/m2 pentru femei. Am evaluat compoziția corporală prin analiza de impedanță bioelectrică (BIA) cu un dispozitiv Tanita BF-300. Măsurarea BIA a fost efectuată cu o tehnică standard folosind o singură frecvență de 50 KHz și plasarea a patru electrozi în poziție distală (patru electrozi la picioare). Participantul a fost măsurat în poziție în picioare(ortostatism). Valorile reactanței și rezistenței au fost apoi înregistrate odată ce pacientul a fost stabilizat. Masa musculară a fost calculată folosind formula lui Janssen și colab.: masa musculara (kg) = [(inaltime2 / R × 0,401) + (3,825 × sex) + (−0,701 × varsta) + 5102, unde inaltimea este exprimata in cm, R in ohmi, varsta in ani si la femeie sexul are valoarea zero, iar bărbații valoarea unu. Indicele de masă musculară (MMI) este definit ca masa musculară pe care o are o persoană, corectată în funcție de suprafața corpului (masă musculară/înălțime2). Forța musculară a fost măsurată în mâna dominantă cu un dinamometru cu mâner (Saehan Smedley Hand Dynamometer®), testul a fost întotdeauna repetat de trei ori pe o perioadă de 5 minute, fiind înregistrată valoarea medie a încercărilor.
Pentru evaluarea funcției respiratorii musculare s-a ales o evaluare spirometrică pentru a colecta principalele volume și fluxuri pulmonare, precum și o evaluare a presiunilor respiratorii maxime măsurate în gură produsă de contracția mușchilor respiratori pentru a aduna forța musculară respiratorie.
Pentru efectuarea spirometriei, pacientul a fost așezat, cu spatele sprijinit pe un spătar și cu pense nazale pentru a evita scurgerile de aer. Manevra a fost explicată în detaliu, iar pacientul a fost instruit să înceapă cu inspirație maximă până la atingerea capacității pulmonare totale, urmată de expirație forțată maximă până când nu mai poate fi evacuat aer. Au fost efectuate trei repetări ale manevrei, cu o pauză de 1 minut între ele, și s-a înregistrat cea mai mare valoare a celor trei repetări. Evaluarea spirometrică a urmat recomandările standardizate ale Societății Europene de Respirație.
Datele obținute au fost volume și capacități pulmonare forțate: capacitate vitală forțată (FVC), volum expirator forțat în prima secundă (FEV1), VEMS/FVC, volum expirator forțat în piste cu diametru mai mic de 1 mm (FEV2575, VEMS25, VEMS, VEMS75). ) și debitul expirator de vârf (PEF). Valorile absolute și valorile relative au fost obținute cu privire la un eșantion de subiecți sănătoși similari.
Presiunile respiratorii statice maxime la nivelul gurii, inspiratorii (MIP) și expiratorii (MEP), au fost evaluate pentru măsurarea forței mușchilor respiratori. Măsurătorile presiunilor maxime inspiratorii statice (MIP) sau expiratorii (MEP) la gură permit o evaluare simplă a forței globale a mușchilor respiratori într-un cadru clinic. Testele sunt volitive și necesită cooperarea deplină a subiectului pentru a obține un efort izometric maxim. MIP a fost măsurat la volumul rezidual și MEP la capacitatea pulmonară totală pentru a înregistra valoarea maximă a trei manevre care variază cu mai puțin de 10%. Au fost respectate reglementările standardizate pentru acest test. Pentru a obține cele mai bune performanțe posibile, pacienții au fost instruiți cu atenție de către un cercetător și apoi au început testul. Au fost efectuate cel puțin trei studii (cu o variație mai mică de 10% între încercări sau au fost eliminate) și s-a înregistrat cel mai mare rezultat.
2.4. Evaluare Geriatrică
Am efectuat o evaluare psiho-geriatrică completă la momentul inițial și după finalizarea RCT. Indicele Barthel a fost măsurat ca un surogat al capacității de a efectua activitățile de bază ale vieții de zi cu zi, iar intervalul de scor este un indice de puncte 0-100, unde zero este dependența totală și 100 este independența totală. Testul Mini Mental State Examination (MMSE) a fost folosit pentru a estima funcția cognitivă cu un interval de scor de 0-30, adică cele mai mari scoruri indicând performanțe cognitive mai bune. Starea nutrițională a fost evaluată de Mini-Evaluarea Nutrițională (MNA), un instrument utilizat în mod obișnuit în populația geriatrică, care are un interval de scor de 0-30, cu un scor < 24 indicând riscul de malnutriție. Starea generală de sănătate a fost estimată utilizând indicele de comorbiditate Charlson ajustat în funcție de vârstă. Am determinat amploarea activității fizice prin chestionarul internațional de activitate fizică (IPAQ) autoadministrat ale cărui întrebări se referă la timpul petrecut fiind activ fizic în ultimele 7 zile.
2.5. Parametrii analitici ai sângelui
Au fost prelevate probe de sânge în condiții de post între orele 7:30 a.m și 9 a.m. Probele de sânge au fost colectate prin două tuburi vacutainer (unul pentru plasmă și celălalt pentru ser) care conțineau EDTA. După extracție, probele au fost centrifugate la 1500 rpm timp de 10 minute la temperatura camerei. Supernatanții au fost ulterior alicoți și depozitați la -20 ° C până la analiză. Pentru toate celelalte determinări analitice au fost utilizate extracții de sânge controlate de centru rezidențial. Au fost măsurați hemograma și câțiva parametri biochimici (glucoză, uree, urat, colesterol, trigliceride, proteine totale, creatinina, calciu, sodiu, potasiu, transaminaze, vitamina D (sub formă de 25OHD), proteină C reactivă) în laboratoare clinice aparținând centrelor publice de sănătate. Concentrația citokinelor TNF-α și IL-6 în plasmă a fost realizată utilizând un kit comercial de analiză imunosorbantă legat de enzime, conform instrucțiunilor producătorului (TNF-α (ab100654), IL-6 (ab100572), Human ELISA Kit, Abcam ®). Toate măsurătorile de citokine au fost efectuate în duplicat și în aceeași zi pentru a minimiza varianța testului.
2.6. Analiza Statistică
Statisticile descriptive includ media și abaterea standard pentru variabilele cantitative și frecvența pentru variabilele calitative. Distribuția normală a datelor pentru fiecare variabilă a fost estimată cu testul Shapiro-Wilk. Testul neparametric Mann–Whitney U a fost efectuat pentru a verifica orice diferențe între cele două grupuri experimentale pentru variabile cantitative. Pentru a analiza modul în care modificările timpului de mers pe jos au fost legate de cantitatea de activitate fizică, am folosit testul Spearman de corelație neparametrică (forța identificată prin coeficientul rho Spearman și valoarea p). Pentru a estima amploarea modificărilor semnificative (p < 0,05) între cele două grupuri experimentale am calculat d-ul lui Cohen și mărimea efectului r (mic (d = 0,2), mediu (d = 0,5) și mare (d ≥ 0,8) ). Semnificația statistică a fost stabilită la p < 0,05 și analiza statistică a fost efectuată cu pachetul software SPSS 24.0 (SPSS Inc., Chicago, IL, SUA).
3. Rezultate
3.1. Proiectarea și studiul populației
Vârsta medie a participanților a fost 78,9 ± 7,9 (SD) (interval 65-93 ani). Nu a fost observată nicio diferență semnificativă (p = 0,81) între vârsta medie a indivizilor din grupul cu leucină (78,4 ± 8,4) comparativ cu grupul placebo (79,0 ± 7,6). Nu a fost găsită nicio diferență semnificativă (p = 0,97) în ceea ce privește distribuția pe sexe în loturile experimentale. Aportul mediu de energie la momentul inițial din rapoartele dieteticienilor a fost de 1770 ± 196 kcal/zi pentru grupul cu leucină și 1758 ± 168 kcal/zi pentru grupul placebo, fără diferențe între grupuri (p = 0,96). La 6 săptămâni de tratament, aportul mediu de energie a fost de 1632 ± 188 kcal/zi pentru grupul cu leucină și 1690 ± 204 kcal/zi pentru grupul placebo, fără diferențe între grupuri (p = 0,83). După finalizarea studiului, aportul mediu de energie a fost de 1694 ± 152 kcal/zi pentru grupul cu leucină și 1707 ± 195 kcal/zi pentru grupul placebo, fără diferențe între grupuri (p = 0,91).
Rezultatul primar măsurat a fost efectul tratamentului asupra criteriilor de sarcopenie, de exemplu, masa slabă, forța musculară, performanța fizică și funcția mușchilor respiratori, de exemplu, exprimat prin presiunile respiratorii statice maxime la nivelul gurii în timpul inspirației (MIP) și expirării (MEP) . Rezultatul secundar a fost efectul asupra activității funcționale evaluat de indicele Barthel, afectarea cognitivă prin scorul de examinare Mini Mental și starea nutrițională de către Mini.
Evaluarea nutrițională (MNA). De asemenea, am analizat dacă tratamentul a influențat valorile parametrilor analitici comuni ai sângelui și hemograma. Participanții au fost înrolați și toate evaluările clinice (sarcopenie și evaluări geriatrice) și analitice (anale de sânge) au fost efectuate la momentul inițial (săptămâna zero). Randomizarea a fost efectuată după ce au fost finalizate înscrierea și evaluările de bază. Intervenția a avut loc în perioada iunie – septembrie 2019. Participanții au fost selectați pe baza criteriilor de includere și excludere (vezi Populația studiului). Evaluarea inițială a fost efectuată cu aproximativ 5 săptămâni înainte de randomizare, din cauza problemelor de protocol etic în casele de bătrâni. În timpul săptămânii inițiale, cercetătorii s-au întâlnit cu personalul din cele trei case de bătrâni participante pentru a explica obiectivele studiului și protocolul experimental. În a doua săptămână, cercetătorii s-au întâlnit cu rezidenți ai azilelor de bătrâni care au îndeplinit criteriile de includere. În săptămâna a treia, cercetătorii s-au întâlnit cu rudele rezidenților caselor de bătrâni care îndeplineau criteriile de includere. Informarea familiilor rezidenților din casele de bătrâni a fost o cerință necesară înainte de a începe orice nouă intervenție. În ultimele două săptămâni înainte de începerea studiului, compușii au fost pregătiți, sticlele care conțineau compușii de testat au fost etichetate mascat și apoi acestea au fost expediate la casele de bătrâni (din Țările de Jos în Spania). Tratamentul cu leucină sau placebo a durat 13 săptămâni. Toți participanții au fost reevaluați (sarcopenie, evaluări geriatrice și analize de probe de sânge) în termen de 1 lună de la finalizarea studiului.
3.2. Abandonările, siguranța și conformitatea
Diagrama RCT este prezentată în Figura 1. Un total de patruzeci și doi de participanți au finalizat studiul (86,0%) (14 bărbați și 29 femei). Ratele de abandon nu au fost semnificativ diferite (p = 0,71) între grupuri (cinci participanți din grupul cu leucină și trei participanți din grupul placebo au oprit tratamentul și nu au dorit să participe din motive necunoscute). Nu au fost observate modificări semnificative (p = 0,84) în administrarea medicamentelor prescrise pentru comorbiditățile între cele două grupuri în timpul studiului. La acei indivizi care au completat întregul protocol de studiu și au fost incluse în analiză, conformitatea intervenției a fost ridicată (91,5% în grupul cu leucină și 93,5% în grupul placebo) de la momentul inițial până la urmărire și nu a diferit semnificativ între grupuri.
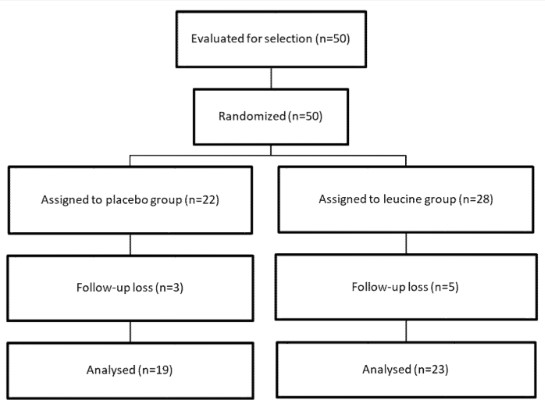
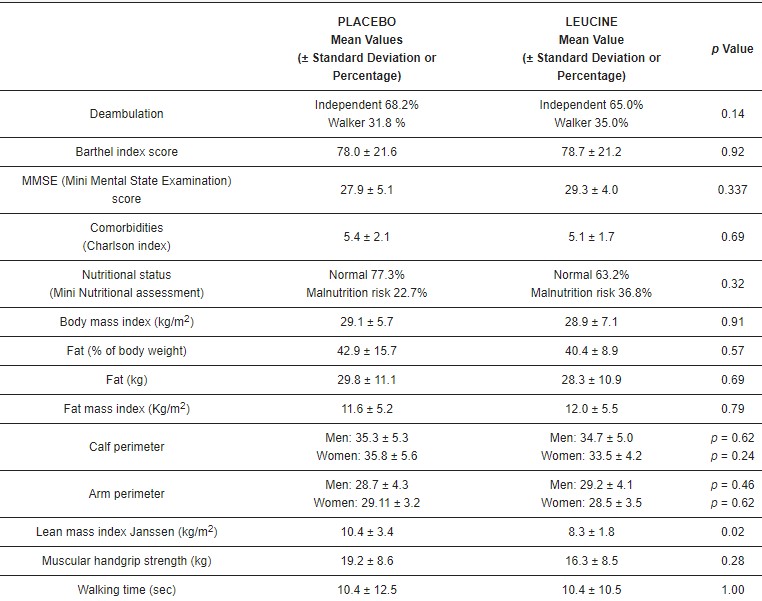
Nu au fost înregistrate evenimente adverse în rândul participanților care au renunțat la studiu. Cele două grupuri experimentale (leucină și placebo) nu au fost semnificativ diferite la momentul inițial (a se vedea tabelul 1), cu excepția indicelui de masă slabă, care a fost semnificativ mai scăzut în grupul cu leucină comparativ cu grupul martor (p = 0,02).
Tabelul 1. Caracteristicile inițiale psiho-geriatrice ale participanților înscriși în studiu.
3.3. Efectul administrării de leucină asupra criteriilor de sarcopenie
Puterea mânuirii și valorile timpului de mers nu au fost diferite între grupuri la momentul inițial (grupul cu leucină: 43,03 ± 4,10 față de grupul placebo: 35,97 ± 0,41; p = 0,242 și grupul cu leucină 10,7 ± 2,85 față de grupul placebo: 10,97 ± 0,42; p = 2,43; 0,944 respectiv). Singurele diferențe au fost în ceea ce privește indicele de masă musculară, cu o masă musculară mai mare în grupul de control comparativ cu grupul cu leucină (grupul cu leucină: 8,3 ± 1,8 față de grupul placebo: 10,4 ± 3,4; p = 0,02, d = 0,77 Cohen, efect mărimea r = 0,36). În urma intervenției, nu a existat nicio diferență între grupuri pentru indicele de masă musculară: grupul cu leucină: 8,3 ± 1,7 și grupul placebo: 9,9 ± 3,4; p = 0,08, iar în valorile rezistenței(gripul) mânerului: grupul leucină: 16,4 ± 10,7 față de grupul placebo: 18,3 ± 8,8; p = 0,55 și valorile timpului de mers pe jos au fost: grupul cu leucină: 8,27 ± 1,10 față de grupul placebo: 9,92 ± 1,05; p = 0,285. Modificările induse de administrarea de leucină în parametrii sarcopeniei, de exemplu, indicele de masă musculară scheletică, puterea(grip) mânerului și timpul de mers sunt prezentate în Figura 2A.
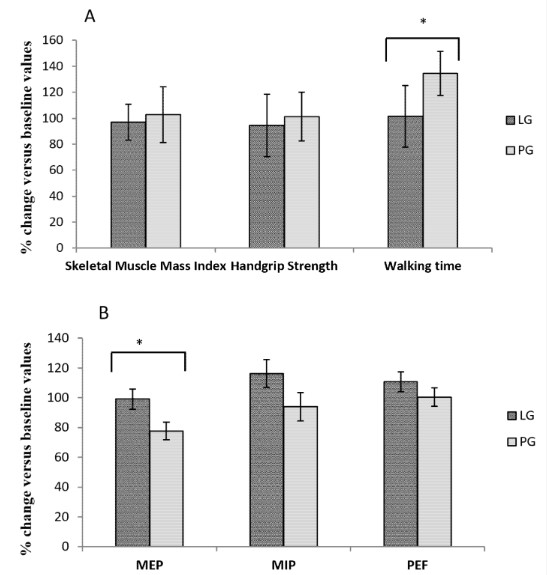
Figura 2. Efectul administrării de leucină asupra criteriilor de sarcopenie (A) și sarcopeniei respiratorii musculare (B). (A) Comparația modificărilor procentuale în comparație cu valorile inițiale după tratamentul cu leucină sau placebo pentru indicele de masă musculară, puterea(grip) mânerului și timpul de mers * p = 0,011. (B) Compararea modificărilor procentuale în comparație cu valorile inițiale după tratamentul cu leucină sau placebo pentru funcția mușchilor respiratori * p = 0,026. grupa leucină (LG); grupul placebo (PG); presiuni respiratorii maxime statice inspiratorii (MIP) si expiratorii (MEP) la nivelul gurii; debitul expirator maxim (PEF).
A existat o diferență semnificativă în timpul de mers în comparație cu nivelurile inițiale, exprimate ca 100% între grupurile cu leucină și placebo, cu o creștere a timpului necesar pentru a parcurge distanța în grupul placebo (grupul cu leucină: 101,43 ± 6,00 față de grupul placebo : 134,41 ± 10,47 p = 0,011, Cohen d = 3,88, dimensiunea efectului r = 0,89). Nu au existat diferențe semnificative între grupuri în ceea ce privește indicele de masă musculară scheletică în comparație cu nivelurile inițiale, exprimate ca 100% (grupul cu leucină: 97,09 ± 3,24 față de grupul placebo: 102,75 ± 2,29; p = 0,168) sau pentru puterea(grip) mânerului (grupul cu leucină: 94,44 ± 2,88 față de grupul placebo: 101,33 ± 8,22 p = 0,437). Modificarea semnificativă a timpului de mers pe jos a dus la o creștere a prevalenței subiecților care îndeplinesc criteriul sarcopeniei timp de mers în grupul de control (p = 0,027). Modificările procentuale ale perimetrelor gambei după administrarea de leucină au fost 97,95 ± 1,19 pentru grupul cu leucină față de 99,59 ± 1,10 pentru grupul placebo; p = 0,325. Aceeași tendință a fost observată în perimetrul brațului, fără diferențe la momentul inițial sau după tratament, sau în modificarea procentuală între grupuri (grupul cu leucină: 101,58 ± 1,48 vs. grupul placebo: 99,81 ± 2,17; p = 0,505). De asemenea, nu au existat diferențe între grupuri înainte și după tratament atunci când am analizat aceste variabile ca dihotomice în prezența sau absența sarcopeniei, conform punctelor de limită stabilite de Setiati și colab. 2010. În mod similar, nu s-au găsit diferențe între grupuri atunci când s-au analizat modificările indicelui de masă grasă (p = 0,45) sau scorul total MNA (p = 0,27) sau riscul de malnutriție (p = 0,18) pe baza unui scor limită < 24 în testul de screening MNA.
Nu a existat nicio diferență între grupuri (p = 0,929) la analiza vitezei de mers în ceea ce privește utilizarea mijloacelor de mers (persoane în vârstă care pot merge independent sau care necesită utilizarea unui baston sau a unui premergător). Când a fost studiat nivelul de efort efectuat de subiecți, nu au fost observate diferențe între subiecții din grupul cu leucină și placebo. În plus, nu au fost găsite corelații semnificative între activitatea fizică ușoară (p = 0,163, rho = 0,238, test Spearman) și nici moderată (p = 0,481, rho = 0,121, test Spearman) prin IPAQ și viteza de mers. Aceste rezultate au sugerat că îmbunătățirea timpului de mers pe jos nu a fost asociată cu cantitatea de activitate fizică auto-referită.
3.4. Efectul suplimentării cu leucină asupra criteriilor sarcopeniei ale mușchilor respiratori
Nu au fost observate diferențe între cele două loturi la momentul inițial sau după intervenție pentru parametrii funcției respiratorii stabiliți ca determinanți ai prezenței sarcopeniei respiratorii. Valorile inițiale ale MIP au fost LG: 29,85 ± 3,05 vs. PG: 29,62 ± 3,05; p = 0,958; valorile MEP au fost LG: 50,44 ± 5,14 vs. PG: 59,30 ± 3,79; p = 0,188 și valorile PEF au fost LG: 2,59 ± 0,26 vs. PG: 2,66 ± 0,27; p = 0,858. În urma intervenției, valorile MIP au fost LG: 31,89 ± 3,17 vs. PG: 26,75 ± 3,62; p = 0,291, valorile MEP au fost LG: 46,91 ± 4,68 vs. PG: 45,83 ± 4,90; p = 0,875 și valorile PEF au fost LG: 2,73 ± 0,26 vs. PG: 2,39 ± 0,20; p = 0,325. Modificările valorilor sarcopeniei respiratorii exprimate ca procent din nivelurile de bază sunt prezentate în Figura 2B. A existat o diferență semnificativă în MEP între grupul cu leucină și placebo, cu o scădere semnificativă a forței mușchilor expiratori în grupul placebo (LG: 99,05 ± 6,80 vs. PG: 77,67 ± 5,85; p = 0,026, Cohen d = 3,37, efect mărimea r = 0,86). Nu au existat diferențe statistice între grupuri pentru MIP (LG: 116,32 ± 9,44 vs. PG: 93,94 ± 9,40; p = 0,105) sau valorile PEF (LG: 110,75 ± 6,61 vs. PG: 100,0,24; ± p = 6,24; 24 ± 2,46). Având în vedere relevanța consumului de bronhodilatatoare și a fumatului, s-a decis că vom studia rezultatele obținute în acei termeni. Cu toate acestea, nu au fost găsite diferențe pentru niciunul dintre parametrii studiați în funcție de utilizarea bronhodilatatoarelor (p = 0,287; p = 0,242; p = 0,792) sau consumului de tutun (p = 0,379; p = 0,495; p = 0,380), pentru MIP , MEP și, respectiv, PEF.
3.5. Efectul administrării leucinei asupra parametrilor analitici ai sângelui
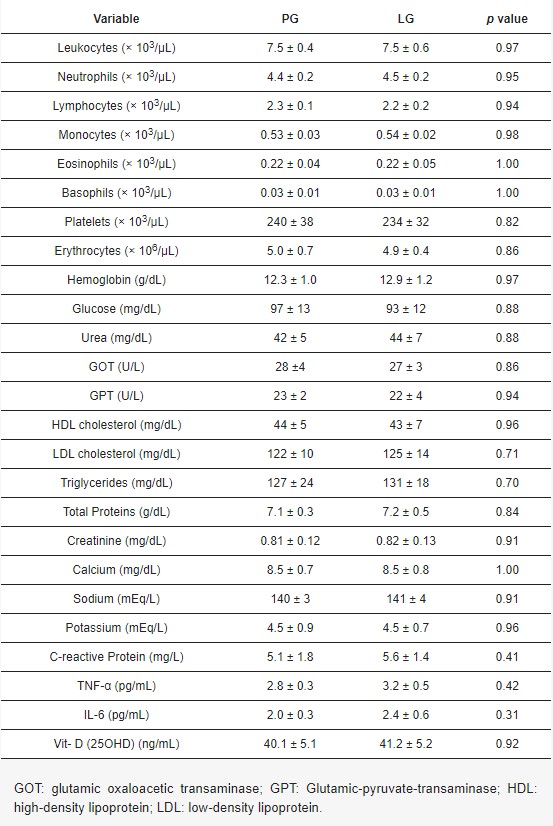
S-au efectuat analize sanguine de rutină, de exemplu, hemogramă și markeri ai funcției hepatice (transaminaze), funcției renale (creatinină), profil lipidic, glucoză și proteine totale, ioni și vitamina D (ca 25(OH)D total). În plus, am măsurat markeri ai inflamației, cum ar fi proteina C-reactivă, TNF-α și IL-6. După cum se arată în Tabelul 2, nu au fost observate diferențe semnificative între grupurile cu leucină și placebo (semnificație la p < 0,05). Nu au fost observate diferențe semnificative în acești parametri analitici între cele două grupuri la momentul inițial și după finalizarea studiului (Tabelul 2).
Tabelul 2. Analiza sângelui și hemograma după tratamentul cu grupul placebo (PG) sau grupul cu leucină (LG).
4. Discuție
Cele mai eficiente intervenții pentru tratarea sarcopeniei sau diminuarea agravării acesteia în timp se bazează în prezent pe practicarea exercițiilor fizice precum antrenamentele de rezistență și administrarea unor suplimente nutritive. Cu toate acestea, multe persoane în vârstă sunt sedentare și fie nu pot (bariere sociale și sprijin familial, deficiențe funcționale și cognitive) fie nu doresc să facă mișcare. În aceste cazuri, intervențiile nutriționale rămân cea mai promițătoare măsură pentru întârzierea progresiei sarcopeniei și prevenirea consecințelor adverse ale acesteia, cum ar fi căderile, pierderea mobilității și stilul de viață de la pat la canapea. Suplimentarea proteinei din zer care conține cantități mari de aminoacid leucină sau un amestec de aminoacizi cu lanțuri ramificate cu sau fără alte suplimente nutritive au fost cele mai frecvente intervenții testate pentru tratarea sarcopeniei la persoanele în vârstă. Cu toate acestea, efectul leucinei în monoterapie, aminoacidul care s-a dovedit a stimula sinteza musculară și reduce turnover-ul în cel mai puternic mod, a fost rareori evaluat și nu s-au efectuat studii la persoane vârstnice instituționalizate care să arate rate ridicate de sarcopenie, tulburări funcționale și de comorbidități care favorizează toate pierderea musculară. În plus, majoritatea studiilor privind suplimentarea cu proteine îmbogățite cu leucină au fost efectuate la persoane care locuiesc în comunitate, iar efectele asupra persoanelor în vârstă instituționalizate pot prezenta rezultate diferite, deoarece rata comorbidităților și a deteriorării funcționale este mai mare la persoanele instituționalizate. Suplimentarea cu leucină are efecte mici, dar semnificative asupra indicelui de masă musculară, nu pentru că a îmbunătățit acești parametri la acei indivizi suplimentați cu leucină, ci pentru că în grupul placebo a existat o scădere a acestui parametru de sarcopenie. Aceste rezultate ar putea însemna că suplimentarea cu leucină a ajutat la menținerea masei musculare slabe pe perioade mai lungi de timp. În plus, efectul benefic al menținerii stabile a masei musculare în timp poate fi legat și de îmbunătățirea stării nutriționale realizată în rândul indivizilor din grupul tratat cu leucină, deoarece la momentul inițial, 38% dintre indivizii din acest grup prezentau un risc de malnutriție (așa cum a fost evaluat prin testul MNA) și suplimentarea cu leucină ar fi putut oferi un anumit beneficiu în acest subgrup de pacienți malnutriți. În schimb, în grupul placebo, riscul de malnutriție a apărut în 23% din eșantion și este puțin probabil ca această diferență să fi explicat pierderea de masă musculară observată în grupul placebo în timp. Modificările în masa slabă nu sunt paralele cu modificările forței musculare și nu au fost observate diferențe în acest parametru între cele două grupuri. Rezultatele noastre pentru lipsa efectului asupra masei musculare și forței în grupul cu leucină sunt în concordanță cu două studii efectuate pe bărbați în vârstă, în care suplimentarea cu leucină (7,5 g/zi) nu a modificat masa musculară sau puterea nici la bărbații în vârstă sănătoși (vârsta medie de 71 de ani) sau bărbați mai în vârstă cu diabet de tip 2.
În schimb, am observat o îmbunătățire semnificativă a performanței fizice (timp de mers) după suplimentarea cu leucină în comparație cu valorile inițiale, în timp ce nu a fost observat niciun efect în grupul de control (placebo). O posibilă explicație pentru efectul benefic asupra performanței fizice la indivizii suplimentați cu leucină ar putea fi legată de faptul că performanța fizică nu este mediată doar de o masă slabă eficientă și adecvată, ci și de sistemul nervos central și periferic, modulând activitatea motorie și funcţia musculară prin unitatea neuromusculară. De fapt, efectele benefice asupra activării neuromusculare preced efectele benefice asupra creșterii masei musculare ca răspuns la antrenamentul de rezistență. În majoritatea studiilor, nu au existat paralele clare între efectul pozitiv asupra creșterii sau menținerii masei slabe și efectul pozitiv asupra forței musculare sau a performanței fizice, confirmând rolul crucial al sistemului nervos în refacerea forței musculare în sarcopenia legată de vârstă; prin urmare, prezența unui efect puternic asupra sarcopeniei necesită atât efecte benefice asupra mușchilor, cât și asupra sistemului nervos. Doar un studiu a raportat efectul benefic al suplimentelor de leucină atât asupra vitezei de mers pe jos, cât și asupra forței musculare la persoanele în vârstă dar, în acel studiu, leucina a fost administrată împreună cu alți aminoacizi esențiali (3 g/zi), vitamina D și cu trigliceride cu catenă medie (6 g) . Co-suplimentarea ar fi putut aduce beneficii forței musculare, care nu este afectată numai de suplimentarea cu leucină, așa cum se arată în prezentul RCT.
Interesant este că la persoanele în vârstă cu activitate fizică scăzută, efectul suplimentării cu leucină asupra performanței fizice semăna cu cel obținut prin exerciții fizice la indivizii cu caracteristici similare, ca în studiul de față. De fapt, un studiu recent de intervenție longitudinală asupra persoanelor vârstnice care a evaluat efectul unui program de antrenament de rezistență asupra sarcopeniei și funcționalității persoanelor în vârstă, a găsit o îmbunătățire semnificativă a performanței fizice, echilibrului și vitezei de mers în indivizii tratați cu leucină. Najafi și colab., într-un RCT efectuat la șaizeci și trei de adulți în vârstă, au arătat că o activitate fizică distractivă (inclusiv forță, echilibru, rezistență și activități de mers sub formă de mișcări de rotație a mâinilor cu bile de plastic) a redus progresia sarcopeniei prin îmbunătățirea echilibrului, creșterea distanțelor parcurse și în acest caz și întărirea mușchilor. Riscul de complicații și infecții respiratorii crește substanțial la vârsta înaintată, ceea ce se poate datora parțial sarcopeniei mușchilor diafragmei și a altor mușchi respiratori, reducând în principal capacitatea lor de generare a forței și afectând capacitatea de a efectua comportamente motorii expulsive neventilatorii critice pentru curățarea căilor respiratorii. Am evaluat funcția mușchilor respiratori și am constatat că administrarea de leucină a îmbunătățit toți parametrii mușchilor respiratori, dar efectul a fost semnificativ pentru MEP. Mai multe rapoarte au demonstrat că intervenția nutrițională poate îmbunătăți funcția mușchilor respiratori la pacienții cu boală pulmonară obstructivă cronică (BPOC), chiar și simpla suplimentare nutrițională la indivizii malnutriți poate îmbunătăți acești parametri și la pacienții cu BPOC.
Acesta este primul raport care arată că suplimentarea cu leucină poate crește funcția MEP, iar aceste efecte nu pot fi atribuite unui număr diferit de pacienți cu BPOC și utilizării corespunzătoare a medicamentelor bronhodilatatoare între cele două grupuri (patru persoane din grupul cu leucină și trei persoane din grupul placebo). Îmbunătățirile atât ale timpului de mers pe jos, cât și ale capacității respiratorii ar putea fi legate între ele prin efectul stimulator cunoscut al leucinei asupra țintei rapamicinei la mamifere (mTOR) în mușchii scheletici. Un studiu recent a arătat că suplimentarea cu leucină la șoarecii obezi induși de dietă a îmbunătățit semnificativ funcția mitocondrială în mușchii scheletici prin activarea mTOR1. Același efect a fost observat și la diafragma șobolanilor sedentari și antrenați. Masa musculară nu a crescut în ambele studii pe animale, ceea ce este, de asemenea, în concordanță cu rezultatele studiului nostru clinic. În cele din urmă, efectele benefice ale suplimentării cu leucină în acest studiu par să nu aibă legătură cu modificările markerilor inflamatori din sânge, cum ar fi numărul de leucocite, proteina C reactivă, IL-6 și TNF-alfa, care au fost toate asociate cu sarcopenia. Cu toate acestea, rolul altor molecule în cascada inflamatorie complexă nu poate fi exclus. Am evaluat concentrația de vitamina D în sânge (ca 25(OH)D total) deoarece prezintă factori importanți pentru evaluarea fiziologiei masei și funcției musculare și a sarcopeniei. Orientările actuale stabilesc deficitul de vitamina D atunci când nivelurile serice de 25-hidroxivitamina D (25(OH)D) sunt mai mici de 20 ng/mL (50 nmol/litru). În studiul nostru, nivelurile medii au fost în jur de 40 ng/mL și niciunul dintre indivizi nu a avut niveluri sub 20 ng/mL. Un raport efectuat în populația SUA (referitor la perioada 2003-2006) a afirmat că 9% aveau concentrație seric scăzută de 25-hidroxivitamina D (<50 nmol/L). Motivul pentru lipsa deficienței de vitamina D se poate datora beneficiilor instituționalizării, cum ar fi urmarea unei diete controlate de la un nutriționist/dietetician (care probabil asigură un aport adecvat de vitamina D). În plus, în casele de bătrâni din Spania, suplimentarea cu vitamina D la persoanele cu deficit este efectuată de medicii care lucrează în aceste instituții. În studiul nostru, au existat patru persoane care au primit vitamina D în grupul cu leucină și cinci persoane în grupul placebo. În toate cazurile, administrarea de vitamina D și calciu au fost prescrise ca tratamente anti-osteoporotice înainte și în timpul studiului. Nu s-au observat diferențe în rezultatele comparând indivizii sub suplimentare cu vitamina D.
Studiul prezintă câteva limitări. Au existat opt participanți (16%) care nu au dorit să continue din motive necunoscute, ceea ce ar fi putut influența rezultatele în comparație cu o analiză intenționată de a trata. Cu toate acestea, caracteristicile inițiale ale abandonului au fost comparabile cu acei subiecți incluși în analiza finală, iar rata abandonului nu a fost semnificativ diferită între grupuri. Informațiile despre sănătatea participanților nu au fost colectate săptămânal; prin urmare, nu se știe când participanții au arătat pentru prima dată îmbunătățiri pe baza criteriilor de sarcopenie. Acest studiu s-a concentrat pe modificări ale forței și funcției musculare, deși dimensiunea mușchilor nu a fost evaluată direct prin tomografie computerizată sau imagistica prin rezonanță magnetică. Astfel, nu se poate exclude că modificările masei musculare slabe ar fi putut fi detectate cu aceste măsurători mai sofisticate. Una dintre măsurătorile principale ale rezultatului, puterea (grip)mânerului, este o măsurători proxy bine validată pentru forța inferioară a corpului, dar este mai puțin sensibilă decât alte măsuri de forță. Sunt necesare cercetări suplimentare pentru a investiga rezultatele sensibile și specifice pentru sarcopenie, cum ar fi puterea și funcția extremităților inferioare. Eșantionul de populație înscris în studiul de față s-a caracterizat prin activitate fizică scăzută și majoritatea aveau un stil de viață sedentar. După cum se arată în Tabelul 1, asistența la mers (adică ajutorul de mers) a fost necesară de 31,8% în grupul placebo și 35% în grupul cu leucină. În toate casele de bătrâni participante a existat o sală de sport în care rezidenții se puteau antrena. Doar trei participanți din grupul placebo și doi participanți din grupul cu leucină au efectuat exerciții regulate, care au implicat ciclism staționar timp de aproximativ 30 de minute pe zi la o intensitate scăzută.
Toți ceilalți participanți prezenti la gimnaziu pentru a întreprinde activități psihomotorii la intensitate scăzută, cum ar fi, de exemplu, exerciții pe scaun, aruncarea și prinderea mingii. Cu toate acestea, participanții au fost stratificați pentru activitatea fizică randomizată din rezultatele IPAQ-ului auto-administrat. Trebuie remarcat faptul că niciun participant nu a efectuat activități fizice viguroase sau activități fizice moderate. Majoritatea se plimbau prin grădinile căminelor de bătrâni și aveau un stil de viață destul de sedentar. Studiile viitoare ar trebui să includă utilizarea accelerometrelor pentru evaluarea activității fizice, precum și măsurători obiective ale aptitudinii cardiorespiratorii, de exemplu, teste pe bandă de alergare sau de ciclism. Avantajul prezentului design al studiului este că poate fi implementat cu ușurință în casele de bătrâni în perioadele în care exercițiul nu este posibil, nici fezabil sau pur și simplu când rezidenții nu doresc să facă mișcare. Chiar și cele mai bune abordări pentru tratarea sarcopeniei sau amânarea progresiei acesteia în timp se bazează în prezent atât pe exerciții fizice cât și pe suplimentarea nutrițională; RCT nostru a demonstrat că această intervenție nutrițională nu afectează negativ rata de pierdere a mușchilor scheletici dar îmbunătățește performanța fizică și funcția mușchilor respiratori, care ar putea fi de asemenea, semnificativ benefice pentru persoanele instituționalizate care prezintă o povară uriașă de comorbidități și deficiențe funcționale.
By. Bitanu-Alexandru Sebastian-Alin
Referințe :
1. Cruz-Jentoft, A.J.; Baeyens, J.P.; Bauer, J.M.; Boirie, Y.; Cederholm, T.; Landi, F.; Martin, F.C.; Michel, J.-P.;
Rolland, Y.; Schneider, S.M.; et al. Sarcopenia: European consensus on definition and diagnosis: Report of
the European Working Group on Sarcopenia in Older People. Age Ageing 2010, 39, 412–423. [CrossRef]
2. Janssen, I. The epidemiology of sarcopenia. Clin. Geriatr. Med. 2011, 27, 355–363. [CrossRef]
3. von Haehling, S.; Morley, J.E.; Anker, S.D. An overview of sarcopenia: Facts and numbers on prevalence and
clinical impact. J. Cachexia Sarcopenia Muscle 2010, 1, 129–133. [CrossRef]
4. Follis, S.; Cook, A.; Bea, J.W.; Going, S.B.; Laddu, D.; Cauley, J.A.; Shadyab, A.H.; Stefanick, M.L.; Chen, Z.
Association between sarcopenic obesity and falls in a multiethnic cohort of postmenopausal women. J. Am.
Geriatr. Soc. 2018, 66, 2314–2320. [CrossRef]
5. Sim, M.; Prince, R.L.; Scott, D.; Daly, R.M.; Duque, G.; Inderjeeth, C.A.; Zhu, K.;Woodman, R.J.; Hodgson, J.M.;
Lewis, J.R. Utility of four sarcopenia criteria for the prediction of falls-related hospitalization in older
Australian women. Osteoporos. Int. 2019, 30, 167–176. [CrossRef]
Nutrients 2020, 12, 932 13 of 16
6. Srikanthan, P.; Karlamangla, A.S. Muscle mass index as a predictor of longevity in older adults. Am. J. Med.
2014, 127, 547–553. [CrossRef]
7. Cuthbertson, D.J.; Bell, J.A.; Ng, S.Y.; Kemp, G.J.; Kivimaki, M.; Hamer, M. Dynapenic obesity and the risk
of incident Type 2 diabetes: The English Longitudinal Study of Ageing. Diabet. Med. 2016, 33, 1052–1059.
[CrossRef]
8. Srikanthan, P.; Hevener, A.L.; Karlamangla, A.S. Sarcopenia exacerbates obesity-associated insulin resistance
and dysglycemia: Findings from the National Health and Nutrition Examination Survey III. PLoS ONE 2010,
5, e10805. [CrossRef]
9. Cruz-Jentoft, A.J.; Dawson Hughes, B.; Scott, D.; Sanders, K.M.; Rizzoli, R. Nutritional strategies for
maintaining muscle mass and strength from middle age to later life: A narrative review. Maturitas 2020, 132,
57–64. [CrossRef]
10. Masanés, F.; Rojano i Luque, X.; Salvà, A.; Serra-Rexach, J.A.; Artaza, I.; Formiga, F.; Cuesta, F.; López Soto, A.;
Ruiz, D.; Cruz-Jentoft, A.J. Cut-o_ points for muscle mass—Not grip strength or gait speed—Determine
variations in sarcopenia prevalence. J. Nutr. Heal. Aging 2017, 21, 825–829. [CrossRef]
11. Santos, C.D.S.; Nascimento, F.E.L. Isolated branched-chain amino acid intake and muscle protein synthesis
in humans: A biochemical review. Einstein (Sao Paulo) 2019, 17, eRB4898. [CrossRef] [PubMed]
12. Kouw, I.W.; Holwerda, A.M.; Trommelen, J.; Kramer, I.F.; Bastiaanse, J.; Halson, S.L.; Wodzig, W.K.;
Verdijk, L.B.; van Loon, L.J. Protein Ingestion before Sleep Increases Overnight Muscle Protein Synthesis
Rates in Healthy Older Men: A Randomized Controlled Trial. J. Nutr. 2017, 147, 2252–2261. [CrossRef]
[PubMed]
13. Hamarsland, H.; Nordengen, A.L.; Nyvik Aas, S.; Holte, K.; Garthe, I.; Paulsen, G.; Cotter, M.; Børsheim, E.;
Benestad, H.B.; Raastad, T. Native whey protein with high levels of leucine results in similar post-exercise
muscular anabolic responses as regular whey protein: A randomized controlled trial. J. Int. Soc. Sports Nutr.
2017, 14, 43. [CrossRef] [PubMed]
14. Martínez-Arnau, F.M.; Fonfría-Vivas, R.; Cauli, O. Beneficial e_ects of leucine supplementation on criteria
for sarcopenia: A systematic review. Nutrients 2019, 11, 2504. [CrossRef] [PubMed]
15. Komar, B.; Schwingshackl, L.; Ho_mann, G. E_ects of leucine-rich protein supplements on anthropometric
parameter and muscle strength in the elderly: A systematic review and meta-analysis. J. Nutr. Heal. Aging
2015, 19, 437–446. [CrossRef]
16. Bonnefoy, M.; Gilbert, T.; Bruyère, O.; Paillaud, E.; Raynaud-Simon, A.; Guérin, O.; Jeandel, C.; Le Sourd, B.;
Haine, M.; Ferry, M.; et al. Quels bénéfices attendre de la supplémentation en protéines pour limiter la perte
de masse et de fonction musculaire chez le sujet âgé fragile? Geriatr. Psychol. Neuropsychiatr. Vieil. 2019, 17,
137–143.
17. Janssen, I.; Heymsfield, S.B.; Baumgartner, R.N.; Ross, R. Estimation of skeletal muscle mass by bioelectrical
impedance analysis. J. Appl. Physiol. 2000, 89, 465–471. [CrossRef]
18. Miller, M.R.; Hankinson, J.; Brusasco, V.; Burgos, F.; Casaburi, R.; Coates, A.; Crapo, R.; Enright, P.; van
der Grinten, C.P.M.; Gustafsson, P.; et al. Standardisation of spirometry. Eur. Respir. J. 2005, 26, 319–338.
[CrossRef]
19. Laveneziana, P.; Albuquerque, A.; Aliverti, A.; Babb, T.; Barreiro, E.; Dres, M.; Dubé, B.P.; Fauroux, B.; Gea, J.;
Guenette, J.A.; et al. ERS statement on respiratory muscle testing at rest and during exercise. Eur. Respir. J.
2019, 53. [CrossRef]
20. ATS/ERS Statement on respiratory muscle testing. Am. J. Respir. Crit. Care Med. 2002, 166, 518–624.
[CrossRef]
21. Mahoney, F.I.; Barthel, D.W. Functional evaluation: The Barthel index. Md. State Med. J. 1965, 14, 61–65.
[PubMed]
22. Hickey, G.L.; Grant, S.W.; Dunning, J.; Siepe, M. Statistical primer: Sample size and power calculations-why,
when and how? Eur. J. Cardio Thorac. Surg. 2018, 54, 4–9. [CrossRef] [PubMed]
23. Lobo, A.; Ezquerra, J.; Gómez Burgada, F.; Sala, J.M.; Seva Díaz, A. Cognocitive mini-test (a simple practical
test to detect intellectual changes in medical patients). Actas Luso Esp. Neurol. Psiquiatr. Cienc. Afines 1979, 7,
189–202.
24. Vellas, B.; Villars, H.; Abellan, G.; Soto, M.E.; Rolland, Y.; Guigoz, Y.; Morley, J.E.; Chumlea,W.; Salva, A.;
Rubenstein, L.Z.; et al. Overview of the MNA®—Its history and challenges. J. Nutr. Heal. Aging 2006, 10,
456–463.
Nutrients 2020, 12, 932 14 of 16
25. Charlson, M.E.; Pompei, P.; Ales, K.L.; MacKenzie, C.R. A new method of classifying prognostic comorbidity
in longitudinal studies: Development and validation. J. Chronic Dis. 1987, 40, 373–383. [CrossRef]
26. Setiati, S.; Istanti, R.; Andayani, R.; Kuswardhani, R.A.T.; Aryana, I.G.P.S.; Putu, I.D.; Apandi, M.; Ichwani, J.;
Soewoto, S.; Dinda, R.; et al. Cut-o_ of anthropometry measurement and nutritional status among elderly
outpatient in Indonesia: Multi-centre study. Acta Med. Indones. 2010, 42, 224–230. [PubMed]
27. Makanae, Y.; Fujita, S. Role of Exercise and Nutrition in the Prevention of Sarcopenia. J. Nutr. Sci. Vitaminol.
2015, 61, S125–S127. [CrossRef]
28. Kirk, B.; Mooney, K.; Amirabdollahian, F.; Khaiyat, O. Exercise and Dietary-Protein as a Countermeasure to
Skeletal Muscle Weakness: Liverpool Hope University—Sarcopenia Aging Trial (LHU-SAT). Front. Physiol.
2019, 10, 445. [CrossRef]
29. Tang, J.E.; Moore, D.R.; Kujbida, G.W.; Tarnopolsky, M.A.; Phillips, S.M. Ingestion of whey hydrolysate,
casein, or soy protein isolate: E_ects on mixed muscle protein synthesis at rest and following resistance
exercise in young men. J. Appl. Physiol. 2009, 107, 987–992. [CrossRef]
30. Abe, S.; Ezaki, O.; Suzuki, M. Medium-chain triglycerides in combination with leucine and Vitamin D
increase muscle strength and function in frail elderly adults in a randomized controlled trial. J. Nutr. 2016,
146, 1017–1026. [CrossRef]
31. Bukhari, S.S.I.; Phillips, B.E.; Wilkinson, D.J.; Limb, M.C.; Rankin, D.; Mitchell, W.K.; Kobayashi, H.;
Greenha_, P.L.; Smith, K.; Atherton, P.J. Intake of low-dose leucine-rich essential amino acids stimulates
muscle anabolism equivalently to bolus whey protein in older women at rest and after exercise. Am. J.
Physiol. Endocrinol. Metab. 2015, 308, E1056–E1065. [CrossRef] [PubMed]
32. Ispoglou, T.; White, H.; Preston, T.; McElhone, S.; McKenna, J.; Hind, K. Double-blind, placebo-controlled
pilot trial of L-Leucine-enriched amino-acid mixtures on body composition and physical performance in
men and women aged 65–75 years. Eur. J. Clin. Nutr. 2016, 70, 182–188. [CrossRef] [PubMed]
33. Kim, H.K.; Suzuki, T.; Saito, K.; Yoshida, H.; Kobayashi, H.; Kato, H.; Katayama, M. E_ects of exercise and
amino acid supplementation on body composition and physical function in community-dwelling elderly
Japanese sarcopenic women: A randomized controlled trial. J. Am. Geriatr. Soc. 2012, 60, 16–23. [CrossRef]
[PubMed]
34. Dal Negro, R.W.; Testa, A.; Aquilani, R.; Tognella, S.; Pasini, E.; Barbieri, A.; Boschi, F. Essential amino acid
supplementation in patients with severe COPD: A step towards home rehabilitation. Monaldi Arch. Chest Dis.
2012, 77, 67–75. [CrossRef] [PubMed]
35. Rondanelli, M.; Klersy, C.; Terracol, G.; Talluri, J.; Maugeri, R.; Guido, D.; Faliva, M.A.; Solerte, B.S.;
Fioravanti, M.; Lukaski, H.; et al. Whey protein, amino acids, and vitamin D supplementation with physical
activity increases fat-free mass and strength, functionality, and quality of life and decreases inflammation in
sarcopenic elderly. Am. J. Clin. Nutr. 2016, 103, 830–840. [CrossRef]
36. Verreijen, A.M.; Verlaan, S.; Engberink, M.F.; Swinkels, S.; de Vogel-van den Bosch, J.;Weijs, P.J.M. A high
whey protein-, leucine-, and vitamin D-enriched supplement preserves muscle mass during intentional
weight loss in obese older adults: A double-blind randomized controlled trial. Am. J. Clin. Nutr. 2015, 101,
279–286. [CrossRef]
37. Verhoeven, S.; Vanschoonbeek, K.; Verdijk, L.B.; Koopman, R.;Wodzig,W.K.W.H.; Dendale, P.; van Loon, L.J.C.
Long-term leucine supplementation does not increase muscle mass or strength in healthy elderly men. Am. J.
Clin. Nutr. 2009, 89, 1468–1475. [CrossRef]
38. Leenders, M.; Verdijk, L.B.; van der Hoeven, L.; van Kranenburg, J.; Hartgens, F.; Wodzig, W.K.W.H.;
Saris, W.H.M.; van Loon, L.J.C. Prolonged leucine supplementation does not augment muscle mass or a_ect
glycemic control in elderly type 2 diabetic men. J. Nutr. 2011, 141, 1070–1076. [CrossRef]
39. Tieland, M.; Trouwborst, I.; Clark, B.C. Skeletal muscle performance and ageing. J. Cachexia Sarcopenia Muscle
2018, 9, 3–19. [CrossRef]
40. McGregor, R.A.; Cameron-Smith, D.; Poppitt, S.D. It is not just muscle mass: A review of muscle quality,
composition and metabolism during ageing as determinants of muscle function and mobility in later life.
Longev. Heal. 2014, 3, 9. [CrossRef]
41. Bano, G.; Trevisan, C.; Carraro, S.; Solmi, M.; Luchini, C.; Stubbs, B.; Manzato, E.; Sergi, G.; Veronese, N.
Inflammation and sarcopenia: A systematic review and meta-analysis. Maturitas 2017, 96, 10–15. [CrossRef]
[PubMed]
Nutrients 2020, 12, 932 15 of 16
42. del Campo Cervantes, J.M.; Macías Cervantes, M.H.; Monroy Torres, R. E_ect of a resistance training program
on sarcopenia and functionality of the older adults living in a nursing home. J. Nutr. Heal. Aging 2019, 23,
829–836. [CrossRef] [PubMed]
43. Najafi, Z.; Kooshyar, H.; Mazloom, R.; Azhari, A. The e_ect of fun physical activities on sarcopenia progression
among elderly residents in nursing homes: A randomized controlled trial. J. Caring Sci. 2018, 7, 137–142.
[CrossRef] [PubMed]
44. Elliott, J.E.; Greising, S.M.; Mantilla, C.B.; Sieck, G.C. Functional impact of sarcopenia in respiratory muscles.
Respir. Physiol. Neurobiol. 2016, 226, 137–146. [CrossRef]
45. Bone, A.E.; Hepgul, N.; Kon, S.; Maddocks, M. Sarcopenia and frailty in chronic respiratory disease. Chronic
Respir. Dis. 2017, 14, 85–99. [CrossRef]
46. Knowles, J.B.; Fairbarn, M.S.; Wiggs, B.J.; Chan-Yan, C.; Pardy, R.L. Dietary supplementation and respiratory
muscle performance in patients with COPD. Chest 1988, 93, 977–983. [CrossRef]
47. Borghi-Silva, A.; Baldissera, V.; Sampaio, L.M.M.; Pires-DiLorenzo, V.A.; Jamami, M.; Demonte, A.;
Marchini, J.S.; Costa, D. L-carnitine as an ergogenic aid for patients with chronic obstructive pulmonary
disease submitted to whole-body and respiratory muscle training programs. Braz. J. Med. Biol. Res. 2006, 39,
465–474. [CrossRef]
48. Rafiq, R.; Prins, H.J.; Boersma,W.G.; Daniels, J.M.A.; den Heijer, M.; Lips, P.; de Jongh, R.T. E_ects of daily
vitamin D supplementation on respiratory muscle strength and physical performance in vitamin D-deficient
COPD patients: A pilot trial. Int. J. COPD 2017, 12, 2583–2592. [CrossRef]
49. Rogers, R.M.; Donahoe, M.; Costantino, J. Physiologic e_ects of oral supplemental feeding in malnourished
patients with chronic obstructive pulmonary disease: A randomized control study. Am. Rev. Respir. Dis.
1992, 146, 1511–1517. [CrossRef]
50. Ferreira, I.M.; Verreschi, I.T.; Nery, L.E.; Goldstein, R.S.; Zamel, N.; Brooks, D.; Jardim, J.R. The influence of 6
months of oral anabolic steroids on body mass and respiratory muscles in undernourished COPD patients.
Chest 1998, 114, 19–28. [CrossRef]
51. De Bandt, J.-P. Leucine and mammalian target of rapamycin-dependent activation of muscle protein synthesis
in aging. J. Nutr. 2016, 146, 2616S–2624S. [CrossRef] [PubMed]
52. Brunetta, H.S.; de Camargo, C.Q.; Nunes, E.A. Does l-leucine supplementation cause any e_ect on glucose
homeostasis in rodent models of glucose intolerance? A systematic review. Amino Acids 2018, 50, 1663–1678.
[CrossRef]
53. Lollo, P.C.B.; Silva, L.B.C.; Batista, T.M.; Morato, P.N.; Moura, C.S.; Cruz, A.G.; Faria, J.A.F.; Carneiro, E.M.;
Amaya-Farfan, J. E_ects of whey protein and casein plus leucine on diaphragm the mTOR pathway of
sedentary, trained rats. Food Res. Int. 2012, 49, 416–424. [CrossRef]
54. Can, B.; Kara, O.; Kizilarslanoglu, M.C.; Arik, G.; Aycicek, G.S.; Sumer, F.; Civelek, R.; Demirtas, C.; Ulger, Z.
Serum markers of inflammation and oxidative stress in sarcopenia. Aging Clin. Exp. Res. 2017, 29, 745–752.
[CrossRef] [PubMed]
55. Bian, A.L.; Hu, H.Y.; Rong, Y.D.;Wang, J.;Wang, J.X.; Zhou, X.Z. A study on relationship between elderly
sarcopenia and inflammatory factors IL-6 and TNF-_. Eur. J. Med. Res. 2017, 22, 25. [CrossRef] [PubMed]
56. Rong, Y.D.; Bian, A.L.; Hu, H.Y.; Ma, Y.; Zhou, X.Z. Study on relationship between elderly sarcopenia and
inflammatory cytokine IL-6, anti-inflammatory cytokine IL-10. BMC Geriatr. 2018, 18, 308. [CrossRef]
57. Remelli, F.; Vitali, A.; Zurlo, A.; Volpato, S. Vitamin D deficiency and sarcopenia in older persons. Nutrients
2019, 11, 2861. [CrossRef]
58. Pludowski, P.; Holick, M.F.; Grant, W.B.; Konstantynowicz, J.; Mascarenhas, M.R.; Haq, A.; Povoroznyuk, V.;
Balatska, N.; Paula, A.; Karonova, T.; et al. Vitamin D supplementation guidelines. J. Steroid Biochem.
Mol. Biol. 2017, 175, 11. [CrossRef]
59. Pfei_er, C.M.; Sternberg, M.R.; Schleicher, R.L.; Haynes, B.M.H.; Rybak, M.E.; Pirkle, J.L. The CDC’s second
national report on biochemical indicators of diet and nutrition in the U.S. population is a valuable tool for
researchers and policy makers. J. Nutr. 2013, 143, 938S–947S. [CrossRef]
60. Holick, M.F.; Binkley, N.C.; Bischo_-Ferrari, H.A.; Gordon, C.M.; Hanley, D.A.; Heaney, R.P.; Murad, M.H.;
Weaver, C.M. Evaluation, treatment, and prevention of vitamin D deficiency: An endocrine society clinical
practice guideline. J. Clin. Endocrinol. Metab. 2011, 96, 1911–1930. [CrossRef]
Nutrients 2020, 12, 932 16 of 16
61. Tieland, M.; Verdijk, L.B.; de Groot, L.C.P.G.M.; van Loon, L.J.C. Handgrip strength does not represent an
appropriate measure to evaluate changes in muscle strength during an exercise intervention program in frail
older people. Int. J. Sport Nutr. Exerc. Metab. 2015, 25, 27–36. [CrossRef] [PubMed]
62. Coelho-Júnior, H.J.; de Oliveira Gonçalvez, I.; Sampaio, R.A.C.; Sewo Sampaio, P.Y.; Cadore, E.L.;
Izquierdo, M.; Marzetti, E.; Uchida, M.C. Periodized and non-periodized resistance training programs on
body composition and physical function of older women. Exp. Gerontol. 2019, 121, 10–18. [CrossRef]
[PubMed]
63. Osuka, Y.; Kojima, N.; Wakaba, K.; Miyauchi, D.; Tanaka, K.; Kim, H. E_ects of resistance training
and/or beta-hydroxy-beta-methylbutyrate supplementation on muscle mass, muscle strength and physical
performance in older women with reduced muscle mass: Protocol for a randomised, double-blind,
placebo-controlled trial. BMJ Open 2019, 9, e025723. [CrossRef] [PubMed]
64. Tsuzuku, S.; Kajioka, T.; Sakakibara, H.; Shimaoka, K. Slow movement resistance training using body weight
improves muscle mass in the elderly: A randomized controlled trial. Scand. J. Med. Sci. Sports 2018, 28,
1339–1344. [CrossRef] [PubMed]