Manipularea aportului alimentar și modificările concentrațiilor de testosteron.

Testosteronul, împreună cu metabolitul său puternic, dihidrotestosteronul (DHT), sunt principalii androgeni ai mamiferelor (masculi), inclusiv a oamenilor. Sunt hormoni importanți pentru diferite procese biologice și sunt vitali pentru dezvoltarea și menținerea caracteristicilor masculine secundare. Ei sunt, de asemenea, esențiali pentru funcțiile de reproducere, compoziția corpului, sănătatea mușchilor și a oaselor.
Ca steroid anabolic primar, testosteronul promovează o creștere a producției de proteine, precum și stimularea atât a funcțiilor anabolice, cât și anticatabolice în mușchii scheletici și țesutul neuronal, ceea ce duce la creșterea forței musculare, a puterii, rezistenței și hipertrofiei într-o manieră dependentă de doză. Testosteronul este, de asemenea, responsabil pentru masa, densitatea și rezistența osului. În ceea ce privește efectele sale androgenice, testosteronul mediază dezvoltarea caracteristicilor masculine primare și secundare, cum ar fi creșterea organelor sexuale, adâncirea vocii și creșterea părului facial și corporal.
Din punct de vedere structural, testosteronul are o structură caracteristică de steroizi C18 cu patru inele și este sintetizat din colesterol printr-un proces enzimatic în mai multe etape, în principal în celulele Leydig (~95%), care sunt situate în interstițiul testiculelor. Glandele suprarenale produc, de asemenea, cantități mici (~5%) de androgeni. La femei, testosteronul este produs în cantități mult mai mici, în principal din glandele suprarenale și ovare. Există două căi metabolice, căile progesteronului (delta-4) și dehidroepiandrosteronului (DHEA) (delta-5). Odată sintetizat, testosteronul este secretat în fluxul sanguin și livrat către țesutul țintă. În sânge, majoritatea testosteronului este transportat legat de mai multe proteine, în principal albumina serică și globulina care leagă hormonii sexuali (SHBG). O cantitate mică este transportată nelegată, denumită testosteron liber (FT). FT este forma activă a testosteronului, în timp ce testosteronul legat de proteine este inactiv. Când testosteronul ajunge la țesuturile țintă, difuzează prin membrana grasă a celulelor, unde poate interacționa cu receptorul său stimulând efectele biologice sau poate fi redus în DHT de enzima citoplasmatică 5α-reductaza, care este foarte exprimată în organele reproducătoare masculine, pielea și creierul.
Testosteronul este sintetizat sub controlul axului hipotalamo-hipofizo-gonadal anterior. Hormonul de eliberare a gonadotropinei (GnRH), eliberat din hipotalamus, stimulează eliberarea hormonului luteinizant (LH) din glanda pituitară anterioară în circulație. LH stimulează apoi celulele Leydig din testicule pentru a sintetiza testosteron. Creșterea concentrațiilor circulante de testosteron va avea ca rezultat o inhibare a eliberării gonadotrofinelor (GnRH și LH) printr-un mecanism de buclă de feedback negativ. GnRH funcționează sub controlul mai multor neuropeptide hipotalamice.
Efectele biologice clasice ale androgenilor sunt mediate în primul rând de legarea FT de receptorul androgenic (AR). DHT se leagă de același AR chiar mai puternic decât testosteronul, astfel încât potența sa androgenă este de aproximativ cinci ori mai puternică decât testosteronul. Complexul AR suferă o schimbare structurală care îi permite să se deplaseze în nucleul celulei și să se lege direct de secvențe de nucleotide specifice ale ADN-ului, ducând la transcrierea anumitor gene. Complexul AR în sine servește ca factor de transcripție. Testosteronul poate fi, de asemenea, transformat în estradiol (E2) de către enzima aromatază și apoi activează anumiți receptori de estrogen. Osul, țesutul adipos și creierul sunt țesuturi în care efectul principal al testosteronului este prin aromatizarea la E2. Enzima aromatază este un membru al superfamiliei de enzime citocrom P450 care catalizează conversia androstenedionei și testosteronului în steroizii estrogenici aromatici estronă și respectiv estradiol. Aceștia sunt ultimii pași cheie în catalizarea androgenilor în estrogeni, prin urmare inhibarea activității aromatazei poate crește concentrațiile de androgeni. Există numeroase substanțe naturale care au fost testate științific sau sugerate pentru a inhiba activitatea aromatazei, alături de compuși farmaceutici a căror utilizare non-medicală este considerată ilegală.
Manipularea concentrațiilor de testosteron fără utilizarea de steroizi anabolizanți a fost un subiect foarte investigat din cauza efectului cunoscut pe care îl are testosteronul asupra îmbunătățirii performanței atletice. Deși utilizarea androgenilor în atletismul competițional este ilegală, aceasta nu a oprit căutarea unor modalități „naturale” de a crește concentrațiile de testosteron. În această revizuire, vom examina efectul specific al diferitilor macronutrienți și micronutrienți asupra creșterii concentrațiilor circulante de testosteron în repaus și în timpul exercițiilor fizice. În plus, vom discuta și despre rolul disponibilității scăzute de energie, o condiție în creștere în populația sportivă și efectul acesteia asupra concentrațiilor de testosteron. În timp ce alte recenzii au discutat anterior, efectul nutriției asupra statusului testosteronului, majoritatea acestor lucrări au examinat rolul unui singur nutrient (macro/micro) sau al grupurilor de alimente. Din câte știm, această recenzie este prima care se concentrează asupra influenței nutrienților asupra concentrațiilor circulante de testosteron. Scopul său este de a oferi o evaluare bazată pe dovezi a modului în care nutrienții specifici găsiți în dietă sau manipularea dietei specifice pot îmbunătăți răspunsul androgenic, presupunând că creșterea androgenilor circulanți va îmbunătăți răspunsul anabolic și poate îmbunătăți performanța la efort.
- Extracte de produse naturale și inhibarea aromatazei
Extractele din multe surse naturale și nutrienți, o parte dintre ele utilizate de medicina tradițională, au fost testate și s-au dovedit că posedă activitate de inhibare a aromatazei. Figura 1 oferă o privire de ansamblu asupra efectului pe care acești diferiți compuși îl au asupra activității aromatazei. Aceste surse naturale includ Brassaiopsis glomerulata din familia de plante Araliaceae (adică ginseng). Această specie are mai multe utilizări medicinale raportate în sudul și sud-estul Asiei, cum ar fi tratamentul reumatismului și durerilor de spate, ajutând la digestie și ameliorarea constipației, tratarea fracturilor și entorselor osoase și a altor probleme de sănătate. Balunas și colegii au raportat o inhibare puternică a aromatazei a extractului hexan de Brassaiopsis glomerulata, cuplată cu posibilitatea unui profil de siguranță favorabil. Cicadele au fost folosite de numeroase culturi în scopuri medicinale, cum ar fi tratamentul anumitor tumori, tratarea rănilor, hemoroizilor și multe altele. Kowalska și colegii au raportat că cinci specii diferite de cycad folia au activitate de inhibare a aromatazei. Acești cercetători au raportat că alte câteva specii de plante posedă și capacități de inhibare a aromatazei similare cu inhibitorul puternic de aromatază, l0-propargylestr.4-ene-3,17-diona, inclusiv membri ai familiilor Loranthaceae, Santalaceae și Zingiberaceae, toate plante cu flori.
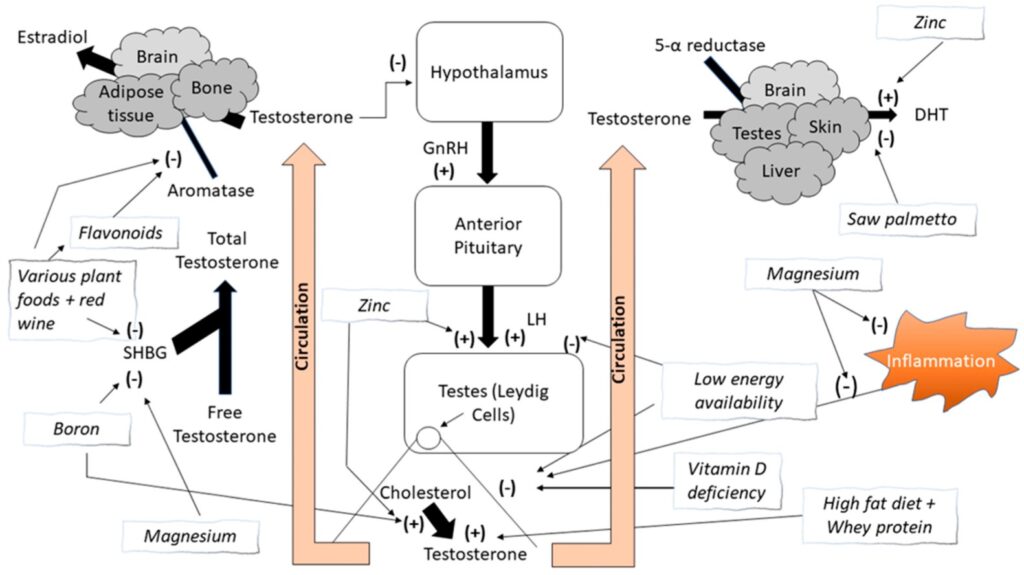
Figura 1. Efectul diferitelor grupe de alimente, macronutrienți și micronutrienți asupra circulației testosteronului și mecanismele sale propuse. (+) = Crește sau stimulează; (−) = Scade sau inhibă; DHT = dihidrotestosteron; LH = hormon luteinizant; SHBG = globulina de legare a hormonilor sexuali.
Isodon excisus var. coreanus, un membru al familiei Lamiaceae, este una dintre plantele endemice din Coreea și a fost folosită pentru tratamentul anorexiei, indigestiei, durerilor de stomac, inflamației și carcinomului esofagian. Jeong și colegii săi au raportat patru compuși izolați din această plantă, inclusiv extract de eter dietilic, inflexină, acid ursolic și 3-O-acetat de acid ursolic, care au activitate inhibitorie semnificativă a aromatazei. Lee și colegii săi au raportat că extractele din Euonymus alatus, un membru al familiei Celastraceae, au de asemenea, o inhibare puternică a aromatazei.
Beneficiile vinului roșu pentru sănătate au fost bine examinate iar în ultimele decenii studiile au raportat că consumul de vin roșu are efecte antioxidante, de reglare a lipidelor și antiinflamatoare. Interesant, s-a raportat că vinul roșu are ca rezultat inhibarea aromatazei. Au existat cinci soiuri de vin roșu despre care s-a raportat activitate de inhibare a aromatazei, cel mai activ fiind cabernet sauvignon. În concordanță cu beneficiile anti-aromataze asociate cu vinul roșu, Kijima și colegii săi au raportat că extractul de semințe de struguri este un inhibitor puternic al aromatazei și un supresor al expresiei aromatazei. Shufelt și colegii au raportat că consumul de vin roșu a dus la concentrații semnificativ mai mari de FT și concentrații mai scăzute de SHBG și E2 la femei. Acest lucru poate avea implicații importante în ceea ce privește riscul de cancer de sân. Interesant, vinul roșu a fost semnificativ mai benefic decât vinul alb. Nu este bine înțeles dacă același răspuns este văzut la bărbați.
S-a raportat, de asemenea, că alte grupuri de alimente au activitate anti-aromataze. Ciupercile albe sunt cunoscute pentru creșterea răspunsului imun înnăscut și pentru rolul lor în metabolismul grăsimilor, ceea ce duce la scăderea concentrației de colesterol. Grube și colegii săi au raportat că consumul de ciuperci albe poate inhiba activitatea aromatazei și proliferarea celulelor canceroase de sân la femei. Cu toate acestea, există dovezi limitate în acest sens la bărbați. Extractul de floare de trifoi roșu, adesea folosit pentru a îmbunătăți textura părului și a pielii, sa raportat, de asemenea, că inhibă activitatea 5-α-reductazei. Interesant, Almstrup și colegii au raportat că florile de trifoi roșu inhibă activitatea aromatazei la concentrații scăzute, dar devin estrogenice la concentrații mai mari, rezultând o curbă doză-răspuns în formă de U.
Balunas și colegii săi au raportat că un extract dintr-un fruct tropical numit mangosteen are capacități puternice de inhibiție a enzimei aromatazei. Deși această echipă de cercetare s-a concentrat în primul rând pe rolul pe care l-a avut acest fruct în prevenirea sau tratarea cancerului de sân, alții au examinat efectul ergogenic al acestui fruct. Konda și colegii săi au examinat efectele ergogenice ale Garcina mangostana atât asupra rozătoarelor cât și asupra oamenilor. Șoarecii suplimentați cu Garcina mangostana au experimentat timpi de înot, distanță de înot și putere de prindere semnificativ mai mari decât șoarecii de control. În plus, bărbaților antrenați pentru rezistență li s-au administrat 42 de zile de supliment (800 mg·zi-1) și au experimentat creșteri semnificative mai mari ale forței maxime la impins din decubit dorsal și presa pentru picioare, comparativ cu un grup controlat cu placebo. În plus, grupul care a consumat suplimentul a efectuat mult mai multe repetări la exercițiul de extensie a picioarelor și a realizat creșteri semnificativ mai mari ale masei corporale slabe și ale circumferinței brațului decât grupul placebo. Au fost raportate îmbunătățiri semnificative ale concentrațiilor de FT în grupul cu supliment, comparativ cu grupul placebo. Din câte știm, acesta este singurul studiu care a examinat efectele anabolice ale Garcina mangostana la oameni. Cercetări suplimentare asupra acestui extract par justificate.
Sultan și colegii au raportat că un extract din saw palmetto (Serenoa repens), un tip de palmier, scade in vitro 5α-reductaza a androgenilor. Saw Palmetto a fost folosit pentru a trata infecțiile tractului urinar și bolile de prostată. Sudeep și colegii săi au investigat 12 săptămâni de suplimentare cu ulei de saw palmetto pe bărbații cu deficiență de androgeni și au raportat creșteri semnificative atât ale concentrațiilor de FT, cât și ale calității vieții la bărbații suplimentați, comparativ cu bărbații tratați cu placebo. Alții au raportat că două săptămâni de suplimentare cu saw palmetto pot crește semnificativ testosteronul total și pot scădea concentrațiile de DHT și E2 folosind atât doze mici (800 mg·zi-1) cât și mari (2000 mg·zi-1). Deși eficacitatea saw palmetto a fost demonstrată la bărbații cu deficiență de androgeni, există date limitate despre bărbații mai tineri, eugonadali.
Există numeroase alte extracte de plante din guză, frunze de roșii, ceai, cafea, cacao, varză, frunze de cartofi care au fost raportate că au activitate de inhibare ridicată a aromatazei. Cu toate acestea, majoritatea cercetărilor au fost efectuate pe populații relevante din punct de vedere clinic și nu pe bărbați tineri, sportivi, pentru a îmbunătăți răspunsul la androgeni. Indiferent, mecanismul responsabil pentru o mare parte a inhibării aromatazei atribuite acestor produse este atribuit conținutului de flavonoide al acestor nutrienți.
- Flavonoide
S-a sugerat că mai mulți compuși aparținând clasei de flavonoide acționează ca inhibitori de aromatază. Flavonoidele sunt un grup de substanțe naturale cu structuri fenolice variabile. Ei aparțin unei clase de metaboliți secundari ai plantelor și se găsesc pe scară largă în fructe, legume și anumite băuturi. Aceste produse naturale sunt bine cunoscute pentru efectele lor benefice asupra sănătății datorită proprietăților lor antioxidante, antiinflamatorii, anti-mutagene și anti-carcinogene, cuplate cu capacitatea lor de a modula funcțiile cheie ale enzimelor celulare, inclusiv inhibarea aromatazei. Majoritatea activităților biologice ale flavonoidelor sunt atribuite unei grupări catecol din inelul lor B, 2,3-dublă legătură conjugată cu funcția 4-oxo și o grupare 3- (și 5-) hidroxi care captează anionii superoxid, hidroxil, radicalii peroxil, alcoxil și oxid nitric și prin aceasta elimină peroxidarea lipidelor.
Există numeroase tipuri de flavonoide care se găsesc în diferite alimente, oferind o potențială activitate anti-aromataze în mulți dintre nutrienții obișnuiți în dieta cuiva. Apigenina este un flavonoid care se găsește în multe fructe și legume, dar se găsește frecvent în ceaiul de pătrunjel, țelină și mușețel. Flavonoidele se găsesc și în bere. Berea bogată în xantohumol conține o concentrație mare de prenilflavonoide și este remarcată pentru capacitatea sa de a inhiba activitatea aromatazei. Alte flavonoide, cum ar fi catechinele, există în concentrații mari în cacao, sucul de prune și uleiul de Açaí.
Neves și colegii săi au identificat mai multe flavonoide ca inhibitori de aromatază egali sau mai buni în comparație cu medicamentul anti-aromataze aminoglutetimida, inclusiv flavone, flavanone, resveratrol și oleuropeină. Flavonele și flavanone se găsesc în multe fructe și ceai verde, resveratrolul este unul dintre componentele principale ale vinului roșu, iar oleuropeina se găsește în uleiul de măsline. Mai multe studii au raportat activitate anti-aromatazei ridicate în crizina, un flavonoid prezent în concentrații mari în miere și propolis. Cu toate acestea, alții au raportat nicio modificare a concentrațiilor de testosteron la bărbații care consumau miere și propolis timp de 21 de zile. Consumul de alimente sau suplimente alimentare care conțin nutrienți cu inhibitori de aromatază poate oferi un efect ergogenic prin inhibarea conversiei testosteronului în estradiol, crescând indirect concentrațiile de testosteron. Din păcate, majoritatea studiilor care s-au concentrat pe efectul diferitelor alimente asupra inhibării aromatazei s-au interesat în primul rând de potențiala utilizare clinică pentru tratamentul sau prevenirea diferitelor boli precum cancerul de sân și nu de potențialul ergogenic pe care îl pot avea pentru sportivii de competiție. Sunt necesare cercetări suplimentare pentru a investiga efectul ergogenic potențial pe care inhibitorii de aromatază îl au asupra concentrațiilor de testosteron în populațiile sportive.
- Alți nutrienți
Au existat și alți nutrienți naturali care s-au sugerat că au un efect anabolic potențial prin creșterea concentrațiilor de testosteron. Un supliment cu mai multe ingrediente constând din indol-3-carbinol (un extract din legume crucifere), chrysin, saw palmetto și Tribulus terrestris, o plantă din familia Caltrop, consumată în combinație cu pro-hormonii androstendionă și dehidroepiandrosteron a crescut concentrația de FT într-o măsură mai mare la bărbații de vârstă mijlocie, comparat numai pro-hormonii. Alții au examinat capacitatea elementului bor asupra capacității sale de creștere a testosteronului. Dovezile indică creșteri semnificative ale concentrațiilor de testosteron la femeile aflate în postmenopauză și la bărbații sănătoși după suplimentarea cu bor, dar alți halterofili care au examinat nu au arătat nicio diferență între sportivii care au suplimentat cu bor în comparație cu placebo. Mecanismul a sugerat că creșterea concentrațiilor de testosteron din aportul de bor este legată de rolul borului în etapa de hidroxilare în timpul formării testosteronului și de capacitatea sa de a scădea SHBG. O scădere a nivelurilor de SHBG ar duce la o creștere a concentrațiilor de FT. Diverse alimente precum fructele, tuberculii, vinul, cidrul, berea, cafeaua, laptele, fasolea uscată și fiartă, cartofii și leguminoasele conțin cele mai mari cantități de bor. Cercetări suplimentare par justificate în ceea ce privește eficacitatea borului în creșterea concentrațiilor de testosteron.
Fosfatidilserina (PS) a fost, de asemenea, propusă pentru a îmbunătăți răspunsul anabolic la exerciții fizice. Cu toate acestea, există doar dovezi umane limitate care susțin această ipoteză. PS este un fosfolipid găsit în membrana celulară a unei varietăți de țesuturi, inclusiv creierul, plămânii, inima, ficatul și mușchiul scheletic. Cele mai bune surse alimentare de PS sunt organele precum creierul, ficatul, inima și rinichii. Peștele gras, carnea și fasolea albă pot oferi PS în cantități mai mici. Într-un studiu pe bărbați tineri sănătoși, Starks și colegii săi au raportat că suplimentarea cu PS a crescut semnificativ raportul testosteron și cortizol în timpul unui exercițiu de intensitate moderată pe un cicloergometru. În ciuda acestor rezultate pozitive, nu pare să existe nicio cercetare suplimentară care să susțină rolul PS asupra modificărilor concentrațiilor de testosteron. Cu toate acestea, alți cercetători care au examinat o altă fosfolipidă (adică acidul fosfatidic) au raportat o creștere atât a forței, cât și a grosimii musculare la bărbații tineri și sănătoși. Cu toate acestea, mecanismul care a fost sugerat a fost legat de rolul pe care îl poate avea acidul fosfatidic în stimularea căii de semnalizare a proteinei mTor și nu de un răspuns androgen crescut. Cu toate acestea, acesta din urmă nu a fost măsurat.
Se pare că există o abundență de stimulente de testosteron care sunt comercializate consumatorului. Balasubramanian și colegii săi au examinat recent eficacitatea celor cinci produse de top și au raportat că numărul de studii efectuate pe oameni nu a oferit dovezi definitive pentru eficacitatea acestor produse. În mod similar, Clemesha și colegii săi au raportat că doar ~ 25% din cele 50 de produse pe care le-au testat pretinzând că sunt stimulatoare de testosteron au avut date științifice care să susțină afirmațiile lor. Acesta este un domeniu de studiu care atrage mult atleții de forță/putere competitivi, dar dovezile care să susțină utilizarea acestor nutrienți lipsesc adesea.
2. Efectele macronutrienților asupra modificărilor concentrațiilor de testosteron
2.1. Disponibilitate redusă de energie și aport de calorii
Sportivii de competiție care se concentrează pe îmbunătățirea performanței lor atletice se străduiesc adesea să-și îmbunătățească compoziția corporală prin creșterea masei corporale slabe și scăderea masei de grăsime. În absența unei îndrumări adecvate (de exemplu, consultarea unui nutriționist sportiv), mulți sportivi își modifică aportul alimentar, creând potențial un deficit energetic, care este adesea asociat cu o disponibilitate scăzută de energie. Disponibilitatea energiei este definită ca diferența dintre aportul de energie și cheltuiala de energie, în raport cu masa fără grăsimi (FFM) a unui individ. Disponibilitatea scăzută de energie poate reduce rezervele de energie ale organismului, limitând capacitatea acestuia de a susține funcția fiziologică normală necesară pentru menținerea sănătății optime. De exemplu, un atlet care se antrenează la o intensitate mare sau o durată prelungită, în timp ce încearcă să piardă masa de grăsime prin reducerea aportului caloric, poate provoca o disponibilitate scăzută de energie. Se recomandă ca sportivii să aibă o disponibilitate energetică de >45 kcal·kg FFM·zi-1. Disponibilitatea scăzută de energie este definită ca <30 kcal·kg FFM·zi-1. Impactul disponibilității scăzute de energie asupra diferitelor sisteme fiziologice din organism nu este scopul principal al acestei lucrări, în schimb, accentul este îndreptat asupra efectului disponibilității scăzute de energie asupra concentrației circulante de testosteron și asupra biosintezei testosteronului.
Mai multe studii au demonstrat că o disponibilitate scăzută de energie poate scădea concentrațiile de LH, afectând ulterior sinteza testosteronului. Investigațiile inițiale au raportat că o disponibilitate scăzută de energie (adică 13 kcal·kg FFM·zi-1) a modificat semnificativ frecvența și amplitudinea pulsului LH. Cercetările ulterioare, care examinează o disponibilitate și mai mică de energie (adică, 10 kcal·kg FFM·zi-1) au raportat, de asemenea, scăderi semnificative ale producției de LH și ale frecvenței pulsului LH. O altă investigație, comparând participanții la studiu care se confruntă cu o disponibilitate energetică scăzută de <30 kcal·kg FFM·zi-1 cu participanții la studiu cu o disponibilitate energetică de 45 kcal·kg FFM·zi-1 a raportat o reducere semnificativă a producției de LH și a frecvenței pulsului în grupul mai mic de energie disponibil. Aceste studii indică clar efectul negativ pe care disponibilitatea energetică scăzută îl are asupra axei hipotalamo-hipofizo-gonadale.
Deficitele mari de energie par să afecteze negativ concentrațiile de testosteron. Hu și colegii săi au observat o scădere semnificativă a concentrațiilor de testosteron atunci când aportul de macronutrienți din dietă a fost redus. Alții au raportat că o reducere cu 40% a aportului caloric total a fost asociată cu scăderi semnificative ale concentrațiilor circulante de testosteron, în ciuda unui procent mare din aportul caloric provenind din surse de proteine. Situațiile de disponibilitate energetică scăzută sunt raportate atât la sportivii de anduranță, cât și la sportivii de forță/putere și sunt relevante în special în sporturile în care competiția se bazează pe clasa de greutate. O investigație care a examinat efectele restricției energetice și ale volumului de antrenament asupra concentrațiilor circulante de testosteron a raportat o reducere semnificativă a concentrațiilor de testosteron în rândul sportivilor physique care și-au crescut volumul de antrenament, în timp ce au fost restricționați de energie în comparație cu sportivii physique care și-au menținut dieta obișnuită și volumul de antrenament (descris). în tabelul 1). Cercetări suplimentare au raportat scăderi semnificative ale concentrațiilor de testosteron la alergătorii pe distanțe lungi care au fost clasificați ca „energie disponibilă scăzută” (<30 kcal·kg FFM·zi-1) în comparație cu alergătorii clasificați ca „energie disponibilă moderată” (30–45 kcal· kg FFM·zi−1) . Alții au raportat creșteri semnificative ale cortizolului, scăderi ale testosteronului și un raport testosteron/cortizol mai scăzut în 24 de ore după o sesiune de exerciții intense, care a dus la un deficit energetic de peste 400 kcal la sportivii de sex masculin. Aceste investigații au indicat că disponibilitatea scăzută a energiei are un efect dăunător asupra diferitelor sisteme fiziologice din organism, în special asupra sistemului endocrin.
Tabelul 1. Efectul disponibilității scăzute de energie și al deficitelor de energie asupra concentrațiilor circulante de testosteron.

2.2. Diete bogate în grăsimi și grăsimi dietetice
Pentru ca sistemul hormonal să funcționeze optim, grăsimea devine un macronutrient important, deoarece este coloana vertebrală pentru producția de hormoni steroizi. Recomandarea minimă pentru consumul de grăsimi din dietă nu trebuie să fie sub 25% atât pentru populația generală, cât și pentru cea sportivă. Colesterolul, o componentă a grăsimii dietetice, este unul dintre elementele de bază ale producției de testosteron. Având în vedere că dietele bogate în grăsimi (HFD) cresc nivelul de colesterol, s-a sugerat că creșterea consumului de grăsimi din dietă poate duce la o creștere a producției de testosteron.
Mai multe studii au examinat efectul HFD asupra concentrațiilor circulante de testosteron.
Un studiu a examinat efectul dietelor ketogenice (KD) și non-ketogenice (NKD) asupra forței, compoziției corporale și a profilului hormonal la bărbații antrenați pentru rezistență. Ambele grupuri de studiu au consumat o dietă bogată în grăsimi (75% față de 65% pentru KD și, respectiv, NKD). Diferența principală dintre diete a fost că grupul KD a ingerat o cantitate foarte mică de carbohidrați din dietă (5%) comparativ cu NKD (15%). Ambele grupuri au participat la un program de antrenament de rezistență de 12 săptămâni. Rezultatele au indicat că ambele grupuri au experimentat o creștere semnificativă față de valoarea inițială a concentrațiilor de testosteron total (TT) și FT în toate cele patru perioade de evaluare (săptămânile 2, 4, 6 și 8) ale studiului. În plus, concentrațiile de TT și FT în săptămânile 4, 6, 8 au fost semnificativ crescute în comparație cu săptămâna 2. Deși echipa de investigație nu a angajat un grup de control care consumă o dietă cu conținut scăzut de grăsimi (LFD), rezultatele sugerează că un HFD bogat în colesterol a crescut TT și FT la bărbații antrenați pentru rezistență, indiferent de starea de cetoză.
Un studiu similar a investigat diferențele dintre KD și dietele occidentale (WD) cu privire la compoziția corpului, forța, puterea și profilurile hormonale la bărbații antrenați pentru rezistență. În acest studiu, a fost observată o diferență mare în consumul de carbohidrați și grăsimi între cele două grupuri. Profilul de macronutrienți pentru grupul WD a fost de 20%, 55% și 25% pentru proteine, carbohidrați și respectiv, grăsimi, în timp ce pentru grupul KD a fost de 20%, 5% și respectiv 75%. Ambele grupuri au participat la un program de antrenament de rezistență de 10 săptămâni. Deși ambele grupuri au avut creșteri similare ale grosimii musculare, masei corporale slabe și măsurilor de forță (genuflexiuni 1RM și impins din decubit dorsal), doar grupul KD a experimentat o creștere semnificativă a concentrațiilor de TT. S-a sugerat că creșterile concentrațiilor de testosteron rezultate din KD sunt legate de aportul alimentar ridicat de colesterol.
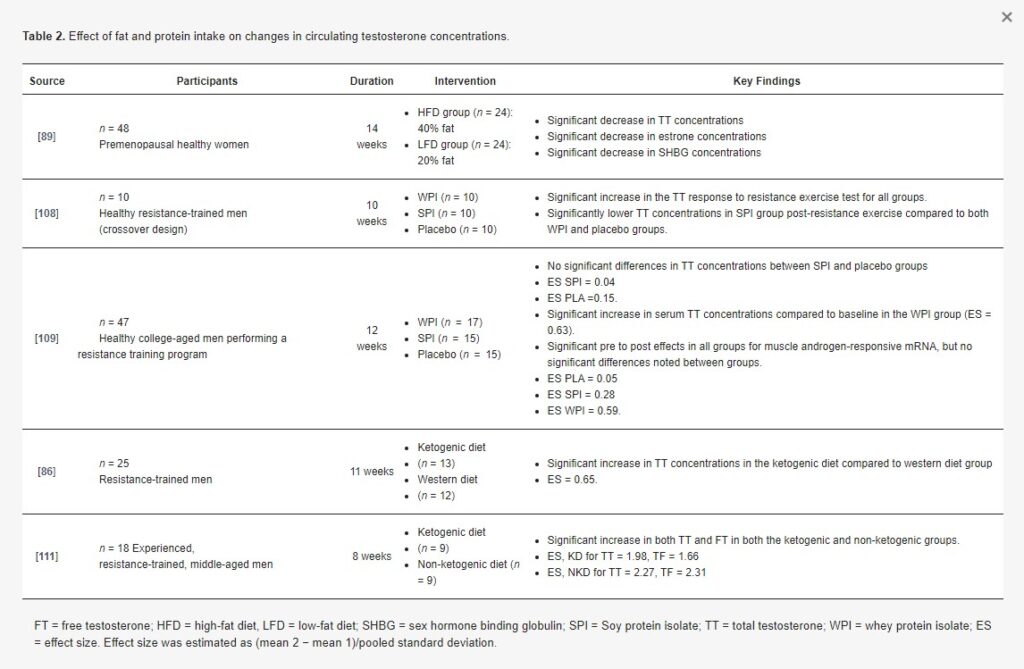
Un alt studiu care a examinat efectul nutrienților dietetici asupra concentrațiilor de testosteron la persoanele antrenate pentru rezistență a raportat o corelație semnificativă (r = 0,72) între concentrațiile de testosteron în repaus și consumul de grăsimi din dietă. O investigație la femei a raportat că o dietă care includea 40% din calorii, din grăsimi alimentare a fost superioară pentru creșterea concentrațiilor de testosteron și estrogen, comparativ cu o dietă al cărei aport total de grăsimi a fost de 20% din aportul caloric total (descris în Tabelul 2). O revizuire sistematică recentă a investigat efectul LFD asupra concentrațiilor de testosteron la bărbați. LFD a avut un efect mic până la moderat asupra scăderii concentrațiilor totale de testosteron în comparație cu HFD. Deși dovezile indică un efect pozitiv al grăsimilor alimentare asupra concentrațiilor circulante de testosteron, nu trebuie respins faptul că grăsimea nu este sursa optimă de combustibil pentru sportivii care participă la sporturi de forță/putere. Ca atare, nutriționiștii sportivi pot ezita să recomande diete bogate în grăsimi.
2.3. Proteine alimentare și suplimente proteice
Aportul alimentar de proteine are un rol important în performanța atletică. Mușchiul scheletic, locul de producere a forței, este compus în principal din proteine. Proteinele dietetice sprijină refacerea proteinelor musculare scheletice, deoarece sunt degradate sau deteriorate de exercițiile intense. Exercițiile fizice și aportul inadecvat de proteine pot duce la un răspuns catabolic al mușchilor. Adică, dacă aportul de proteine nu este ajustat pentru a satisface nevoile de proteine ale organismului, capacitatea de a menține sau de a crește masa musculară și performanța musculară devine o provocare. Pentru a menține un echilibru adecvat al proteinelor musculare, în care sinteza proteinelor musculare este egală sau depășește descompunerea proteinelor musculare, se recomandă ca aportul de proteine din dietă pentru sportivi să fie între 1,6–2,2 g·kg-1·zi-1. Deși proteina alimentară are un rol important în adaptarea dimensiunii și forței mușchilor scheletici, influența aportului de proteine din dietă asupra concentrațiilor de testosteron nu pare să aibă un rol major, iar recomandările generale de 1,6–2,2 g·kg−1·zi-1 par a fi suficiente pentru a optimiza concentrațiile de testosteron.
Un tip de proteină care a primit o atenție considerabilă în ceea ce privește efectul său asupra concentrațiilor circulante de testosteron este proteina din soia. Deși s-a demonstrat că consumul de proteine de soia are beneficii semnificative asupra performanței de forță după 12 săptămâni de antrenament de rezistență, rolul său în biologia androgenilor a făcut din acesta un subiect de interes. Acest interes este legat de înțelegerea faptului că boabele de soia conțin cantități relevante din punct de vedere biologic de izoflavone. Izoflavonele sunt denumite și fitoestrogeni și sunt compuși care se leagă de receptorii de estrogeni, provocând o cascadă de evenimente care exercită efecte asemănătoare estrogenului. Popularitatea utilizării proteinei din soia în rândul sportivilor vegani a dus la concentrarea asupra efectului acesteia asupra performanței sportive și asupra modificărilor concentrațiilor de testosteron. Studiile asupra rozătoarelor masculi au dus la rezultate contradictorii. Unele investigații au indicat că rozătoarele hrănite cu proteine din soia au prezentat concentrații mai scăzute de testosteron seric, în timp ce altele nu au raportat efecte negative asupra testosteronului circulant. O meta-analiză care examinează efectul izoflavonelor și aportului de proteine din soia asupra concentrațiilor de testosteron și SHBG la bărbați a concluzionat că nu a existat niciun efect negativ al aportului de proteine din soia asupra TT, FT sau SHBG. Cu toate acestea, cercetările ulterioare continuă să ridice problema că consumul de proteine din soia poate duce la reduceri ale concentrațiilor de testosteron în repaus și a răspunsului la exerciții fizice. Kraemer și coleg au examinat efectul suplimentării cu proteine din soia asupra răspunsului la testosteron și estradiol la bărbați sănătoși, antrenați pentru rezistență.
Folosind un design cross-over, participanții au fost randomizați în trei grupuri: supliment de proteine din zer (WPS), supliment de proteine de soia (SPS) și maltodextrină (placebo, PLA). Participanților li sa oferit fiecare tratament timp de 14 zile. După perioada de suplimentare, participanții au efectuat o sesiune de exerciții de rezistență acută constând din 6 seturi de 10 repetări în exercițiul de genuflexiuni la 80% din maximul unei repetări a participantului. Concentrațiile de testosteron și estradiol au fost examinate la diferite momente în timpul și după sesiunea de exerciții acute. Deși concentrațiile de testosteron au fost semnificativ crescute față de valoarea inițială în timpul și până la 5 minute după exercițiu, numai studiile WPS și PLA au dus la creșteri semnificative ale concentrațiilor de testosteron la măsurile de 15 și 30 de minute după exercițiu. În plus, concentrațiile de testosteron au fost semnificativ mai mici în timpul SPS în comparație atât cu WPS, cât și cu PLA în perioada post-exercițiu. Nu au fost observate diferențe semnificative în concentrația de estradiol între cele trei grupuri în niciun moment. Cercetările ulterioare, folosind aceleași trei grupuri, deși timp de 12 săptămâni și combinate cu exerciții de rezistență, nu au raportat nicio modificare semnificativă înainte sau după antrenament în concentrațiile serice de estradiol în niciunul dintre grupurile de studiu.
Deși nu au fost observate diferențe semnificative în concentrațiile de TT atât în grupul SPS, cât și în grupul PLA, a fost observată o creștere a TT seric în grupul WPS. În plus, ARNm-ul sensibil la androgeni musculari a fost crescut în toate grupurile ca urmare a stimulului de antrenament (efecte principale semnificative pentru timp), dar nu au fost observate diferențe semnificative între cele trei grupuri. Rezultatele acestor studii nu oferă nicio dovadă concludentă cu privire la proteina din soia care are un efect negativ asupra producției de testosteron. Cu toate acestea, ele sunt consecvente în a demonstra că suplimentarea cu proteine din zer poate fi suplimentul proteic superior pentru îmbunătățirea răspunsului de testosteron la antrenament. De asemenea, este important de reținut că suplimentarea cu proteine, indiferent de sursa acesteia (soia sau zer), atunci când este combinată cu antrenamentul de rezistență, poate duce la o creștere semnificativă a masei corporale slabe.
Tabelul 2. Efectul aportului de grăsimi și proteine asupra modificărilor concentrațiilor circulante de testosteron.
3. Efectele micronutrienților asupra concentrațiilor de testosteron
3.1. Vitamina D
Vitamina D este un micronutrient care acționează și ca un prohormon. Vitamina D a atras o atenție considerabilă în rândul populațiilor sportive generale și competitive, în primul rând datorită rolului său asupra diferitelor sisteme fiziologice din organism și efectului pe care deficiența de vitamina D îl are asupra multor boli. Vitamina D are două forme biologice, vitamina D3 (colecalciferol) și vitamina D2 (ergocalciferol). Vitamina D3 este cea mai biodisponibilă și cea mai suplimentată formă de vitamina D și este sintetizată în piele la expunerea la lumina soarelui. Efectele fiziologice specifice ale vitaminei D și mecanismele sale specifice depășesc scopul acestei lucrări, dar cititorii sunt încurajați să exploreze acest lucru în altă parte. Pe scurt, vitamina D, indiferent dacă este sintetizată endogen sau consumată ca aliment sau supliment, suferă hidroxilare pentru a deveni activă. Prima etapă de hidroxilare are loc în ficat, unde vitamina D este transformată în 25-hidroxivitamina D [25(OH)D]. A doua etapă de hidroxilare este efectuată în principal în rinichi pentru a forma 1,25-dihidroxivitamina D3, denumită și 1,25-dihidroxicolecalciferol, care este forma biologic activă a vitaminei D. Institutul de Medicină al Statelor Unite a indicat că intervalul pentru concentrațiile de vitamina D ar trebui să fie între 25-50 nmol·L-1. Studiile asupra sportivilor au sugerat că limita pentru deficitul de vitamina D ar trebui să fie > 30 nmol·L-1 sau chiar mai mare.
Receptorul de vitamina D, care joacă un rol central în acțiunea biologică a vitaminei, a fost observat în țesuturile de reproducere, cum ar fi ovare, prostată și testicule, precum și în sperma umană. Receptorii de vitamina D sunt prezenți pe celulele Leydig din testicule, unde are loc sinteza testosteronului din colesterol, sugerând un rol important al vitaminei D în sinteza testosteronului. Bărbații cu deficit de vitamina D au prezentat concentrații semnificativ mai mici de testosteron în comparație cu bărbații cu concentrații normale de vitamina D. S-au observat, de asemenea, asociații semnificative între concentrațiile de vitamina D și concentrațiile circulante de testosteron și SHBG, precum și indicele de androgeni liberi. Aceste constatări sunt în concordanță cu investigațiile ulterioare care raportează corelații semnificative între concentrațiile de vitamina D și testosteron.
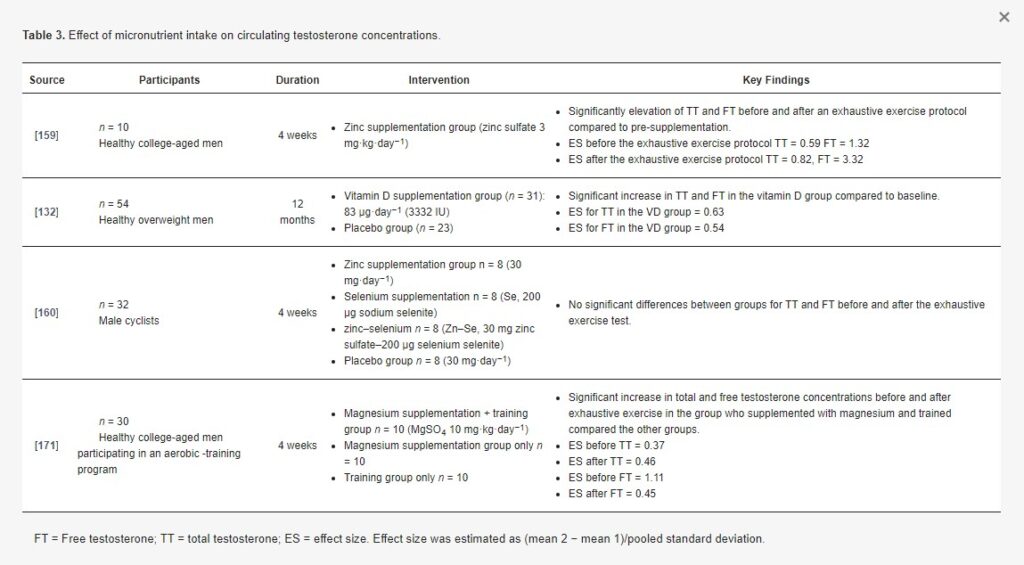
Sportivii, în general, prezintă un risc mai mare de deficiență de vitamina D, în special sportivii care participă la sporturi în interior. Suplimentarea cu vitamina D este o opțiune potențială pentru menținerea unui status normal de vitamina D, dar și pentru creșterea potențială a concentrațiilor de testosteron. Un studiu dublu-orb, randomizat-control cu placebo, cu 54 de bărbați, a raportat că grupul care a primit o suplimentare zilnică de 83 μg (3332 UI) de vitamina D timp de 12 luni a experimentat creșteri semnificative ale concentrațiilor circulante de 25-hidroxivitamina D, TT și FT în comparație cu grupul placebo (descris în Tabelul 3). Deși s-a sugerat că doza zilnică de suplimente de vitamina D pentru sportivi ar trebui să fie de 5000 UI·zi-1 pentru îmbunătățirea performanței și restabilirea nivelurilor de vitamina D, nu există un consens cu privire la intervalul optim pentru nivelurile de vitamina D. În plus, efectul suplimentelor cu vitamina D asupra modificării concentrațiilor de testosteron în repaus nu este încă bine înțeles și necesită cercetări suplimentare.
3.2. Zinc
Zincul este un mineral care influențează și interacționează cu multe sisteme biologice, în special cu sistemul endocrin. Zincul are un rol important în funcționarea sistemului imunitar și în modularea proceselor inflamatorii. În timp ce zincul poate fi găsit în multe surse de alimente, forma mai biodisponibilă de zinc poate fi găsită în țesuturile animale. Doza zilnică recomandată de zinc este între 14-40 mg·zi-1. Rolul fiziologic al zincului în biologia testosteronului este legat de necesarul său în sinteza și secreția LH. După cum sa discutat anterior, LH stimulează sinteza testosteronului în celulele Leydig. Zincul este, de asemenea, important în conversia testosteronului în DHT. DHT este convertit din testosteron de către enzima 5α-reductază din citoplasma celulei. DHT se găsește în principal în țesuturile periferice, cum ar fi prostata, pielea, foliculii de păr și ficatul. După cum sa discutat mai devreme, se crede că DHT are un efect androgenic mai puternic decât testosteronul datorită afinității sale de legare de patru ori mai mare pentru receptorul androgenic decât testosteronul și o rată de disociere de trei ori mai lentă decât testosteronul. DHT are un rol vital în dezvoltarea sexuală a bărbaților și diferențierea sexuală a organelor, promovează creșterea prostatei, chelie de tip masculin și creșterea părului corporal, facial și pubian.
Zincul are, de asemenea, un rol indirect în sinteza testosteronului. Zincul este necesar pentru funcționarea normală a enzimei de conversie a angiotensinei (ACE), o dicarboxipeptidază dependentă de zinc, care are un situs de legare a zincului în domeniul său ciclic. Se raportează că ACE crește producția de LH pituitar, influențând astfel producția de androgeni. Deficiența de zinc poate afecta sinteza testosteronului și s-a demonstrat că se corelează cu reducerile concentrațiilor de testosteron. Sportivii de competiție par să aibă un risc mai mare de deficit de zinc în comparație cu populația generală. Având în vedere că deficiența de zinc pare să fie legată de hipogonadism, eforturile de a menține nivelurile de zinc în limite normale par importante. Mai multe studii au arătat că suplimentarea cu zinc poate restabili concentrațiile de testosteron la intervalul lor fiziologic normal. Un studiu a examinat efectul suplimentelor de zinc asupra concentrațiilor de TT și FT la adulții tineri sănătoși înainte și după un protocol exhaustiv de exerciții fizice. Participanții la studiu au fost suplimentați cu sulfat de zinc (3 mg·kg·zi-1) timp de patru săptămâni. Anchetatorii au raportat că suplimentarea cu zinc a crescut atât concentrațiile de TT, cât și de FT înainte și după protocolul de exercițiu exhaustiv, în comparație cu rezultatele pre-suplimente. În schimb, alții nu au raportat nicio diferență în răspunsul TT sau FT la exercițiile fizice exhaustive între cicliștii bărbați suplimentați cu sulfat de zinc (30 mg) timp de patru săptămâni, comparativ cu un grup controlat cu placebo. Deși zincul are un rol important în reglarea producției de testosteron, nu au fost efectuate studii pe termen lung la sportivii de competiție. Nu este bine înțeles dacă suplimentarea cu zinc este eficientă numai în perioadele de deficit de zinc sau dacă poate crește concentrațiile normale de testosteron, indiferent de concentrațiile de bază.
3.3. Magneziu
Magneziul este unul dintre cele mai abundente minerale din organism. Are un rol important în diferite sisteme biologice, inclusiv sinteza proteinelor, producerea de energie celulară, creșterea celulelor și reproducerea. Din perspectiva performanței atletice, magneziul este implicat în funcția mușchilor scheletici și în producerea de energie, sugerând un posibil efect ergogenic. Doza alimentară recomandată pentru aportul de magneziu pentru bărbați este între 400 și 420 mg·zi-1 și 310-320 mg·zi-1 pentru femei. Mai multe studii au raportat că sportivii nu consumă suficient magneziu din dieta lor, ceea ce duce la un risc mai mare de deficiență de magneziu. Mai multe investigații au raportat o relație între concentrațiile de magneziu și testosteron. Un studiu a indicat că suplimentarea cu magneziu la bărbații tineri sănătoși, în combinație cu un program de antrenament de anduranță de patru săptămâni, a crescut atât concentrațiile de FT, cât și de TT în repaus și după exerciții exhaustive. Un studiu suplimentar efectuat pe aproape 400 de bărbați adulți în vârstă a raportat o corelație semnificativă între statusul de magneziu și concentrațiile de testosteron (r = 0,20, p < 0,05). Mecanismul responsabil pentru această relație nu a fost încă elucidat. Cu toate acestea, este posibil ca acesta să fie mai mult indirect decât direct. Se știe că magneziul are un rol în scăderea stresului oxidativ și a inflamației. Având în vedere că concentrațiile de testosteron pot fi puternic influențate de stresul oxidativ, este posibil ca rolul magneziului în scăderea stresului oxidativ să ofere stimulul pentru menținerea concentrațiilor de testosteron în perioadele de stres oxidativ. S-a raportat o corelație pozitivă puternică între capacitatea antioxidantă totală și concentrațiile de testosteron (r = 0,807). Magneziul are un rol important în menținerea capacității antioxidante și controlul stresului oxidativ. S-a demonstrat că deficitul de magneziu crește producția de radicali liberi de oxigen, crește deteriorarea oxidativă a țesuturilor, scade activitatea enzimelor antioxidante, scade nivelurile de antioxidanti celulari și crește producția de peroxid de oxigen. În schimb, nivelurile normale de magneziu pot preveni formarea radicalilor de oxigen prin eliminarea radicalilor liberi și inhibarea creșterilor de xantin oxidaza și nicotinamidă adenin dinucleotide fosfat (NADPH) oxidază.
Deficitul de magneziu a fost, de asemenea, asociat cu inflamația sistemică de grad scăzut și s-a demonstrat că crește citokinele proinflamatorii: factorul de necroză tumorală-alfa (TNF-α) și interleukina 1 (IL-1). S-a demonstrat că inflamația cronică de grad scăzut scade concentrațiile de testosteron prin suprimarea secreției de testosteron din celulele Leydig, rezultând atât un efect inhibitor asupra secreției de LH, cât și o sensibilitate redusă la LH la nivelul celulei Leydig. Creșterea TNF-α activează factorul nuclear κB (NF-κB), un factor de transcripție care guvernează expresia genelor de răspuns precoce implicate în răspunsurile celulare la o gamă largă de semnale. NF-kB inhibă activarea genelor enzimelor steroidogene, cum ar fi Nur77 și SF-1, care reglează steroidogeneza (biosinteza testosteronului din colesterol) în celulele Leydig. Rochelson și colegii săi au demonstrat, printr-o examinare in vitro, că sulfatul de magneziu poate reduce translocarea nucleară a NF-kB. Alții au demonstrat că suplimentarea cu magneziu poate reduce starea inflamatorie și poate scădea nivelurile de TNF-α și IL-1.
De asemenea, magneziul pare să reducă legarea testosteronului de SHBG. Majoritatea testosteronului circulant este legat de SHBG; totuși, biodisponibilitatea testosteronului este legată de concentrațiile de testosteron liber, care reprezintă doar o fracțiune din testosteronul circulant. Magneziul pare să se lege de SHBG, ceea ce duce la blocarea capacității testosteronului de a se lega de SHBG, sporind ulterior biodisponibilitatea testosteronului. Deficitul de magneziu pare să mărească legarea testosteronului de SHBG, scăzând potențial biodisponibilitatea acestuia. Nu este bine înțeles dacă suplimentarea cu magneziu este eficientă în creșterea sintezei de testosteron ca agent anabolic.
Tabelul 3. Efectul aportului de micronutrienți asupra concentrațiilor circulante de testosteron.
4. Rezumat
În rezumat, acest articol a discutat despre câțiva nutrienți despre care s-a propus să aibă activitate anti-aromataze. Deși au fost prezentate dovezi care susțin beneficiile anumitor nutrienți, dovezile care susțin majoritatea nutrienților sugerați că influențează activitatea anti-aromatazei rămân în mare parte neconcludente. O mare parte din această problemă este legată de dimensiunile mici ale eșantionului găsite în multe dintre aceste lucrări și de limitările care sunt asociate cu examinarea populațiilor antrenate și atletice. Mai mult efort pare să se fi concentrat asupra efectelor aportului de energie și asupra manipulării compoziției macronutrienților, în special compoziției proteinelor și grăsimilor, asupra modificărilor nivelurilor circulante de testosteron în repaus și ca răspuns la diferite stresuri ale exercițiilor fizice. Dovezile sunt consistente în demonstrarea faptului că aportul scăzut de energie are un impact negativ asupra concentrațiilor de testosteron care pot afecta performanța umană. În plus, anumite vitamine și minerale au roluri importante în sinteza testosteronului. Importanța suplimentării acestor vitamine și minerale pare să devină eficientă atunci când organismul devine deficitar în acești micronutrienți specifici. Cu toate acestea, lipsesc dovezi care susțin orice beneficii ale suplimentării cu acești micronutrienți pentru a crește concentrațiile de testosteron.
By. Bitanu-Alexandru
Referințe:
1. Hackett, G.; Kirby, M.; Edwards, D.; Jones, T.H.; Wylie, K.; Ossei-Gerning, N.; David, J.; Muneer, A. British Society for Sexual Medicine Guidelines on Adult Testosterone Deficiency, with Statements for UK Practice. J. Sex. Med. 2017, 14, 1504–1523.
[CrossRef]
2. Bhasin, S.; Hatfield, D.L.; Hoffman, J.R.; Kraemer,W.J.; Labotz, M.; Phillips, S.M.; Ratamess, N.A. Anabolic-Androgenic Steroid Use in Sports, Health, and Society. Med. Sci. Sports Exerc. 2021, 53, 1778–1794. [CrossRef]
3. Kraemer, W.J.; Ratamess, N.A.; Nindl, B.C. Recovery responses of testosterone, growth hormone, and IGF-1 after resistance exercise. J. Appl. Physiol. 2017, 122, 549–558. [CrossRef]
4. A Hiipakka, R.; Liao, S. Molecular Mechanism of Androgen Action. Trends Endocrinol. Metab. 1998, 9, 317–324. [CrossRef]
5. Ratnasabapathy, R.; Dhillo, W.S. The effects of kisspeptin in human reproductive function—Therapeutic implications. Curr. Drug Targets 2013, 14, 365–371. [PubMed]
6. Hoffman, J.R.; Kraemer,W.J.; Bhasin, S.; Storer, T.; Ratamess, N.A.; Haff, G.G.;Willoughby, D.S.; Rogol, A.D. Position stand on androgen and human growth hormone use. J. Strength Cond. Res. 2009, 23, S1–S59. [CrossRef] [PubMed]
7. O’Donnell, L.; Stanton, P.; de Kretser, D.M. Endocrinology of the Male Reproductive System and Spermatogenesis; Feingold, K.R.,Anawalt, B., Boyce, A., Chrousos, G., de Herder,W.W., Dhatariya, K., Dungan, K., Grossman, A., Hershman, J.M., Hofland, J.,
et al., Eds.; Endotext [Internet]; MDText.com, Inc.: South Dartmouth, MA, USA, 2000.
8. Dunn, J.F.; Nisula, B.C.; Rodbard, D. Transport of Steroid Hormones: Binding of 21 Endogenous Steroids to Both Testosterone-Binding Globulin and Corticosteroid-Binding Globulin in Human Plasma. J. Clin. Endocrinol. Metab. 1981, 53, 58–68. [CrossRef]
[PubMed]
9. Hoffman, J.R. Testosterone: A review of exercise responses and physiological effects. NSCA Journal. 1992, 14, 10–17.
10. Breiner, M.; Romalo, G.; Schweikert, H.-U. Inhibition of androgen receptor binding by natural and synthetic steroids in culturedhuman genital skin fibroblasts. J. Mol. Med. 1986, 64, 732–737. [CrossRef]
11. Kraemer,W.J.; Ratamess, N.A.; Hymer, W.C.; Nindl, B.C.; Fragala, M.S. Growth Hormone(s), Testosterone, Insulin-Like GrowtFactors, and Cortisol: Roles and Integration for Cellular Development and Growth with Exercise. Front. Endocrinol. 2020, 11, 33.
[CrossRef]
12. Bennett, N.C.; Gardiner, R.A.; Hooper, J.; Johnson, D.; Gobe, G.C. Molecular cell biology of androgen receptor signalling. Int. J.Biochem. Cell Biol. 2010, 42, 813–827. [CrossRef]
13. Hooper, D.R.; Kraemer,W.J.; Saenz, C.; Schill, K.E.; Focht, B.C.; Volek, J.S.; Maresh, C.M. The presence of symptoms of testosteronedeficiency in the exercise-hypogonadal male condition and the role of nutrition. Eur. J. Appl. Physiol. 2017, 117, 1349–1357.
[CrossRef]
14. Wrzosek, M.;Wo´zniak, J.; Włodarek, D. The causes of adverse changes of testosterone levels in men. Expert Rev. Endocrinol. Metab.2020, 15, 355–362. [CrossRef]
15. Fantus, R.J.; Halpern, J.A.; Chang, C.; Keeter, M.K.; Bennett, N.E.; Helfand, B.; Brannigan, R.E. The Association between PopularDiets and Serum Testosterone among Men in the United States. J. Urol. 2020, 203, 398–404. [CrossRef]
Nutrients 2021, 13, 3375 16 of 22
16. Baltaci, A.K.; Mogulkoc, R.; Baltaci, S.B. Review: The role of zinc in the endocrine system. Pak. J. Pharm. Sci. 2019, 32, 231–239.
[PubMed]
17. Van Kiem, P.; Dat, N.T.; Van Minh, C.; Lee, J.J.; Kim, Y.H. Lupane-triterpenes from the leaves of Brassaiopsis glomerulata. ArchPharmacal Res. 2003, 26, 594–596. [CrossRef] [PubMed]
18. Balunas, M.J.; Su, B.; Riswan, S.; Fong, H.H.; Brueggemeier, R.W.; Pezzuto, J.M.; Kinghorn, A.D. Isolation and characterization ofaromatase inhibitors from Brassaiopsis glomerulata (Araliaceae). Phytochem. Lett. 2009, 2, 29–33. [CrossRef]
19. Kowalska, M.T.; Itzhak, Y.; Puett, D. Presence of aromatase inhibitors in cycads. J. Ethnopharmacol. 1995, 47, 113–116. [CrossRef]
20. Hargrove, J.L.; Greenspan, P.; Hartle, D.K.; Dowd, C. Inhibition of Aromatase and _-Amylase by Flavonoids and Proanthocyanidinsfrom Sorghum bicolor Bran Extracts. J. Med. Food 2011, 14, 799–807. [CrossRef] [PubMed]
21. Kim, H.K.; Whang, W.K.; Kim, I.H. Constituents of the herb ofIsodon excisus var.coreanus. Arch. Pharmacal Res. 1997, 20, 291–296.[CrossRef] [PubMed]
22. Jeong, H.-J.; Chang, L.C.; Kim, H.-K.; Kim, I.-H.; Kinghorn, A.D.; Pezzuto, J.M. Aromatase inhibitors fromIsodon excisusvar.coreanus. Arch. Pharmacal Res. 2000, 23, 243–245. [CrossRef] [PubMed]
23. Lee, T.; Kim, D.; Han, J.; Kim, C. Inhibitory Effects of Scutellaria Barbata D. Don. and Euonymus Alatus Sieb. on Aromatase Activitof Human Leiomyomal Cells. Immunopharmacol. Immunotoxicol. 2004, 26, 315–327. [CrossRef] [PubMed]
24. Golan, R.; Gepner, Y.; Shai, I.Wine and Health-New Evidence. Eur. J. Clin. Nutr. 2019, 72, 55–59. [CrossRef]
25. Eng, E.T.; Ye, J.;Williams, D.; Phung, S.; Moore, R.; Young, M.K.; Gruntmanis, U.; Braunstein, G.; Chen, S. Suppression of estrogebiosynthesis by procyanidin dimers in red wine and grape seeds. Cancer Res. 2003, 63, 8516–8522.
26. Eng, E.T.;Williams, D.; Mandava, U.; Kirma, N.; Tekmal, R.R.; Chen, S. Anti-aromatase chemicals in red wine. Ann. N. Y. Acad.Sci. 2006, 963, 239–246. [CrossRef]
27. Eng, E.T.;Williams, D.; Mandava, U.; Kirma, N.; Tekmal, R.R.; Chen, S. Suppression of aromatase (estrogen synthetase) by redwine phytochemicals. Breast Cancer Res. Treat. 2001, 67, 133–146. [CrossRef]
28. Kijima, I.; Phung, S.; Hur, G.; Kwok, S.-L.; Chen, S. Grape Seed Extract Is an Aromatase Inhibitor and a Suppressor of AromataseExpression. Cancer Res. 2006, 66, 5960–5967. [CrossRef]
29. Shufelt, C.; Merz, C.N.B.; Yang, Y.; Kirschner, J.; Polk, D.; Stanczyk, F.; Paul-Labrador, M.; Braunstein, G.D. Red Versus WhiteWineas a Nutritional Aromatase Inhibitor in PremenopausalWomen: A Pilot Study. J. Women’s Health 2012, 21, 281–284. [CrossRef]
[PubMed]
30. Ren, Z.; Guo, Z.; Meydani, S.N.; Wu, D. White Button Mushroom Enhances Maturation of Bone Marrow-Derived Dendritic Cellsand Their Antigen Presenting Function in Mice. J. Nutr. 2008, 138, 544–550. [CrossRef]
31. Rop, O.; Mlcek, J.; Juríková, T. Beta-glucans in higher fungi and their health effects. Nutr. Rev. 2009, 67, 624–631. [CrossRef][PubMed]
32. Grube, B.J.; Eng, E.T.; Kao, Y.-C.; Kwon, A.; Chen, S. White button mushroom phytochemicals inhibit aromatase activity andbreast cancer cell proliferation. J. Nutr. 2001, 131, 3288–3293. [CrossRef]
33. Loing, E.; Lachance, R.; Ollier, V.; Hocquaux, M. A new strategy to modulate alopecia using a combination of two specific andunique ingredients. J. Cosmet. Sci. 2013, 64, 45–58.
34. Lipovac, M.; Chedraui, P.; Gruenhut, C.; Gocan, A.; Kurz, C.; Neuber, B.; Imhof, M. Effect of Red Clover Isoflavones over Skin,Appendages, and Mucosal Status in Postmenopausal Women. Obstet. Gynecol. Int. 2011, 2011, 1–6. [CrossRef]
35. Almstrup, K.; Fernandez, M.F.; Petersen, J.H.; Olea, N.; Skakkebaek, N.E.; Leffers, H. Dual effects of phytoestrogens result inu-shaped dose-response curves. Environ. Health Perspect. 2002, 110, 743–748. [CrossRef]
36. Balunas, M.; Su, B.; Brueggemeier, R.W.; Kinghorn, A.D. Xanthones from the Botanical Dietary Supplement Mangosteen (Garciniamangostana) with Aromatase Inhibitory Activity. J. Nat. Prod. 2008, 71, 1161–1166. [CrossRef] [PubMed]
37. Konda, M.R.; Alluri, K.V.; Janardhanan, P.K.; Trimurtulu, G.; Sengupta, K. Combined extracts of Garcinia mangostana fruit rindand Cinnamomum tamala leaf supplementation enhances muscle strength and endurance in resistance trained males. J. Int. Soc.
Sports Nutr. 2018, 15, 50. [CrossRef]
38. Sultan, C.; Terraza, A.; Devillier, C.; Carilla, E.; Briley, M.; Loire, C.; Descomps, B. Inhibition of androgen metabolism and bindingby a liposterolic extract of “serenoa repens B” in human foreskin fibroblasts. J. Steroid Biochem. 1984, 20, 515–519. [CrossRef]
39. Sudeep, H.V.; Thomas, J.V.; Shyamprasad, K. A double blind, placebo-controlled randomized comparative study on the efficacof phytosterol-enriched and conventional saw palmetto oil in mitigating benign prostate hyperplasia and androgen deficiency.
BMC Urol. 2020, 20, 1–11. [CrossRef] [PubMed]
40. Angwafor, F.; Anderson, M.L. An open label, dose response study to determine the effect of a dietary supplement on dihydrotestosteronetestosterone and estradiol levels in healthy males. J. Int. Soc. Sports Nutr. 2008, 5, 12. [CrossRef]
41. Osawa, Y.; Tochigi, B.; Tochigi, M.; Ohnishi, S.; Watanabe, Y.; Bullion, K.; Osawa, G.; Nakabayashi, Y.; Yarborough, C. AromataseInhibitors in Cigarette Smoke, Tobacco Leaves and Other Plants. J. Enzym. Inhib. 1990, 4, 187–200. [CrossRef]
42. Panche, A.N.; Diwan, A.D.; Chandra, S.R. Flavonoids: An overview. J. Nutr. Sci. 2016, 5, e47. [CrossRef]
43. Hatti, K.S.; Diwakar, L.; Rao, G.V.; Kush, A.; Reddy, G.C. Abyssinones and related flavonoids as potential steroidogenesismodulators. Bioinformation 2009, 3, 399–402. [CrossRef]
44. Bors,W.; Michel, C.; Stettmaier, K. Antioxidant effects of flavonoids. BioFactors 1997, 6, 399–402. [CrossRef]Nutrients 2021, 13, 3375 17 of 22
45. Arango, D.; Morohashi, K.; Yilmaz, A.; Kuramochi, K.; Parihar, A.; Brahimaj, B.; Grotewold, E.; Doseff, A.I. Molecular basis forthe action of a dietary flavonoid revealed by the comprehensive identification of apigenin human targets. Proc. Natl. Acad. Sci.
USA 2013, 110, E2153–E2162. [CrossRef]
46. Monteiro, R.; Becker, H.; Azevedo, I.; Calhau, C. Effect of Hop (Humulus lupulus L.) Flavonoids on Aromatase (Estrogen SynthaseActivity. J. Agric. Food Chem. 2006, 54, 2938–2943. [CrossRef]
47. Tomas-Barberán, F.A.; Cienfuegos-Jovellanos, E.; Marín, A.; Muguerza, B.; Gil-Izquierdo, A.; Cerdá, B.; Zafrilla, P.; Morillas, J.;
Mulero, J.; Ibarra, A.; et al. A New Process to Develop a Cocoa Powder with Higher Flavonoid Monomer Content and EnhancedBioavailability in Healthy Humans. J. Agric. Food Chem. 2007, 55, 3926–3935. [CrossRef] [PubMed]
48. Chou, H.-C.; Šuklje, K.; Antalick, G.; Schmidtke, L.M.; Blackman, J.W. Late-Season Shiraz Berry Dehydration That AltersComposition and Sensory Traits ofWine. J. Agric. Food Chem. 2018, 66, 7750–7757. [CrossRef] [PubMed]
49. Pacheco-Palencia, L.A.; Mertens-Talcott, S.; Talcott, S.T. Chemical composition, antioxidant properties, and thermal stability of aphytochemical enriched oil from Acai (Euterpe oleracea Mart.). J. Agric. Food Chem. 2008, 56, 4631–4636. [CrossRef] [PubMed]
50. Neves, M.A.C.; Dinis, T.C.P.; Colombo, G.; e Melo, M.L.S. Combining Computational and Biochemical Studies for a Rationale onthe Anti-Aromatase Activity of Natural Polyphenols. ChemMedChem 2007, 2, 1750–1762. [CrossRef] [PubMed]
51. Kao, Y.C.; Zhou, C.; Sherman, M.; Laughton, C.A.; Chen, S. Molecular basis of the inhibition of human aromatase (estrogesynthetase) by flavone and isoflavone phytoestrogens: A site-directed mutagenesis study. Environ. Health Perspect 1998, 106,
85–92. [CrossRef]
52. Kellis, J.; Vickery, L. Inhibition of human estrogen synthetase (aromatase) by flavones. Science 1984, 225, 1032–1034. [CrossRef]
53. Gambelunghe, C.; Rossi, R.; Sommavilla, M.; Ferranti, C.; Rossi, R.; Ciculi, C.; Gizzi, S.; Micheletti, A.; Rufini, S. Effects of Chrysinon Urinary Testosterone Levels in Human Males. J. Med. Food 2003, 6, 387–390. [CrossRef]
54. Brown, G.A.; Vukovich, M.D.; Martini, E.R.; Kohut, M.L.; Franke,W.D.; Jackson, D.A.; King, D.S. Effects of Androstenedione-Herbal Supplementation on Serum Sex Hormone Concentrations in 30- to 59-Year-old Men. Int. J. Vitam. Nutr. Res. 2001, 71,
293–301. [CrossRef]
55. Nielsen, F.H.; Hunt, C.D.; Mullen, L.M.; Hunt, J.R. Effect of dietary boron on mineral, estrogen, and testosterone metabolism inpostmenopausal women 1. FASEB J. 1987, 1, 394–397. [CrossRef] [PubMed]
56. Naghii, M.R.; Samman, S. The effect of boron supplementation on its urinary excretion and selected cardiovascular risk factors inhealthy male subjects. Biol. Trace Elem. Res. 1997, 56, 273–286. [CrossRef] [PubMed]
57. Green, N.R.; Ferrando, A.A. Plasma boron and the effects of boron supplementation in males. Environ. Health Perspect. 1994, 10(Suppl. 7), 73–77. [PubMed]
58. Naghii, M.; Samman, S. The effect of boron on plasma testosterone and plasma lipids in rats. Nutr. Res. 1997, 17, 523–531.[CrossRef]
59. Naghii, M.R.; Mofid, M.; Asgari, A.R.; Hedayati, M.; Daneshpour, M.A. Comparative effects of daily and weekly borosupplementation on plasma steroid hormones and proinflammatory cytokines. J. Trace Elem. Med. Biol. 2011, 25, 54–58. [CrossRef]
60. Rainey, C.J.; A Nyquist, L.; E Christensen, R.; Strong, P.L.; Culver, B.D.; Coughlin, J.R. Daily Boron Intake from the American Diet.J. Am. Diet. Assoc. 1999, 99, 335–340. [CrossRef]
61. Starks, M.A.; Starks, S.L.; Kingsley, M.; Purpura, M.; Jäger, R. The effects of phosphatidylserine on endocrine response to moderateintensity exercise. J. Int. Soc. Sports Nutr. 2008, 5, 11. [CrossRef]
62. Hoffman, J.R.; Stout, J.R.; Williams, D.R.; Wells, A.J.; Fragala, M.S.; Mangine, G.T.; Gonzalez, A.M.; Emerson, N.S.; McCormackW.P.; Scanlon, T.C.; et al. Efficacy of phosphatidic acid ingestion on lean body mass, muscle thickness and strength gains in
resistance-trained men. J. Int. Soc. Sports Nutr. 2012, 9, 47. [CrossRef]
63. Balasubramanian, A.; Thirumavalavan, N.; Srivatsav, A.; Yu, J.; Lipshultz, L.I.; Pastuszak, A.W. Testosterone Imposters: AnAnalysis of Popular Online Testosterone Boosting Supplements. J. Sex. Med. 2019, 16, 203–212. [CrossRef]
64. Clemesha, C.G.; Thaker, H.; Samplaski, M.K. ‘Testosterone Boosting’ Supplements Composition and Claims Are not Supportedby the Academic Literature. World J. Men’s Health 2020, 38, 115–122. [CrossRef] [PubMed]
65. Kavvoura, A.; Zaras, N.; Stasinaki, A.-N.; Arnaoutis, G.; Methenitis, S.; Terzis, G. The Importance of Lean Body Mass for the Rateof Force Development in Taekwondo Athletes and Track and Field Throwers. J. Funct. Morphol. Kinesiol. 2018, 3, 43. [CrossRef]
[PubMed]
66. Zaras, N.; Stasinaki, A.-N.; Spiliopoulou, P.; Hadjicharalambous, M.; Terzis, G. Lean Body Mass, Muscle Architecture, anPerformance in Well-Trained FemaleWeightlifters. Sports 2020, 8, 67. [CrossRef] [PubMed]
67. Sundgot-Borgen, J.; Torstveit, M.K. Aspects of disordered eating continuum in elite high-intensity sports. Scand. J. Med. Sci.Sports 2010, 20, 112–121. [CrossRef] [PubMed]
68. Wasserfurth, P.; Palmowski, J.; Hahn, A.; Krüger, K. Reasons for and Consequences of Low Energy Availability in Female anMale Athletes: Social Environment, Adaptations, and Prevention. Sports Med. Open 2020, 6, 1–14. [CrossRef]
69. Mountjoy, M.; Sundgot-Borgen, J.K.; Burke, L.M.; Ackerman, K.E.; Blauwet, C.; Constantini, N.; Lebrun, C.; Lundy, B.; Melin,A.K.; Meyer, N.L.; et al. IOC consensus statement on relative energy deficiency in sport (RED-S): 2018 update. Br. J. Sports Med.
2018, 52, 687–697. [CrossRef]
70. Melin, A.K.; Heikura, I.; Tenforde, A.; Mountjoy, M. Energy Availability in Athletics: Health, Performance, and Physique. Int. JSport Nutr. Exerc. Metab. 2019, 29, 152–164. [CrossRef]Nutrients 2021, 13, 3375 18 of 22
71. Egger, T.; Flueck, J.L. Energy Availability in Male and Female Elite Wheelchair Athletes over Seven Consecutive Training DaysNutr. 2020, 12, 3262. [CrossRef]
72. Loucks, A.B.; Heath, E.M. Dietary restriction reduces luteinizing hormone (LH) pulse frequency during waking hours andincreases LH pulse amplitude during sleep in young menstruating women. J. Clin. Endocrinol. Metab. 1994, 78, 910–915. [CrossRef]
[PubMed]
73. Loucks, A.B.; Verdun, M. Slow restoration of LH pulsatility by refeeding in energetically disrupted women. Am. J. Physiol. Integr.Comp. Physiol. 1998, 275, R1218–R1226. [CrossRef] [PubMed]
74. Loucks, A.B.; Thuma, J.R. Luteinizing Hormone Pulsatility Is Disrupted at a Threshold of Energy Availability in RegularlMenstruating Women. J. Clin. Endocrinol. Metab. 2003, 88, 297–311. [CrossRef] [PubMed]
75. Hu, T.-Y.; Chen, Y.C.; Lin, P.; Shih, C.-K.; Bai, C.-H.; Yuan, K.-C.; Lee, S.-Y.; Chang, J.-S. Testosterone-Associated Dietary PatternPredicts Low Testosterone Levels and Hypogonadism. Nutrients 2018, 10, 1786. [CrossRef]
76. Henning, P.C.; Margolis, L.M.; McClung, J.P.; Young, A.J.; Pasiakos, S.M. High protein diets do not attenuate decrements itestosterone and IGF-I during energy deficit. Metabolism 2014, 63, 628–632. [CrossRef]
77. Hooper, D.R.; Tenforde, A.S.; Hackney, A.C. Treating exercise-associated low testosterone and its related symptoms. PhysicianSportsmed. 2018, 46, 427–434. [CrossRef]
78. Mäestu, J.; Eliakim, A.; Jürimäe, J.; Valter, I.; Jürimäe, T. Anabolic and Catabolic Hormones and Energy Balance of the MalBodybuilders During the Preparation for the Competition. J. Strength Cond. Res. 2010, 24, 1074–1081. [CrossRef]
79. Heikura, I.A.; Uusitalo, A.L.T.; Stellingwerff, T.; Bergland, D.; Mero, A.A.; Burke, L.M. Low Energy Availability Is Difficult toAssess but Outcomes Have Large Impact on Bone Injury Rates in Elite Distance Athletes. Int. J. Sport Nutr. Exerc. Metab. 2018, 28,
403–411. [CrossRef]
80. Torstveit, M.K.; Fahrenholtz, I.; Stenqvist, T.B.; Sylta, Ø.; Melin, A. Within-Day Energy Deficiency and Metabolic Perturbation inMale Endurance Athletes. Int. J. Sport Nutr. Exerc. Metab. 2018, 28, 419–427. [CrossRef]
81. Lichtenstein, A.H.; Kennedy, E.; Barrier, P.; Danford, D.; Ernst, N.D.; Grundy, S.M.; Leveille, G.A.; Horn, L.; Williams, C.L.; Booth,
S.L. Dietary Fat Consumption and Health. Nutr. Rev. 2009, 56, 3–19. [CrossRef]
82. Trumbo, P.; Schlicker, S.; Yates, A.A.; Poos, M. Food and Nutrition Board of the Institute of Medicine TeNA: Dietary referencintakes for energy, carbohydrate, fiber, fat, fatty acids, cholesterol, protein and amino acids. J. Am. Diet. Assoc. 2002, 102,
1621–1630. [CrossRef]
83. Mota, J.A.; Nuckols, G.; Smith-Ryan, A.E. Nutritional Periodization: Applications for the Strength Athlete. Strength Cond. J. 2019,41, 69–78. [CrossRef]
84. Aranceta, J.; Pérez-Rodrigo, C. Recommended dietary reference intakes, nutritional goals and dietary guidelines for fat and fattyacids: A systematic review. Br. J. Nutr. 2012, 107, S8–S22. [CrossRef]
85. Whittaker, J.;Wu, K. Low-fat diets and testosterone in men: Systematic review and meta-analysis of intervention studies. J. SteroidBiochem. Mol. Biol. 2021, 210, 105878. [CrossRef] [PubMed]
86. Wilson, J.M.; Lowery, R.P.; Roberts, M.D.; Sharp, M.H.; Joy, J.M.; Shields, K.A.; Partl, J.; Volek, J.S.; D’Agostino, D. The Effects ofKetogenic Dieting on Body Composition, Strength, Power, and Hormonal Profiles in Resistance Training Males. J. Strength Cond.
Res. 2020, 34, 3463–3474. [CrossRef]
87. Volek, J.S.; Kraemer,W.J.; Bush, J.A.; Incledon, T.; Boetes, M. Testosterone and cortisol in relationship to dietary nutrients andresistance exercise. J. Appl. Physiol. 1997, 82, 49–54. [CrossRef]
88. Santos, H.O. Ketogenic diet and testosterone increase: Is the increased cholesterol intake responsible? To what extent and undewhat circumstances can there be benefits? Hormones 2017, 16, 266–270. [CrossRef]
89. Goldin, B.R.;Woods, M.N.; Spiegelman, D.L.; Longcope, C.; Morrill-LaBrode, A.; Dwyer, J.; Gualtieri, L.J.; Hertzmark, E.; Gorbach,S.L. The effect of dietary fat and fiber on serum estrogen concentrations in premenopausal women under controlled dietary
conditions. Cancer 1994, 74, 1125–1131. [CrossRef]
90. Helge, J.W. A high carbohydrate diet remains the evidence based choice for elite athletes to optimise performance. J. Physiol.2017, 595, 2775. [CrossRef] [PubMed]
91. Vigh-Larsen, J.F.; Ørtenblad, N.; Spriet, L.L.; Overgaard, K.; Mohr, M. Muscle Glycogen Metabolism and High-Intensity Exercise
Performance: A Narrative Review. Sports Med. 2021, 51, 1855–1874. [CrossRef] [PubMed]
92. Burke, L.M. Re-Examining High-Fat Diets for Sports Performance: DidWe Call the ‘Nail in the Coffin’ Too Soon? Sports Med.
2015, 45, 33–49. [CrossRef]
93. Taber, C.B.; Vigotsky, A.; Nuckols, G.; Haun, C.T. Exercise-Induced Myofibrillar Hypertrophy is a Contributory Cause of Gains iMuscle Strength. Sports Med. 2019, 49, 993–997. [CrossRef]
94. Slater, G.J.; Dieter, B.P.; Marsh, D.J.; Helms, E.R.; Shaw, G.; Iraki, J. Is an Energy Surplus Required to Maximize Skeletal MuscleHypertrophy Associated With Resistance Training. Front. Nutr. 2019, 6, 131. [CrossRef]
95. Morton, R.W.; McGlory, C.; Phillips, S.M. Nutritional interventions to augment resistance training-induced skeletal musclhypertrophy. Front. Physiol. 2015, 6, 245. [CrossRef]
96. Jäger, R.; Kerksick, C.M.; Campbell, B.I.; Cribb, P.J.; Wells, S.D.; Skwiat, T.M.; Purpura, M.; Ziegenfuss, T.N.; Ferrando, A.A.;Arent, S.M.; et al. International Society of Sports Nutrition Position Stand: Protein and exercise. J. Int. Soc. Sports Nutr. 2017, 14,
20. [CrossRef]Nutrients 2021, 13, 3375 19 of 22
97. Stokes, T.; Hector, A.J.; Morton, R.W.; McGlory, C.; Phillips, S.M. Recent Perspectives Regarding the Role of Dietary Protein forthe Promotion of Muscle Hypertrophy with Resistance Exercise Training. Nutrients 2018, 10, 180. [CrossRef]
98. 98. Morton, R.W.; Murphy, K.T.; McKellar, S.R.; Schoenfeld, B.J.; Henselmans, M.; Helms, E.; Aragon, A.A.; Devries, M.C.;Banfield, L.; Krieger, J.W.; et al. A systematic review, meta-analysis and meta-regression of the effect of protein supplementation
on resistance training-induced gains in muscle mass and strength in healthy adults. Br. J. Sports Med. 2018, 52, 376–384. [CrossRef[PubMed]
99. Candow, D.G.; Burke, N.C.; Smith-Palmer, T.; Burke, D.G. Effect of whey and soy protein supplementation combined withresistance training in young adults. Int. J. Sport Nutr. Exerc. Metab. 2006, 16, 233–244. [CrossRef] [PubMed]
100. Messina, M.; Nagata, C.; Wu, A.H. Estimated Asian Adult Soy Protein and Isoflavone Intakes. Nutr. Cancer 2006, 55, 1–12.[CrossRef] [PubMed]