Efectele suplimentelor cu L-Arginine si Vitamina C asupra performanței fizice, funcției endoteliale și oboselii persistente

O mare parte dintre supraviețuitorii COVID-19 raportează sechele clinice de lungă durată, săptămâni sau luni după debutul simptomelor: o afecțiune cunoscută sub numele de sindrom post-acut COVID-19 sau COVID lung. Long COVID cuprinde o constelație de semne și simptome respiratorii, cardiovasculare, gastrointestinale și neurologice, cum ar fi dispnee, oboseală, aritmii, arsuri la stomac și dificultăți de memorie și atenție („ceața creierului”), cu un impact substanțial asupra calității vieții. COVID-ul prelungit este, de asemenea, asociat cu funcția fizică redusă, care poate împiedica reluarea completă a activităților zilnice. Mai multe procese sunt investigate în prezent pentru implicarea lor în fiziopatologia COVID-ului îndelungat, inclusiv persistența virală, inflamația cronică, autoimunitatea, perturbarea homeostaziei metabolice, redox și disfuncția endotelială. Eterogenitatea manifestărilor clinice ale COVID-ului prelungit a împiedicat elaborarea de tratamente specifice pentru afecțiune, astfel încât gestionarea acesteia se bazează în mare parte pe tratamente simptomatice și recomandări de stil de viață sănătos.
Mai multe suplimente nutritive și alimente bioactive sunt investigate pentru a contracara COVID-ul de lungă durată. L-arginina este un regulator cheie al funcției imune, respiratorii și endoteliale. Proprietățile sale pleiotrope sunt reglate de două enzime metabolizante principale, oxid nitric (NO) sintaza și argine. Fluxul l-argininei către sinteza NO este asociat cu efecte benefice asupra sănătății imune și vasculare, în timp ce catabolismul său la ornitină de către arginază a fost asociat cu un răspuns imunitar anormal și disfuncție endotelială. Dovezile acumulate indică faptul că metabolismul l-argininei este alterat la pacienții cu COVID-19. În timpul COVID-19 acut, reglarea în creștere a activității arginazei reduce nivelurile circulante de l-arginina și schimbă metabolismul acesteia de la producția de NO pentru a induce disfuncție imună și endotelială, inflamație și tromboză, care în cele din urmă duc la ocluzie vasculară și insuficiență multiorganică. Într-adevăr, niveluri plasmatice mai scăzute de l-arginină și activitate mai mare a arginazei au fost găsite atât la pacienții cu COVID-19, cât și la copiii cu sindrom inflamator multisistem (MIS-C) în comparație cu martorii sănătoși. O scădere a nivelurilor plasmatice de l-arginine a fost, de asemenea, descrisă în COVID-19 acut și este asociată cu expansiunea celulelor supresoare derivate din mieloid și cu afectarea proliferării celulelor T, două caracteristici inflamatorii cardinale ale bolii severe.
Pe baza acestor observații, au fost propuse strategii de restabilire a nivelurilor circulante de l-arginina și de creștere a biodisponibilității NO pentru a contracara complicațiile imune, respiratorii și vasculare ale COVID-19. Vitamina C poate susține efectele benefice ale l-argininei asupra funcției endoteliale prin creșterea tetrahidrobiopterinei intracelulare, un cofactor necesar pentru oxidarea l-argininei la NO, în celulele endoteliale. In vitro, suplimentarea cu l-arginina restabileste capacitatea de proliferare a celulelor T obtinute de la pacientii cu sindrom de detresa respiratorie acuta in timpul COVID-19. În plus, s-a demonstrat că suplimentarea orală cu l-arginina reduce nevoia de suport respirator și durata spitalizării la pacienții cu COVID-19 sever. În cele din urmă, suplimentarea orală cu L-arginină plus vitamina C a redus povara simptomelor persistente și a ameliorat efortul perceput de pacienți cu COVID prelungit.
Studiile anterioare au arătat că suplimentarea cu l-arginine îmbunătățește funcția respiratorie și toleranța la efort la pacienții cu boli pulmonare și la cei cu insuficiență cardiacă congestivă, precum și la cei care primesc transplant de inimă. În plus, suplimentarea cu L-arginină poate crește performanța aerobă și anaerobă la adulții sănătoși, în special la persoanele neantrenate. Cu toate acestea, alte studii nu au găsit efecte ale suplimentelor cu l-arginine asupra performanței umane.
Pentru a explora în continuare beneficiile potențiale ale suplimentării cu L-arginina asupra rezultatelor COVID-19, am efectuat un studiu controlat randomizat single-orb pentru a evalua efectele unei suplimentari orale de 28 de zile cu L-arginina plus vitamina C asupra performanței fizice, a forței musculare, funcția endotelială, persistența oboselii și biodisponibilitatea sistemică a l-argininei la adulții cu COVID prelungit.
Materiale și Metode
Proiectarea studiului și participanții
Acesta a fost un studiu clinic randomizat, unic-orb, controlat cu placebo, care a fost efectuat la ambulatoriul post-acut COVID-19 a Fondazione Policlinico A. Gemelli IRCCS (Roma, Italia) în perioada 1 iulie 2021 – 30 aprilie. 30, 2022. Protocolul de studiu a fost aprobat de comisia de etică instituțională (nr. prot. 0013008/20). Consimțământul in format scris a fost colectat de la toți participanții înainte de înscriere. Studiul a fost realizat în conformitate cu liniile directoare ale Consiliului Internațional pentru Armonizarea cerințelor tehnice pentru produsele farmaceutice de uz uman, bunele practici clinice și cu principiile Declarației de la Helsinki. Studiul a fost înregistrat pe ClinicalTrials.gov (NCT04947488).
Participanții eligibili au fost bărbați și femei cu vârsta cuprinsă între 20 și 60 de ani care au îndeplinit următoarele criterii:
(a) infecție anterioară confirmată cu SARS-CoV-2, certificată printr-un test cu tampon molecular RT-PCR pozitiv;
(b) un test cu tampon COVID-19 negativ cu cel puțin patru săptămâni înainte de începerea operațiunilor de testare;
(c) diagnostic de lungă durată COVID, conform criteriilor Organizației Mondiale a Sănătății;
(d) oboseală persistentă, operaționalizată ca răspuns „cel mai mult sau tot timpul” la punctul șapte din Scala de depresie a Centrului pentru Studii Epidemiologice („Am simțit că tot ce am făcut a fost un efort”). Principalele criterii de excludere au fost intoleranța la oricare dintre ingredientele suplimentului (adică, l-arginina și vitamina C), condițiile și/sau terapiile care pot interfera cu rezultatele și procedurile studiului (de exemplu, sarcina sau alăptarea, boală pulmonară cronică, diabet, utilizarea antihipertensive) medicamente, steroizi sau medicamente antiinflamatoare nesteroidiene, imunosupresoare, nitrați) și implicarea în alte studii de intervenție pentru COVID de lungă durată.
Participanții eligibili au fost randomizați folosind un generator de numere aleatorii într-un raport de 1:1 pentru a primi o suplimentare orală de două ori pe zi fie cu o combinație de 1,66 g l-arginină plus 500 mg vitamina C lipozomală (Bioarginina® C, Farmaceutici Damor, Napoli, Italia ) sau un placebo timp de 28 de zile. Flacoanele care conțin suplimentul activ sau placebo au fost furnizate de Farmaceutici Damor și au fost făcute pentru a nu se distinge ca aspect.
Obiectivul principal a fost modificarea de la momentul inițial la ziua 28 a distanței parcurse la testul de mers pe jos de 6 minute. Obiectivele secundare au fost modificările de la valoarea inițială până în ziua 28 ale rezistenței și persistența oboselii până în ziua 28. Nivelurile serice de l-arginine au fost măsurate înainte de intervenție și la 28 de zile. Participanții au fost rugați să se abțină de la exerciții fizice sau să consume orice produse vasoactive (de exemplu, tutun, băuturi cu cofeină) timp de cel puțin 12 ore înainte de evaluarea performanței fizice, a forței musculare, a funcției endoteliale și a extragerii de sânge. Ultimul consum al suplimentelor a avut loc cu o seară înainte de analize. Evaluatorii rezultatelor nu au fost conștienți de alocarea grupului. Evenimentele adverse au fost înregistrate și comparate între grupurile de intervenție.
2.2. Date antropometrice și clinice
Înălțimea și greutatea corporală au fost măsurate printr-un stadiometru standard și respectiv un cântar medical analog. Indicele de masă corporală (IMC, kg/m2) a fost calculat ca raport între greutate și pătratul înălțimii. Severitatea episodului acut de COVID-19 a fost clasificată după cum urmează: (a) fără spitalizare, (b) spitalizare și (c) internare la unitatea de terapie intensivă (UTI). Timpul de la diagnosticarea COVID-19 până la includerea studiului a fost calculat pe baza auto-raportului.
2.3. Măsurarea concentrației serice de l-arginine
Au fost recoltate probe de sânge la momentul inițial și după 28 de zile de intervenție. Sângele a fost extras după postul de peste noapte folosind tuburi de colectare standard (BD Vacutainer®; Becton, Dickinson and Co., Franklin Lakes, NJ, SUA). Probele au fost lăsate la temperatura camerei timp de 30 de minute și apoi au fost centrifugate la 1000 x g timp de 10 minute la 4 ° C. Alicotele de ser au fost păstrate la -80 ° C până la analiză. Au fost colectate probe de ser de la 20 de donatori de sânge potriviți în funcție de vârstă și sex, fără dovezi ale infecției anterioare cu SARS-CoV-2 și au fost utilizate ca referință „sănătoasă”. Nivelurile serice de l-arginina au fost determinate folosind o cromatografie lichidă validată internă cu metoda spectrometriei de masă în tandem. Separarea cromatografică a fost efectuată cu un sistem ACQUITY UPLC I-Class (Waters, Milford, MA, SUA) utilizând o coloană HILIC. Detectarea analitului a fost realizată cu un triplu quadrupol Xevo-TQs Micro (Waters) echipat cu o sursă de ioni electrospray care funcționează în modul ion pozitiv. Un experiment de monitorizare a reacțiilor multiple a fost optimizat pentru detectarea și cuantificarea l-argininei.
2.4. Rezultatul primar
Principala măsură a rezultatului a fost distanța parcursă la testul de mers pe jos de 6 minute. Testul este o măsură validă și ușor de efectuat a capacității de efort la persoanele cu boală pulmonară cronică și este din ce în ce mai utilizat pentru a evalua sechelele COVID-19. Toți participanții au finalizat testul la momentul inițial și după 28 de zile de intervenție. Testul a fost efectuat pe un hol interior de 20 m lungime, cu marcaje plasate la fiecare capăt al pistei, așa cum s-a descris anterior. Distanța totală parcursă în 6 minute a fost înregistrată în metri.
2.5. Rezultate secundare
Toate măsurile de rezultat secundar au fost colectate la momentul inițial și după 28 de zile de intervenție.
Forța musculară a fost evaluată prin testarea rezistenței gripului mainii folosind un dinamometru hidraulic de mână (North Coast Medical, Inc., Morgan Hill, CA, SUA) conform protocoalelor standard internaționale, așa cum este detaliat în altă parte. Pe scurt, participantului i s-a cerut să stea pe un scaun, cu cotul lângă trunchi și îndoit la 90°, mâna în poziție neutră, cu degetul mare îndreptat în sus. Măsura a fost obținută după ce participanții au efectuat un test de familiarizare cu ambele mâini. Pentru analiză a fost utilizată cea mai mare valoare (raportată în kg) din trei încercări. Valorile forței la momentul inițial și după intervenție au fost comparate cu valorile de referință specifice vârstei și sexului.
Funcția endotelială a fost evaluată neinvaziv prin măsurarea dilatației arterei brahiale după o perioadă tranzitorie de ischemie a antebrațului (test de dilatare mediată de flux). Dilatarea mediată de flux a fost măsurată prin ultrasonografie Doppler, folosind un sistem de ultrasunete iU22 2D (Philips Electronics, Amsterdam, Olanda) conform protocoalelor standard, așa cum este descris în altă parte. Pe scurt, diametrul arterei brahiale a fost măsurat la momentul inițial și după eliberarea bruscă a unei manșete de tensiune care a oprit circulația antebrațului (prin aplicarea unei presiuni de 250 mmHg timp de 5 min). Dilatarea mediată de flux, care este mediată în principal de NO, a fost exprimată ca creșterea procentuală a diametrului arterial după eliberarea manșetei în comparație cu diametrul de bază.
Persistența oboselii a fost operaționalizată ca răspuns „cel mai mult sau tot timpul” la punctul șapte din Scala de depresie al Centrului pentru Studii Epidemiologice (CES-D, „Am simțit că tot ce am făcut a fost un efort”). Această operaționalizare a oboselii este utilizată în mod obișnuit în studiile despre fragilitatea fizică. În plus, articolul șapte din CES-D s-a dovedit a fi mai legat de oboseală decât de depresie.
2.6. Analiza Statistică
Pentru estimarea dimensiunii eșantionului, am folosit valori de referință pentru testul de mers de 6 minute la adulți sănătoși publicat de Chetta și colab. S-a estimat că un eșantion de 42 de participanți, 21 per braț de intervenție, am estimat ca oferă o putere de 80% pentru a detecta o diferență între grupuri de cel puțin 35 m la testul de mers de 6 minute, luând în considerare o abatere standard de 50 m și un nivel alfa de 5%. Ținta de recrutare a fost crescută la 50 de participanți (25 per grup) pentru a reprezenta o rată de abandon de 20%. Punctul de tăiere de 35 m a fost ales deoarece corespunde diferenței minime importante din punct de vedere clinic pentru test.
Distribuția normală a datelor a fost evaluată prin testul Shapiro-Wilk. Caracteristicile antropometrice, clinice și funcționale ale participanților la studiu au fost raportate ca mediană (interval intercuartil, IQR) pentru variabilele continue și ca valori absolute (procente) pentru variabilele categorice. Modificările față de valoarea inițială pentru variabilele continue au fost exprimate ca delta (valori la 28 de zile minus valorile de la momentul inițial), iar diferențele dintre grupurile de intervenție au fost evaluate folosind testul t Student pentru variabilele distribuite normal sau testul Mann-Whitney U pentru variabilele distorsionate. Au fost raportate diferențele medii și valorile mărimii efectului (d Cohen pentru testul t Student și corelația de rang pentru testul Mann-Whitney U). Testele Chi-pătrat sau Fisher au fost utilizate pentru a evalua diferențele dintre grupuri în ceea ce privește variabilele categorice. Analizele efectelor intervenției s-au bazat pe principiul intenției de a trata. Toate testele au fost cu două fețe, cu o semnificație statistică stabilită la p < 0,05. Toate analizele au fost efectuate folosind versiunea freeware Jamovi 2.0.0.0 (The Jamovi project, 2021; preluat de pe https://www.jamovi.org; accesat la 19 iulie 2021).
Modelele de clasificare multivariată, bazate pe analiza discriminantă a celor mai mici pătrate parțiale (PLS-DA), au fost construite și validate prin dublă validare încrucișată pentru a obține o evaluare mai cuprinzătoare a efectelor intervențiilor asupra variabilelor de interes. De asemenea, a fost evaluată influența potențială a factorilor de confuzie (adică vârsta și sexul). Analizele multivariate au fost efectuate folosind rutine interne care rulează în mediul MATLAB R2015b (The MathWorks, Natick, MA, SUA) și sunt detaliate în Materialul suplimentar.
3. Rezultate
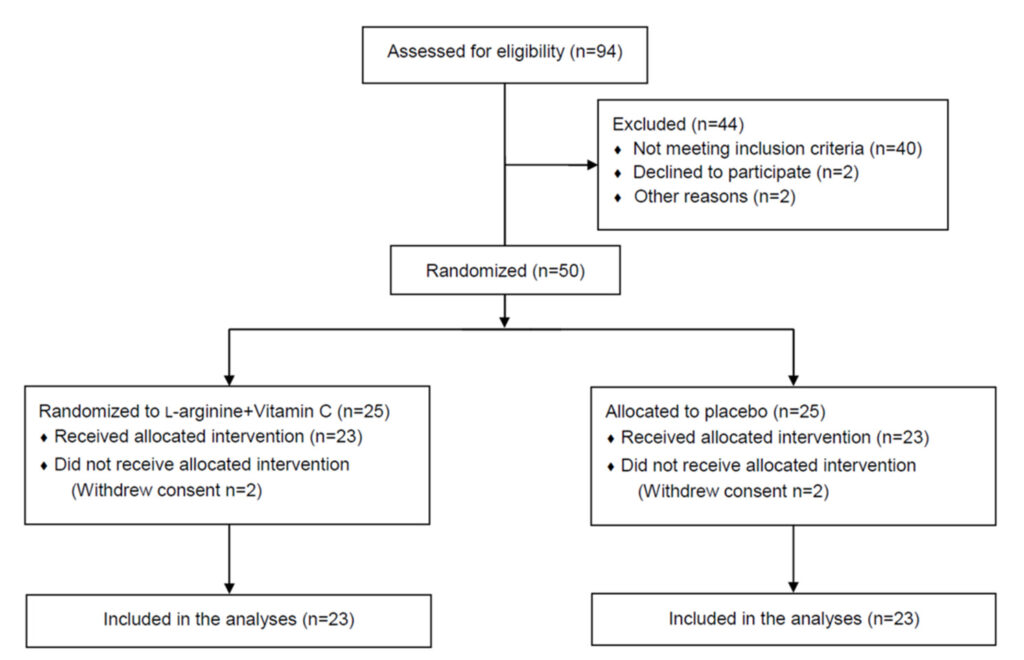
Din cei 94 de participanți candidați examinați, 50 (53,2%) au îndeplinit criteriile de includere și au fost de acord să fie randomizați pentru a primi fie intervenția L-arginină plus vitamina C (n = 25) fie placebo (n = 25). Doi participanți din fiecare grup și-au retras consimțământul înainte de a primi intervenția alocată și nu au fost incluși în analiză (Figura 1).
Caracteristicile antropometrice, clinice și funcționale ale participanților la studiu la momentul inițial au fost comparabile între grupurile de intervenție (Tabelul 1).
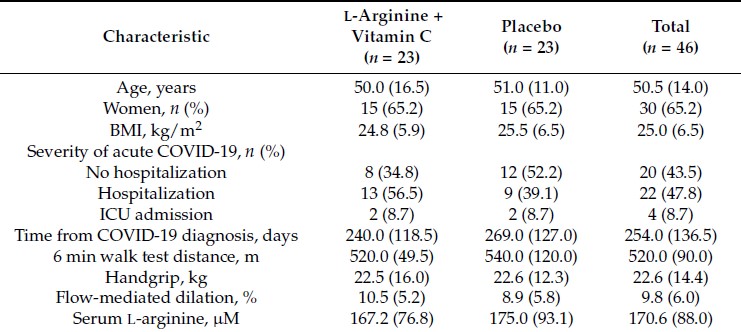
Participanții au avut o vârstă medie (IQR) de 50,5 (14,0) ani și erau predominant femei (65,2%). Aproximativ jumătate dintre participanți au avut nevoie de spitalizare în timpul episodului acut de COVID-19, iar patru (8,7%) au fost internați la UTI. Timpul mediu (IQR) care a trecut de la diagnosticarea COVID-19 până la includerea în studiu a fost de 254,0 (136,5) zile. Distanța mediană (IQR) parcursă la testul de mers pe jos de 6 minute a fost de 520 (90) m, în timp ce rezistența gripului a fost de 22,6 (14,4) kg. Dilatarea mediată de flux la momentul inițial a fost de 9,8%. Concentrația serică mediană (IQR) de l-arginină a fost de 170,6 (88,0) µM, fără diferențe între grupurile de intervenție. Cu toate acestea, valorile l-argininei serice au fost mai mici decât cele observate în eșantion fără dovezi ale infecției anterioare cu SARS-CoV-2 (mediana (IQR) 222,1 (23,1) µM; p = 0,04). La 28 de zile, concentrațiile serice de l-arginina au crescut mai mult la participanții care au primit suplimente cu L-arginina plus vitamina C (+60,2 (85,8) µM) decât în grupul placebo (+11,0 (90,8) µM; p = 0,02; diferență medie 62,4 µM, interval de încredere 95% (CI): 11,1–113,7 µM dimensiunea efectului = 0,72) (Figura 2); După 28 de zile de suplimentare cu l-arginina plus vitamina C, nivelurile serice de l-arginina din grupul activ (222,8 (88,6) µM) au fost comparabile cu cele ale controalelor fără infecție anterioară cu SARS-CoV-2 (p = 0,8).
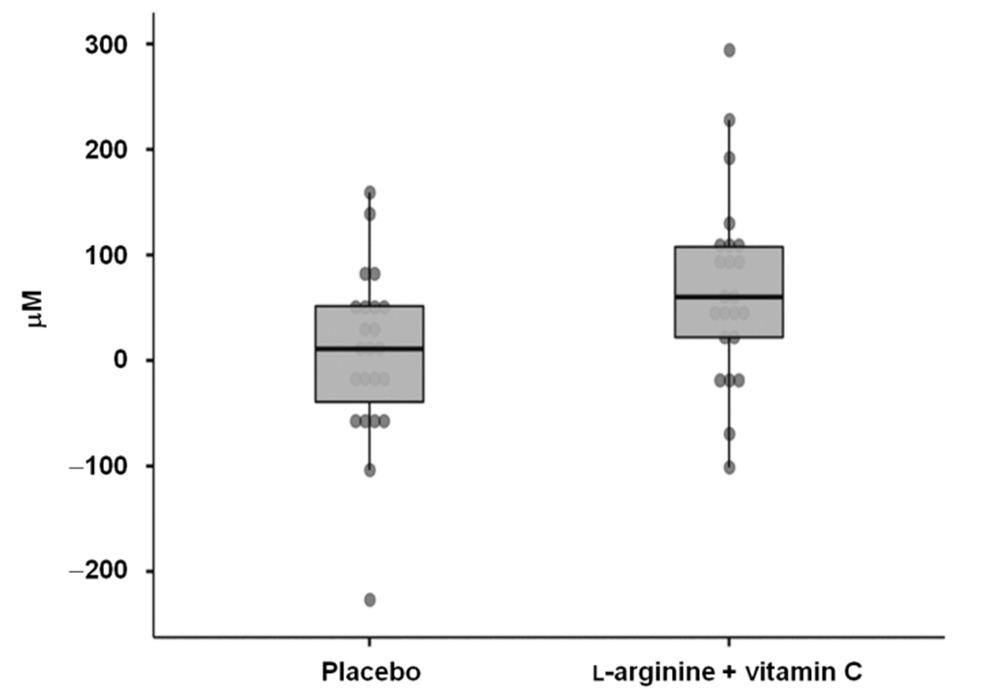
Figura 2. Modificări de la momentul inițial până la ziua 28 ale nivelurilor serice de l-arginine în cele două grupuri de intervenție.
Suplimentarea cu l-arginina plus vitamina C a fost sigura si bine tolerata si nu au fost inregistrate evenimente adverse.
Obiective de eficacitate
L-arginina plus vitamina C au crescut semnificativ distanța parcursă la testul de mers pe jos de 6 minute (modificare mediană (IQR) față de valoarea inițială: +30,0 (40,5) m) comparativ cu placebo (+0,0 (75,0) m; p = 0,001; medie diferență = 50 m, 95% CI: 20,0–80,0 m dimensiunea efectului = 0,56) (Figura 3).
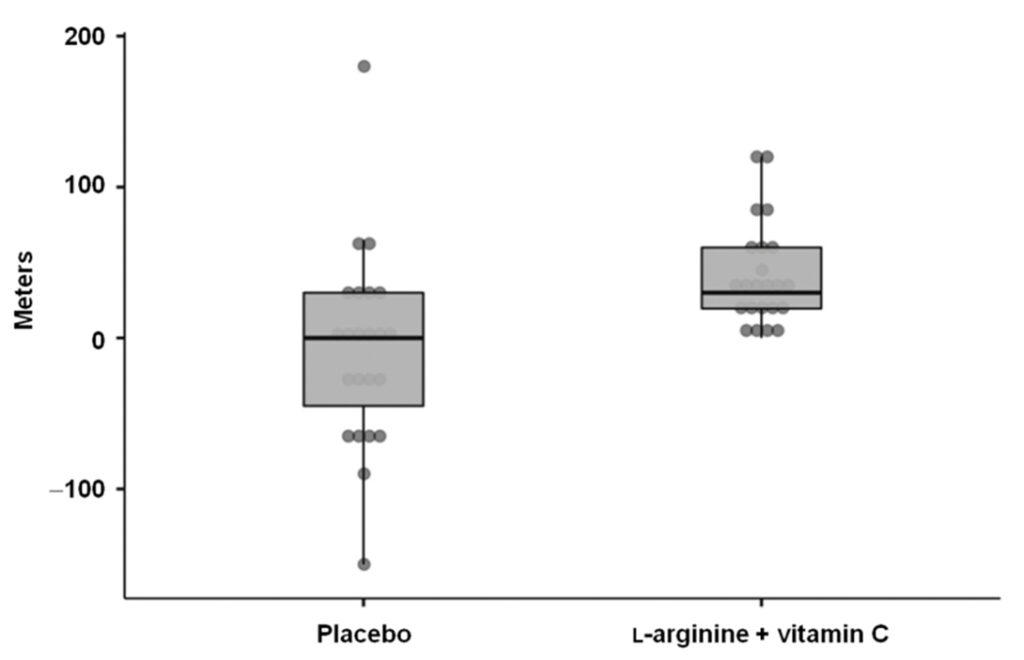
Figura 3. Modificări de la momentul inițial până la ziua 28 în distanța de test de mers pe jos de 6 minute în cele două grupuri de intervenție.
La 28 de zile, suplimentarea cu L-arginina plus vitamina C a indus imbunatatiri mai mari ale rezistentei gripului (+3,4 (7,5) kg) comparativ cu placebo (+1,0 (6,6) kg, p = 0,03; diferenta medie = 3,4 kg, 95% CI : 0,5–9,4 kg dimensiunea efectului = 0,37) (Figura 4A). La momentul inițial, aproximativ 60% dintre participanții la studiu aveau o putere a gripului sub cea de-a 25-a percentila a valorilor de referință specifice vârstei și sexului. După 28 de zile de intervenție, mai mulți participanți care au primit L-arginină plus vitamina C decât cei din grupul placebo (57% față de 30%) au fost peste primul quartil al valorilor de referință pentru rezistența gripului, deși diferența dintre grupuri nu a atins semnificația statistică (p = 0,07).
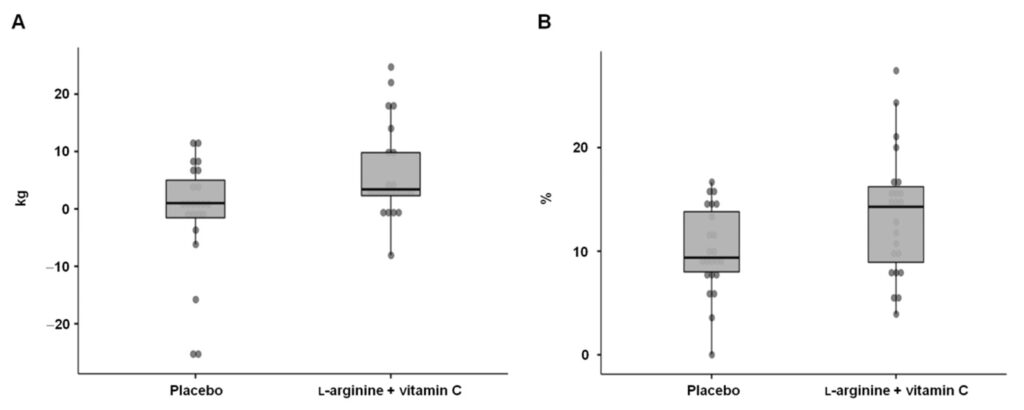
Figura 4. Modificări de la momentul inițial la ziua 28 în (A) rezistența mânerului și (B) dilatația mediată de flux în cele două grupuri de intervenție.
Dilatarea mediată de flux a fost mai mare la participanții care au primit L-arginina plus vitamina C, comparativ cu placebo (14,3% (7,3) vs. 9,4% (5,8), p = 0,03; diferența medie = 3,4%; 95% CI: 0,4– 6,5; dimensiunea efectului = 0,66) (Figura 4B).
În cele din urmă, în ziua 28, oboseala a fost raportată de doi participanți (8,7%) din grupul cu suplimente cu L-arginina plus vitamina C și 21 (80,1%) din grupul placebo (p < 0,0001).
După cum este descris în Materialul suplimentar S1, clasificarea multivariată a arătat un grad ridicat de corelație între cele patru variabile de interes (adică 6 minute distanță de mers pe jos, rezistența gripului, dilatarea mediată de flux și concentrația serică de l-arginina). Precizia medie de clasificare a participanților din cele două brațe de intervenție a fost de 77,7 ± 1,9% (p < 0,001). Clasificarea participanților nu a fost afectată de vârstă. Efectele tratamentului au fost mai evidente la femei decât la bărbați. Acest lucru se poate datora numărului scăzut de participanți de sex masculin, dintre care majoritatea au fost, totuși, clasificați corect în modelul complet.
4. Discuție
În studiul clinic, am arătat că suplimentarea cu L-arginina plus vitamina C a îmbunătățit performanța de mers, forța musculară și funcția endotelială, a redus oboseala și a restabilit concentrațiile serice de L-arginina la adulții cu COVID prelungit. Aceste descoperiri susțin opinia că creșterea biodisponibilității NO prin efectele sinergice ale l-argininei și vitaminei C ameliorează sechelele post-acute ale COVID-19.
Distanța de 6 minute de mers pe jos este o măsurătoare utilă a capacității de efort după COVID-19, deoarece se corelează cu severitatea bolii acute și cu afectarea funcției/structurii pulmonare în faza post-acută. În studiul nostru, participanții alocați în grupul cu l-arginina plus vitamina C au prezentat îmbunătățiri semnificative clinic față de valoarea inițială a distanței parcurse la testul de 6 minute în comparație cu cei care au primit un placebo. Această constatare se aliniază cu dovezile anterioare privind efectele benefice ale suplimentării cu l-arginine asupra funcției pulmonare și a capacității de efort a pacienților cu boli pulmonare cronice. O administrare orală pe termen scurt de l-arginine a scăzut semnificativ presiunea arterială pulmonară medie, rezistența vasculară, a îmbunătățit consumul maxim de oxigen și ventilația în spațiu mort la pacienții cu hipertensiune pulmonară precapilară. O suplimentare cu l-arginina de 12 săptămâni, combinată cu un program de mers pe jos, a crescut distanța de mers de 6 minute, capacitatea aerobă de vârf și calitatea vieții la pacienții stabili clinic cu hipertensiune arterială pulmonară. Mai mult decât atât, suplimentarea orală cu l-arginină a stimulat sinteza NO, a îmbunătățit funcția endotelială, a crescut toleranța la efort la pacienții cu insuficiență cardiacă congestivă și la primitorii de transplant de inimă.
O revizuire sistematică recentă și o meta-analiză asupra efectelor suplimentării cu l-arginine asupra performanței atletice au indicat că suplimentele acute sau cronice de l-arginine ar putea îmbunătăți atât performanța aerobă, cât și cea anaerobă. Pe baza acestor constatări, autorii au concluzionat că suplimentarea cu l-arginina cu 1,5-2 g pe zi de la patru la șapte săptămâni și 10-12 g pe zi timp de opt săptămâni ar putea fi recomandată pentru a îmbunătăți performanța aerobă și respectiv, anaerobă. Interesant este că persoanele neantrenate sau moderat antrenate par să obțină câștiguri mai mari în performanța la exerciții fizice după suplimentarea cu L-arginina decât cei care sunt foarte antrenați. Deși nu există dovezi concludente cu privire la efectele benefice ale suplimentelor cu L-arginina asupra performanței umane, descoperirile noastre indică faptul că o cură scurtă de Suplimentare cu L-arginina plus vitamina C poate avea un impact pozitiv asupra capacității de exercițiu a adulților cu COVID lung.
Forța gripului este un indicator valid al sănătății generale și un predictor puternic al dizabilității, morbidității și mortalității în toate etapele vieții. În timpul unui episod acut de COVID-19, puterea scăzută a gripului a fost asociată cu un risc crescut de spitalizare și cu rezultate slabe. La adulții care au supraviețuit COVID-19 sever, valorile rezistenței gripului după șase luni de la externare au fost semnificativ mai mici decât martorii sănătoși. Mai mult, la 541 de persoane care s-au recuperat de la COVID-19, valorile scăzute ale rezistenței gripului au fost asociate cu un număr mai mare de simptome persistente, inclusiv oboseală și dispnee. În studiul nostru, aproximativ 60% dintre participanți au avut o rezistență scăzută a gripului la momentul inițial. Cei care au primit L-arginina plus vitamina C au experimentat o creștere mai mare a forței gripului decât participanții din grupul placebo după 28 de zile de intervenție. În mod remarcabil, în ziua 28, mai mult de jumătate dintre participanții randomizați la l-arginina plus vitamina C aveau valori de rezistență la grip peste percentila 25 a valorilor de referință specifice vârstei și sexului, comparativ cu 30% în grupul placebo. Într-adevăr, suplimentarea cu l-arginină (fie singură, fie în combinație cu alți aminoacizi și derivați) se numără printre strategiile nutriționale propuse pentru a păstra masa musculară și funcția/forța și pentru a gestiona sarcopenia la adulții în vârstă.
Dilatarea mediată de flux este o măsură neinvazivă a funcției endoteliale și a sănătății vasculare. Studii recente au arătat că pacienții cu COVID-19 acut și supraviețuitorii convalescenți au avut valori reduse de dilatare mediată de flux, ceea ce susține rolul central al disfuncției endoteliale pe tot parcursul bolii. În prezenta investigație, suplimentarea cu L-arginina plus vitamina C a indus o dilatare mai mare mediată de flux decât placebo. Deoarece dilatarea mediată de flux este, cel puțin parțial, mediată de biodisponibilitatea NO, descoperirile noastre oferă prima dovadă că combinația de l-arginina plus vitamina C poate fi eficientă în îmbunătățirea funcției endoteliale în COVID-19 post-acut prin creșterea sintezei de NO. Acest punct de vedere este în concordanță cu rezultatele unei meta-analize a studiilor clinice randomizate care arată că suplimentarea orală pe termen scurt cu l-arginină îmbunătățește funcția endotelială atât la persoanele sănătoase, cât și la cei cu boli cardiovasculare.
Oboseala este unul dintre cele mai răspândite și împovărătoare simptome la persoanele cu COVID prelungit. De remarcat, după 28 de zile de suplimentare cu L-arginina plus vitamina C, doar doi participanți au raportat oboseală, comparativ cu 21 care au primit un placebo. Această constatare este în concordanță cu dovezile recente dintr-un studiu clinic multicentric italian amplu asupra pacienților cu COVID prelungit, care a raportat o ameliorare a oboselii și a efortului perceput după 30 de zile de suplimentare cu l-arginina plus vitamina C. Prin urmare, efectele sinergice ale l -arginina și vitamina C pe sinteza NO pot juca un rol favorabil nu numai asupra funcției endoteliale, ci și asupra reglării răspunsului imunitar, doi determinanți majori ai oboselii în sindroamele de lungă durată COVID și oboseală cronică.
Unele limitări ar trebui luate în considerare în interpretarea rezultatelor studiului. Mărimea eșantionului a fost alimentată în mod adecvat pentru rezultatul primar. Cu toate acestea, din cauza numărului mic de participanți și a naturii unui singur centru a studiului, rezultatele noastre ar trebui considerate preliminare. Studiile ulterioare cu populații mai mari, efectuate în mai multe centre și folosind metodologii diferite de studiu (de exemplu, intervenție mai lungă, proiectare încrucișată) sunt justificate pentru a confirma aceste constatări promițătoare. Nivelurile de activitate fizică, precum și obiceiurile alimentare ale participanților la studiu pot fi influențat efectele intervenției. Cu toate acestea, participanților li sa cerut să se abțină de la exerciții fizice și să limiteze ingestia de alimente bogate în arginină sau cu proprietăți vasoactive cu cel puțin 12 ore înainte de vizitele de studiu. Analizele multivariate au sugerat că efectele suplimentelor cu L-arginina plus vitamina C au fost mai evidente la femei. Cu toate acestea, studiul nu a fost alimentat pentru a evalua diferențele specifice sexului în răspunsul la tratamente. Deoarece nu a fost numit un consiliu de monitorizare a siguranței datelor, am optat pentru o abordare single-orb pentru a maximiza siguranța participanților. După cum sa menționat mai devreme, pentru a păstra integritatea procesului, toate măsurile de rezultat au fost evaluate de anchetatori care nu au fost prezenti la alocarea grupului de participanți. Deși au fost utilizate măsuri bine stabilite de performanță fizică și de forță musculară, este posibil ca teste aerobe și anaerobe mai sofisticate să ofere informații suplimentare despre efectele suplimentelor cu L-arginina plus vitamina C la adulții cu COVID prelungit. În cele din urmă, deși evaluarea nivelurilor serice de l-arginine a oferit informații relevante cu privire la eficacitatea intervenției propuse, nu putem exclude posibilitatea ca o evaluare mai cuprinzătoare a metabolismului l-argininei (de exemplu, măsurarea de compuși ai citrulinei, ornitinei și metil-argininei) pot oferi mai multe perspective asupra mecanismelor prin care sunt transmise efectele benefice ale suplimentelor cu L-arginina și vitamina C asupra rezultatelor de interes.
5. Concluzii
Suplimentarea cu l-arginina plus vitamina C a imbunatatit capacitatea de exercitiu, forta musculara, functia endoteliala si oboseala la adultii cu COVID prelungit. Prin urmare, combinația de l-arginină plus vitamina C poate fi propusă ca un remediu pentru restabilirea performanței fizice și ameliorarea simptomelor persistente la persoanele cu COVID prelungit.
Materiale suplimentare
Următoarele informații justificative pot fi descărcate de la: https://www.mdpi.com/article/10.3390/nu14234984/s1, Clasificarea multivariată prin analiza discriminantă parțială cu cele mai mici pătrate.
Contribuții ale autorului
Conceptualizare, M.T., R.C. și F.L.; metodologie, A.P., H.J.C.-J., C.D.M., J.G., E.G., L.S. (Lavinia Santucci) și B.T.; validare, A.S., L.S. (Luca Santoro), A.U. și E.M.; analiza formală, M.T., R.C., H.J.C.-J. și F.M.; ancheta, F.C., V.G., A.D.G., P.M.L., A.N. și A.M.P.; resurse, E.G., A.S., A.U. și F.L.; scris—întocmirea proiectului original, R.C.; scriere—revizuire și editare, M.T. și E.M.; supraveghere, A.U. și F.L. Toți autorii au citit și au fost de acord cu versiunea publicată a manuscrisului.
Finanțare
Această cercetare nu a primit finanțare externă.
Declarația Comisiei de revizuire instituțională
Studiul a fost realizat în conformitate cu Declarația de la Helsinki și a fost aprobat de comitetul de etică al Università Cattolica del Sacro Cuore di Roma/Fondazione Policlinico Universitario A. Gemelli IRCCS (nr. prot. 0013008/20).
Declarație de consimțământ informat
Consimțământul informat a fost obținut de la toți subiecții implicați în studiu.
Declarație de disponibilitate a datelor
Datele prezentate în acest studiu sunt disponibile de la autorul corespunzător, la cerere rezonabilă, în așteptarea aprobării de către Comitetul științific Gemelli Against COVID.
Conflicte de interese
Autorii nu declară niciun conflict de interese. Suplimentul cu L-arginina plus vitamina C si placebo au fost donate de Farmaceutici Damor, Napoli, Italia. Furnizorul nu a avut niciun rol în proiectarea studiului; în colectarea, analizele sau interpretarea datelor; în scrierea manuscrisului; sau în decizia de a publica rezultatele.
By. Bitanu-Alexandru
Referințe:
1. Nalbandian, A.; Sehgal, K.; Gupta, A.; Madhavan, M.V.; McGroder, C.; Stevens, J.S.; Cook, J.R.; Nordvig, A.S.; Shalev, D.;
Sehrawat, T.S.; et al. Post-acute COVID-19 syndrome. Nat. Med. 2021, 27, 601–615. [CrossRef] [PubMed]
2. Tosato, M.; Carfì, A.; Martis, I.; Pais, C.; Ciciarello, F.; Rota, E.; Tritto, M.; Salerno, A.; Zazzara, M.B.; Martone, A.M.; et al.
Prevalence and Predictors of Persistence of COVID-19 Symptoms in Older Adults: A Single-Center Study. J. Am. Med. Dir. Assoc. 2021, 22, 1840–1844. [CrossRef]
3. Groff, D.; Sun, A.; Ssentongo, A.E.; Ba, D.M.; Parsons, N.; Poudel, G.R.; Lekoubou, A.; Oh, J.S.; Ericson, J.E.; Ssentongo, P.; et al. Short-term and Long-term Rates of Postacute Sequelae of SARS-CoV-2 Infection: A Systematic Review. JAMA Netw. Open 2021, 4,e2128568. [CrossRef]
4. Subramanian, A.; Nirantharakumar, K.; Hughes, S.; Myles, P.; Williams, T.; Gokhale, K.M.; Taverner, T.; Chandan, J.S.; Brown, K.;Simms-Williams, N.; et al. Symptoms and risk factors for long COVID in non-hospitalized adults. Nat. Med. 2022, 28, 1706–1714.[CrossRef] [PubMed]
5. Belli, S.; Balbi, B.; Prince, I.; Cattaneo, D.; Masocco, F.; Zaccaria, S.; Bertalli, L.; Cattini, F.; Lomazzo, A.; Dal Negro, F.; et al. Lowphysical functioning and impaired performance of activities of daily life in COVID-19 patients who survived hospitalisation. Eur.Respir. J. 2020, 56, 2002096. [CrossRef] [PubMed]
6. Davis, H.E.; Assaf, G.S.; McCorkell, L.; Wei, H.; Low, R.J.; Re’em, Y.; Redfield, S.; Austin, J.P.; Akrami, A. Characterizing long
COVID in an international cohort: 7 months of symptoms and their impact. EClinicalMedicine 2021, 38, 101019. [CrossRef]
[PubMed]
7. Mehandru, S.; Merad, M. Pathological sequelae of long-haul COVID. Nat. Immunol. 2022, 23, 194–202. [CrossRef]
8. Merad, M.; Blish, C.A.; Sallusto, F.; Iwasaki, A. The immunology and immunopathology of COVID-19. Science 2022, 375,
1122–1127. [CrossRef]
9. Tosato, M.; Ciciarello, F.; Zazzara, M.B.; Pais, C.; Savera, G.; Picca, A.; Galluzzo, V.; Coelho-Júnior, H.J.; Calvani, R.; Marzetti,E.; et al. Nutraceuticals and Dietary Supplements for Older Adults with Long COVID-19. Clin. Geriatr. Med. 2022, 38, 565–591.[CrossRef]
10. Adebayo, A.; Varzideh, F.; Wilson, S.; Gambardella, J.; Eacobacci, M.; Jankauskas, S.S.; Donkor, K.; Kansakar, U.; Trimarco, V.;Mone, P.; et al. l-Arginine and COVID-19: An Update. Nutrients 2021, 13, 3951. [CrossRef]
11. Durante, W. Targeting Arginine in COVID-19-Induced Immunopathology and Vasculopathy. Metabolites 2022, 12, 240. [CrossRef][PubMed]
12. Lundberg, J.O.;Weitzberg, E. Nitric oxide signaling in health and disease. Cell 2022, 185, 2853–2878. [CrossRef]
13. Martí i Líndez, A.A.; Reith, W. Arginine-dependent immune responses. Cell. Mol. Life Sci. 2021, 78, 5303–5324. [CrossRef]
14. Pernow, J.; Jung, C. Arginase as a potential target in the treatment of cardiovascular disease: Reversal of arginine steal? Cardiovasc.Res. 2013, 98, 334–343. [CrossRef]
15. Rees, C.A.; Rostad, C.A.; Mantus, G.; Anderson, E.J.; Chahroudi, A.; Jaggi, P.;Wrammert, J.; Ochoa, J.B.; Ochoa, A.; Basu, R.K.;et al. Altered amino acid profile in patients with SARS-CoV-2 infection. Proc. Natl. Acad. Sci. USA 2021, 118, e2101708118.[CrossRef] [PubMed]
16. Sacchi, A.; Grassi, G.; Notari, S.; Gili, S.; Bordoni, V.; Tartaglia, E.; Casetti, R.; Cimini, E.; Mariotti, D.; Garotto, G.; et al. Expansionof Myeloid Derived Suppressor Cells Contributes to Platelet Activation by L-Arginine Deprivation during SARS-CoV-2 Infection.Cells 2021, 10, 2111. [CrossRef] [PubMed]
17. Reizine, F.; Lesouhaitier, M.; Gregoire, M.; Pinceaux, K.; Gacouin, A.; Maamar, A.; Painvin, B.; Camus, C.; Le Tulzo, Y.; Tattevin, P.;et al. SARS-CoV-2-Induced ARDS Associates with MDSC Expansion, Lymphocyte Dysfunction, and Arginine Shortage. J. Clin.Immunol. 2021, 41, 515–525. [CrossRef]
18. Gambardella, J.; Khondkar, W.; Morelli, M.B.; Wang, X.; Santulli, G.; Trimarco, V. Arginine and Endothelial Function. Biomedicines2020, 8, 277. [CrossRef]
19. Morelli, M.B.; Gambardella, J.; Castellanos, V.; Trimarco, V.; Santulli, G. Vitamin C and Cardiovascular Disease: An Update.Antioxidants 2020, 9, 1227. [CrossRef]
20. Fiorentino, G.; Coppola, A.; Izzo, R.; Annunziata, A.; Bernardo, M.; Lombardi, A.; Trimarco, V.; Santulli, G.; Trimarco, B. Effectsof adding L-arginine orally to standard therapy in patients with COVID-19: A randomized, double-blind, placebo-controlled,parallel-group trial. Results of the first interim analysis. EClinicalMedicine 2021, 40, 101125. [CrossRef]
21. Izzo, R.; Trimarco, V.; Mone, P.; Aloè, T.; Capra Marzani, M.; Diana, A.; Fazio, G.; Mallardo, M.; Maniscalco, M.; Marazzi, G.;et al. Combining L-Arginine with vitamin C improves long-COVID symptoms: The LINCOLN Survey. Pharmacol. Res. 2022, 183,106360. [CrossRef] [PubMed]
22. Scott, J.A.; Maarsingh, H.; Holguin, F.; Grasemann, H. Arginine Therapy for Lung Diseases. Front. Pharmacol. 2021, 12, 627503.[CrossRef] [PubMed]
23. Doutreleau, S.; Mettauer, B.; Piquard, F.; Rouyer, O.; Schaefer, A.; Lonsdorfer, J.; Geny, B. Chronic L-arginine supplementationenhances endurance exercise tolerance in heart failure patients. Int. J. Sports Med. 2006, 27, 567–572. [CrossRef] [PubMed]
24. Doutreleau, S.; Rouyer, O.; Di Marco, P.; Lonsdorfer, E.; Richard, R.; Piquard, F.; Geny, B. L-arginine supplementation improvesexercise capacity after a heart transplant. Am. J. Clin. Nutr. 2010, 91, 1261–1267. [CrossRef]
25. Viribay, A.; Burgos, J.; Fernández-Landa, J.; Seco-Calvo, J.; Mielgo-Ayuso, J. Effects of Arginine Supplementation on AthleticPerformance Based on Energy Metabolism: A Systematic Review and Meta-Analysis. Nutrients 2020, 12, 1300. [CrossRef]
26. Bescós, R.; Sureda, A.; Tur, J.A.; Pons, A. The effect of nitric-oxide-related supplements on human performance. Sports Med. 2012,42, 99–117. [CrossRef]
27. Abel, T.; Knechtle, B.; Perret, C.; Eser, P.; Von Arx, P.; Knecht, H. Influence of chronic supplementation of arginine aspartate inendurance athletes on performance and substrate metabolism a randomized, double-blind, placebo-controlled study. Int. J.Sports Med. 2005, 26, 344–349. [CrossRef]
28. Alvares, T.S.; Conte-Junior, C.A.; Silva, J.T.; Paschoalin, V.M.F. L-arginine does not improve biochemical and hormonal responsein trained runners after 4 weeks of supplementation. Nutr. Res. 2014, 34, 31–39. [CrossRef]
29. Landi, F.; Gremese, E.; Bernabei, R.; Fantoni, M.; Gasbarrini, A.; Settanni, C.R.; Benvenuto, F.; Bramato, G.; Carfì, A.; Ciciarello,F.; et al. Post-COVID-19 global health strategies: The need for an interdisciplinary approach. Aging Clin. Exp. Res. 2020, 32,1613–1620. [CrossRef]
30. A Clinical Case Definition of Post COVID-19 Condition by a Delphi Consensus, 6 October 2021. Available online: https:
//www.who.int/publications/i/item/WHO-2019-nCoV-Post_COVID-19_condition-Clinical_case_definition-2021.1 (accessed
on 8 September 2022).
31. Radloff, L.S. The CES-D Scale: A Self-Report Depression Scale for Research in the General Population. Appl. Psychol. Meas. 1977,1, 385–401. [CrossRef]
32. Santucci, L.; Lomuscio, S.; Canu, F.; Primiano, A.; Persichilli, S.; Urbani, A.; Gervasoni, J. A rapid method for determination ofunderivatized arginine-related metabolites in human plasma using LC-MS/MS. In Proceedings of the 54_ National Conference ofSocietà Italiana di Biochimica Clinica e Biologia Molecolare Clinica (SIBioC), Genoa, Italy, 5–7 October 2022; Volume 46. Availableonline: https://bc.sibioc.it/bc/numero/bcnum/206 (accessed on 18 November 2022).
33. Guyatt, G.H.; Sullivan, M.J.; Thompson, P.J.; Fallen, E.L.; Pugsley, S.O.; Taylor, D.W.; Berman, L.B. The 6-minute walk: A newmeasure of exercise capacity in patients with chronic heart failure. Can. Med. Assoc. J. 1985, 132, 919–921. [PubMed]
34. Ferioli, M.; Prediletto, I.; Bensai, S.; Betti, S.; Daniele, F.; Scioscio, V.D.; Modolon, C.; Rimondi, M.R.; Nava, S.; Fasano, L. The roleof 6MWT in Covid-19 follow up. Eur. Respir. J. 2021, 58, OA4046. [CrossRef]
35. Galluzzo, V.; Ciciarello, F.; Tosato, M.; Zazzara, M.B.; Pais, C.; Savera, G.; Calvani, R.; Picca, A.; Marzetti, E.; Landi, F. Associationbetween vitamin D status and physical performance in COVID-19 survivors: Results from the Gemelli against COVID-19post-acute care project. Mech. Ageing Dev. 2022, 205, 111684. [CrossRef] [PubMed]
36. Patrizio, E.; Calvani, R.; Marzetti, E.; Cesari, M. Physical Functional Assessment in Older Adults. J. Frailty Aging 2021, 10, 141–149.[CrossRef] [PubMed]
37. Landi, F.; Calvani, R.; Martone, A.M.; Salini, S.; Zazzara, M.B.; Candeloro, M.; Coelho-Junior, H.J.; Tosato, M.; Picca, A.; Marzetti,E. Normative values of muscle strength across ages in a “real world” population: Results from the longevity check-up 7+ project.J. Cachexia Sarcopenia Muscle 2020, 11, 1562–1569. [CrossRef]
38. Deanfield, J.; Donald, A.; Ferri, C.; Giannattasio, C.; Halcox, J.; Halligan, S.; Lerman, A.; Mancia, G.; Oliver, J.J.; Pessina, A.C.; et al.Endothelial function and dysfunction. Part I: Methodological issues for assessment in the different vascular beds: A statement bythe Working Group on Endothelin and Endothelial Factors of the European Society of Hypertension. J. Hypertens. 2005, 23, 7–17.[CrossRef]
39. Corretti, M.C.; Anderson, T.J.; Benjamin, E.J.; Celermajer, D.; Charbonneau, F.; Creager, M.A.; Deanfield, J.; Drexler, H.; Gerhard-Herman, M.; Herrington, D.; et al. Guidelines for the ultrasound assessment of endothelial-dependent flow-mediated vasodilationof the brachial artery: A report of the international brachial artery reactivity task force. J. Am. Coll. Cardiol. 2002, 39, 257–265.[CrossRef]
40. Santoro, L.; Falsetti, L.; Zaccone, V.; Nesci, A.; Tosato, M.; Giupponi, B.; Savastano, M.C.; Moroncini, G.; Gasbarrini, A.; Landi, F.;et al. Impaired Endothelial Function in Convalescent Phase of COVID-19: A 3 Month Follow Up Observational Prospective Study.J. Clin. Med. 2022, 11, 1774. [CrossRef]
41. Fried, L.P.; Tangen, C.M.;Walston, J.; Newman, A.B.; Hirsch, C.; Gottdiener, J.; Seeman, T.; Tracy, R.; Kop,W.J.; Burke, G.; et al.Frailty in older adults: Evidence for a phenotype. J. Gerontol. A Biol. Sci. Med. Sci. 2001, 56, M146–M156. [CrossRef]
42. Michielsen, H.J.; De Vries, J.; Van Heck, G.L. Psychometric qualities of a brief self-rated fatigue measure: The Fatigue AssessmentScale. J. Psychosom. Res. 2003, 54, 345–352. [CrossRef]
43. Chetta, A.; Zanini, A.; Pisi, G.; Aiello, M.; Tzani, P.; Neri, M.; Olivieri, D. Reference values for the 6-min walk test in healthysubjects 20-50 years old. Respir. Med. 2006, 100, 1573–1578. [CrossRef] [PubMed]
44. Bohannon, R.W.; Crouch, R. Minimal clinically important difference for change in 6-minute walk test distance of adults withpathology: A systematic review. J. Eval. Clin. Pract. 2017, 23, 377–381. [CrossRef] [PubMed]
45. Ståhle, L.; Wold, S. Partial least squares analysis with cross-validation for the two-class problem: A Monte Carlo study. J. Chemom.1987, 1, 185–196. [CrossRef]
46. Szyma´ nska, E.; Saccenti, E.; Smilde, A.K.; Westerhuis, J.A. Double-check: Validation of diagnostic statistics for PLS-DA models inmetabolomics studies. Metabolomics 2012, 8, 3–16. [CrossRef]
47. Huang, L.; Yao, Q.; Gu, X.; Wang, Q.; Ren, L.; Wang, Y.; Hu, P.; Guo, L.; Liu, M.; Xu, J.; et al. 1-year outcomes in hospital survivorswith COVID-19: A longitudinal cohort study. Lancet 2021, 398, 747–758. [CrossRef]
48. Nagaya, N.; Uematsu, M.; Oya, H.; Sato, N.; Sakamaki, F.; Kyotani, S.; Ueno, K.; Nakanishi, N.; Yamagishi, M.; Miyatake,
K. Short-term oral administration of L-arginine improves hemodynamics and exercise capacity in patients with precapillary
pulmonary hypertension. Am. J. Respir. Crit. Care Med. 2001, 163, 887–891. [CrossRef]
49. Brown, M.B.; Kempf, A.; Collins, C.M.; Long, G.M.; Owens, M.; Gupta, S.; Hellman, Y.; Wong, V.; Farber, M.; Lahm, T. A
prescribed walking regimen plus arginine supplementation improves function and quality of life for patients with pulmonaryarterial hypertension: A pilot study. Pulm. Circ. 2018, 8, 2045893217743966. [CrossRef]
50. Bednarz, B.; Jaxa-Chamiec, T.; Gebalska, J.; Herbaczy´nska-Cedro, K.; Ceremuzy´ nski, L.; Herbaczynska-Cedro, K.; Ceremuzynski,L. L-arginine supplementation prolongs exercise capacity in congestive heart failure. Kardiol. Pol. 2004, 60, 348–353.
51. Sayer, A.A.; Kirkwood, T.B.L. Grip strength and mortality: A biomarker of ageing? Lancet 2015, 386, 226–227. [CrossRef]
52. Gale, C.R.; Martyn, C.N.; Cooper, C.; Sayer, A.A. Grip strength, body composition, and mortality. Int. J. Epidemiol. 2007, 36,228–235. [CrossRef]
53. Rantanen, T.; Harris, T.; Leveille, S.G.; Visser, M.; Foley, D.; Masaki, K.; Guralnik, J.M. Muscle strength and body massindex aslong-term predictors of mortality in initially healthy men. J. Gerontol. A Biol. Sci. Med. Sci. 2000, 55, M168–M173. [CrossRef][PubMed]
54. Ortega, F.B.; Silventoinen, K.; Tynelius, P.; Rasmussen, F. Muscular strength in male adolescents and premature death: Cohortstudy of one million participants. BMJ 2012, 345, e7279. [CrossRef] [PubMed]
55. Cheval, B.; Sieber, S.; Maltagliati, S.; Millet, G.P.; Formánek, T.; Chalabaev, A.; Cullati, S.; Boisgontier, M.P. Muscle strength isassociated with COVID-19 hospitalization in adults 50 years of age or older. J. Cachexia Sarcopenia Muscle 2021, 12, 1136–1143.[CrossRef] [PubMed]
56. Kara, Ö.; Kara, M.; Akın, M.E.; Özçakar, L. Grip strength as a predictor of disease severity in hospitalized COVID-19 patients.Heart Lung 2021, 50, 743–747. [CrossRef]
57. Pucci, G.; D’Abbondanza, M.; Curcio, R.; Alcidi, R.; Campanella, T.; Chiatti, L.; Gandolfo, V.; Veca, V.; Casarola, G.; Leone, M.C.;et al. Handgrip strength is associated with adverse outcomes in patients hospitalized for COVID-19-associated pneumonia.Intern. Emerg. Med. 2022. Online ahead of print. [CrossRef]
58. Sirayder, U.; Inal-Ince, D.; Kepenek-Varol, B.; Acik, C. Long-Term Characteristics of Severe COVID-19: Respiratory Function,Functional Capacity, and Quality of Life. Int. J. Environ. Res. Public Health 2022, 19, 6304. [CrossRef]
59. Martone, A.M.; Tosato, M.; Ciciarello, F.; Galluzzo, V.; Zazzara, M.B.; Pais, C.; Savera, G.; Calvani, R.; Marzetti, E.; Robles, M.C.;et al. Sarcopenia as potential biological substrate of long COVID-19 syndrome: Prevalence, clinical features, and risk factors. J.Cachexia Sarcopenia Muscle 2022, 13, 1974–1982. [CrossRef]
60. Calvani, R.; Miccheli, A.; Landi, F.; Bossola, M.; Cesari, M.; Leeuwenburgh, C.; Sieber, C.C.; Bernabei, R.; Marzetti, E. Currentnutritional recommendations and novel dietary strategies to manage sarcopenia. J. Frailty Aging 2013, 2, 38–53. [CrossRef]
61. Hickson, M. Nutritional interventions in sarcopenia: A critical review. Proc. Nutr. Soc. 2015, 74, 378–386. [CrossRef]
62. Thijssen, D.H.J.; Black, M.A.; Pyke, K.E.; Padilla, J.; Atkinson, G.; Harris, R.A.; Parker, B.;Widlansky, M.E.; Tschakovsky, M.E.;Green, D.J. Assessment of flow-mediated dilation in humans: A methodological and physiological guideline. Am. J. Physiol. HeartCirc. Physiol. 2011, 300, H2–H12. [CrossRef]
63. Oikonomou, E.; Souvaliotis, N.; Lampsas, S.; Siasos, G.; Poulakou, G.; Theofilis, P.; Papaioannou, T.G.; Haidich, A.B.; Tsaousi,G.; Ntousopoulos, V.; et al. Endothelial dysfunction in acute and long standing COVID-19: A prospective cohort study. Vascul.Pharmacol. 2022, 144, 106975. [CrossRef] [PubMed]
64. Gao, Y.P.; Zhou, W.; Huang, P.N.; Liu, H.Y.; Bi, X.J.; Zhu, Y.; Sun, J.; Tang, Q.Y.; Li, L.; Zhang, J.; et al. Persistent EndothelialDysfunction in Coronavirus Disease-2019 Survivors Late After Recovery. Front. Med. 2022, 9, 809033. [CrossRef]
65. Sardu, C.; Gambardella, J.; Morelli, M.B.; Wang, X.; Marfella, R.; Santulli, G. Hypertension, Thrombosis, Kidney Failure, andDiabetes: Is COVID-19 an Endothelial Disease? A Comprehensive Evaluation of Clinical and Basic Evidence. J. Clin. Med. 2020, 9,1417. [CrossRef] [PubMed]
66. Green, D.J.; Dawson, E.A.; Groenewoud, H.M.M.; Jones, H.; Thijssen, D.H.J. Is flow-mediated dilation nitric oxide mediated?: Ameta-analysis. Hypertension 2014, 63, 376–382. [CrossRef] [PubMed]
67. Bai, Y.; Sun, L.; Yang, T.; Sun, K.; Chen, J.; Hui, R. Increase in fasting vascular endothelial function after short-term oral L-arginineis effective when baseline flow-mediated dilation is low: A meta-analysis of randomized controlled trials. Am. J. Clin. Nutr. 2009,89, 77–84. [CrossRef]
68. Carfì, A.; Bernabei, R.; Landi, F. Persistent Symptoms in Patients After Acute COVID-19. JAMA 2020, 324, 603–605. [CrossRef]
69. Komaroff, A.L. Inflammation correlates with symptoms in chronic fatigue syndrome. Proc. Natl. Acad. Sci. USA 2017, 114,8914–8916. [CrossRef]
70. Haffke, M.; Freitag, H.; Rudolf, G.; Seifert, M.; Doehner,W.; Scherbakov, N.; Hanitsch, L.;Wittke, K.; Bauer, S.; Konietschke, F.;et al. Endothelial dysfunction and altered endothelial biomarkers in patients with post-COVID-19 syndrome and chronic fatiguesyndrome (ME/CFS). J. Transl. Med. 2022, 20, 138. [CrossRef]
71. Zazzara, M.B.; Bellieni, A.; Calvani, R.; Coelho-Junior, H.J.; Picca, A.; Marzetti, E. Inflammaging at the Time of COVID-19. Clin.Geriatr. Med. 2022, 38, 473–481. [CrossRef]