Magneziul și semnele distinctive ale îmbătrânirii

Unul dintre cele mai remarcabile fenomene ale ultimelor timpuri este îmbătrânirea continuă a populației, care este prezentă în ultimul secol și jumătate cu consecințe în toate aspectele societății. Se preconizează că această tendință va continua, cu o creștere de 4,4 ani în medie până în 2040 în 195 de țări. Îmbătrânirea este însoțită frecvent de o pierdere progresivă a integrității fiziologice, ceea ce face persoana mai susceptibilă la boli cronice și dizabilități asociate, umbrind această realizare a umanității.
Magneziul este un mineral fundamental, indispensabil pentru numeroase procese celulare, inclusiv toate procesele de fosforilare oxidativă, peste 600 de reacții enzimatice, generarea de energie, sinteza și stabilitatea acizilor nucleici, sinteza proteinelor și metabolismul carbohidraților. Un status adecvat de magneziu este esențial pentru organele și sistemele corpului uman. Deficiența de magneziu este frecventă la sfârșitul vieții și a fost asociată cu diferite boli cronice legate de vârstă.
În 2013, Lopez-Otin și colab. au propus nouă semne distinctive ale îmbătrânirii, cuprinzând instabilitatea genomică, uzura telomerilor, modificări epigenetice, disfuncția mitocondrială, pierderea proteostazei, dereglarea sensibilității nutritive, senescența celulară, epuizarea celulelor stem și comunicarea intercelulară alterată. Cercetările privind biologia îmbătrânirii au progresat în mod semnificativ pe baza acestei propuneri. Într-adevăr, noi semne distinctive ale îmbătrânirii au fost adăugate celor originale, inclusiv autofagia, tulburarea microbiomului și inflamația, printre altele emergente. Progresele în înțelegerea mecanismelor care stau la baza procesului de îmbătrânire și a posibililor determinanți modificabili pot dezvălui perspective asupra modului de a obține cea mai sănătoasă îmbătrânire posibilă.
Prezenta revizuire narativă își propune să ofere o privire de ansamblu asupra legăturilor dintre magneziu și semnele distinctive ale îmbătrânirii ca căi care ne ajută să explicăm efectele magneziului asupra procesului de îmbătrânire și a bolilor cronice legate de vârstă.
Homeostazia magneziului celular
Magneziul, un element de relevanță fiziologică cardinală, este cel mai abundent cation celular divalent din celulele vii, al doilea cel mai abundent cation intracelular din corpul uman după potasiu și al patrulea cel mai frecvent mineral în întregul corp după calciu, sodiu și potasiu. Magneziul este un cofactor indispensabil pentru acțiunile structurale și catalitice ale numeroaselor reacții enzimatice, acționând și asupra substraturilor acestora; este necesar pentru toate reacțiile de fosforilare oxidative, producerea de energie, sinteza proteinelor, sinteza și stabilitatea acidului nucleic și glicoliză. Magneziul este esențial pentru transportul activ al altor ioni prin membranele celulare; modulează contracția musculară, ritmul cardiac normal și excitabilitatea neuronilor. Magneziul este implicat în sinteza mitocondrială a adenozin trifosfat (ATP) pentru a forma MgATP, care este necesar pentru reacții celulare cruciale și semnalizare, inclusiv toate reacțiile de fosforilare a proteinelor și activarea ciclică a adenozin monofosfatului (cAMP), care este implicată în numeroase procese celulare biochimice, cuprinzând expresia acidului ribonucleic (ARN), sinteza acidului dezoxiribonucleic (ADN), metabolismul glucozei, semnalizarea celulelor musculare și neuronale și controlul tensiunii arteriale. Figura 1 prezintă caracteristicile chimice ale magneziului și relația sa strânsă cu ATP.
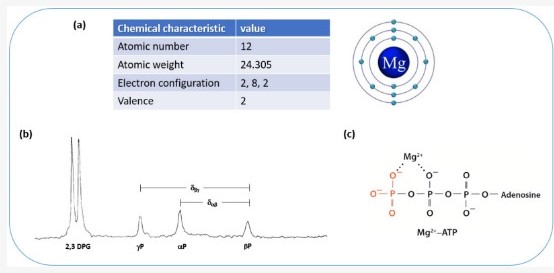
Figura 1. Structura chimică a ionului de magneziu și a MgATP. (a) Caracteristicile chimice ale magneziului; (b) spectrul RMN 31P cu transformată Fourier al ATP demonstrează rezonanțe bine definite ale grupelor α, β și γ-fosforil ale ATP. Deplasările lor chimice depind de starea de formare a complexului ATP cu ionul de magneziu, permițând estimarea magneziului liber; (c) schema relației strânse a ATP cu ionul de magneziu.
Magneziul este un ion predominant intracelular (98%). Nivelurile serice (2% din total) sunt menținute într-o limită îngustă în condiții sănătoase datorită unui echilibru dinamic între aportul alimentar de magneziu, absorbția și excreția intestinală, excreția renală, depozitarea osoasă și cerințele diferitelor țesuturi ale corpului (Figura 2) .
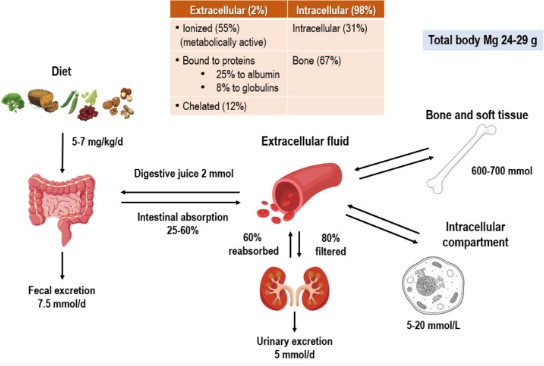
Figura 2. Distribuția magneziului în organism.
Biologia îmbătrânirii
Îmbătrânirea este atât universală, cât și inevitabilă. În timpul îmbătrânirii, apar modificări la nivel biologic, psihologic și fiziologic. Unele dintre aceste modificări sunt benigne, cum ar fi părul gri. Altele au ca rezultat scăderea funcției simțurilor și activităților vieții de zi cu zi și o susceptibilitate crescută la boli, fragilitate și dizabilități. De fapt, înaintarea în vârstă este factorul de risc major pentru numeroase boli cronice.
Populația în vârstă de peste 60 de ani este în prezent grupa de vârstă cu cea mai rapidă creștere, ceea ce subliniază importanța studiilor privind procesul de îmbătrânire și promovarea unor stiluri de viață care maximizează nu numai longevitatea, ci, în primul rând, calitatea vieții în timpul îmbătrânirii. În ciuda declinului funcțional progresiv asociat în vârstă, mulți adulți în vârstă rămân activi fizic și cu funcțiile cognitive păstrate. Chiar dacă acești oameni sunt în general considerați a avea un fundal genetic favorabil, dovezile acumulate indică un stil de viață sănătos pe tot parcursul vieții ca fiind cheia pentru îmbătrânirea de succes.
Scăderea dependentă de vârstă a integrității fiziologice și a funcției diferitelor sisteme de organe pare a fi cauzată de acumularea de leziuni celulare care duce la o pierdere progresivă a funcției biologice. Îmbătrânirea apare ca urmare a unei serii de procese intrinseci și a interacțiunilor acestora cu mediul extern (de exemplu, lumina ultravioletă a soarelui, poluanții atmosferici și radiațiile, substanțele chimice din apă, exercițiile fizice, calitatea dietei). Cercetarea îmbătrânirii a devenit un domeniu extins de studiu. Acest lucru s-a reunit în descrierea semnelor distinctive ale îmbătrânirii, căreia îi sunt dedicați un număr mare de cercetători din întreaga lume și pe care le vom discuta în detaliu mai jos. Studiile privind biologia îmbătrânirii în modele experimentale și în populațiile umane au condus la apariția unor teorii care să explice îmbătrânirea. Procesul de îmbătrânire este atât de complex încât nu există un singur determinant care să-l explice pe deplin. Cu toate acestea, aceste studii au arătat că rata de îmbătrânire poate fi încetinită, sugerând că țintirea mecanismelor de îmbătrânire poate ajuta la reducerea incidenței și povara a numeroase boli și la creșterea duratei de sănătate (porțiunea din viață petrecută în stare bună de sănătate).
Magneziul și îmbătrânirea
Deficiența cronică de magneziu este frecventă la adulții în vârstă, ceea ce poate fi explicat din diverse motive, inclusiv un conținut scăzut de magneziu din alimentație (obișnuit în dietele occidentale), excreția urinară crescută sau absorbția intestinală redusă din cauza mai multor afecțiuni patologice și iatrogenice. Tabelul 1 și Tabelul 2 prezintă principalele cauze ale hipomagnezemiei.
Tabelul 1. Principalele cauze patologice ale hipomagnezemiei.

Tabelul 2. Principalele cauze iatrogene ale hipomagnezemiei.

Mai mult, s-a observat un nivel scăzut de magneziu intracelular la adulții în vârstă chiar și în absența magneziului seric total modificat. Acest lucru a fost raportat și la adulții mai tineri. Deficitele ușoare de magneziu sunt de obicei asimptomatice și atunci când sunt evidente, semnele clinice sunt de obicei absente sau nespecifice și pot fi confundate cu simptomele comune asociate cu îmbătrânirea. Tabelul 3 prezintă simptomele și semnele hipomagnezemiei.
Tabelul 3. Simptome și semne de hipomagnezemie.

Frecvența ridicată a deficitului cronic latent de magneziu la populațiile în vârstă și asocierea acestuia cu mai multe boli, medicamente și proceduri chirurgicale (Tabelul 1 și Tabelul 2) evidențiază necesitatea recomandării unei diete bogate în alimente care conțin magneziu pentru a ajuta la atenuarea deficienței de magneziu și consecințele sale clinice. Figura 3 prezintă sursele alimentare de magneziu și factorii care cresc sau scad biodisponibilitatea acestuia.
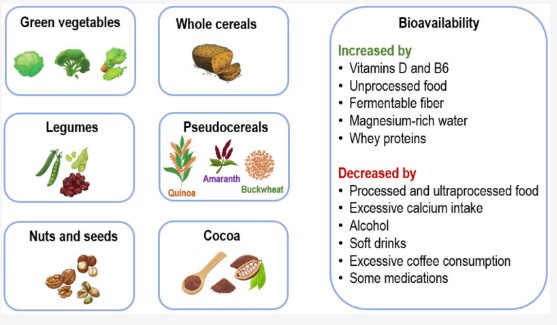
Figura 3. Principalele surse alimentare de magneziu și factori care cresc sau scad biodisponibilitatea acestuia.
Conexiunile de magneziului cu semnele distinctive ale îmbătrânirii
La cele nouă semne distinctive ale îmbătrânirii propuse inițial în 2013 s-au adăugat și altele, inclusiv autofagia dezactivată, tulburarea microbiomului și inflamația. Fiecare dintre aceste semne distinctive satisface următoarele criterii:
(1) apare în timpul îmbătrânirii normale;
(2) exacerbarea sa experimentală accelerează îmbătrânirea;
(3) ameliorarea sa experimentală încetinește îmbătrânirea și în consecință, crește durata de viață. Traiectoria de îmbătrânire este flexibilă și poate fi modulată de factori dietetici, inclusiv de magneziu, și de alți factori determinanți ai stilului de viață. Magneziul este implicat în mai multe procese celulare (Figura 4).
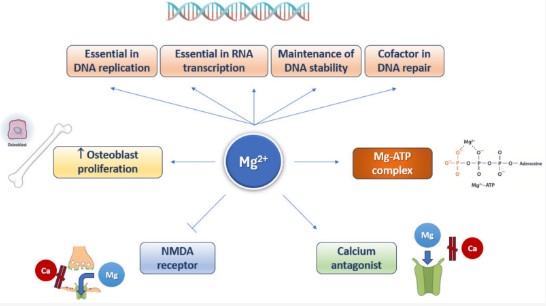
Figura 4. Implicarea magneziului în mai multe procese celulare.
În următoarele subsecțiuni, ne vom concentra asupra diferitelor semne distinctive ale îmbătrânirii, care au fost strâns legate de magneziu (Figura 5).
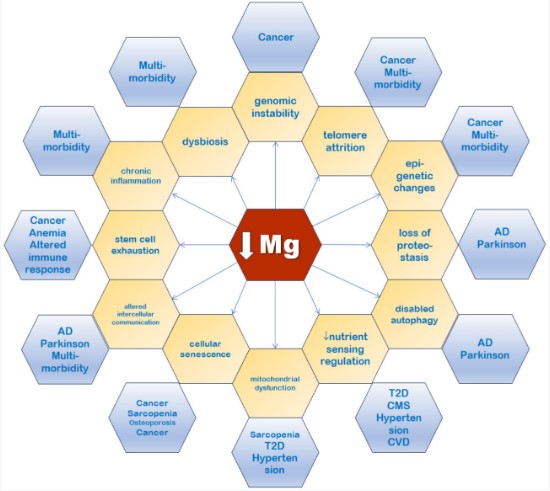
Figura 5. Statutul scăzut de magneziu este asociat cu toate semnele distinctive ale îmbătrânirii (galben). Exemple de boli legate de vârstă legate de semnele distinctive ale îmbătrânirii sunt prezentate cu albastru. AD: boala Alzheimer; CMS: sindrom cardiometabolic; BCV: boli cardiovasculare; și T2D: diabet de tip 2.
Instabilitatea genomică
Instabilitatea genomică se referă la o predispoziție crescută la modificări genomice (de exemplu, deteriorarea ADN-ului, mutații și anomalii cromozomiale) și este generată de efectele modificărilor epigenetice, stresului oxidativ, repararea deficitară a ADN-ului și întreținerea telomerilor. ADN-ul codifică o serie de procese care detectează și repară practic toate aceste forme de daune; cu toate acestea, mecanismele de reparare a ADN-ului devin mai puțin eficiente în timpul îmbătrânirii, favorizând acumularea de mutații genetice, care sunt transferate în fiecare copie viitoare a unei celule. Cancerul este unul dintre rezultatele leziunilor ADN-ului nereparate sau ale reparării incorecte. Mutațiile ADN apar pe tot parcursul vieții; cu cât durata de viață este mai lungă, cu atât este mai probabil să apară. Instabilitatea genomică este, fără îndoială, un factor principal al îmbătrânirii, care afectează în cele din urmă producția de proteine funcționale esențiale necesare reacțiilor celulare biochimice, comunicarea dintre celulă si alta celulă și întreținerea structurii.
Atât șanțurile ADN minore, cât și cele majore au locuri de legare specifice pentru magneziu. Cu aproape cincizeci de ani în urmă, magneziul s-a dovedit a fi esențial pentru fidelitatea replicării ADN-ului în ADN polimerază. Magneziul contribuie la stabilizarea ansamblului cromatinei pe tot parcursul ciclului celular, este implicat în structura secundară și terțiară a ADN-ului și stabilizează conformația ADN-ului prin legături de hidrogen sau forță electrostatică. Fragmentele de ADN se agrează puternic pe sticla tratată cu magneziu într-o manieră dependentă de concentrație. Astfel, menținerea magneziului intracelular la nivel fiziologic este un determinant important al stabilității ADN-ului. În schimb, concentrațiile inadecvate de magneziu slăbesc stabilitatea ADN-ului prin inducerea de deteriorare și stres oxidativ asupra structurii dublu catenare. Magneziul este necesar pentru activarea diferitelor enzime implicate în căile de reparare a ADN-ului, cum ar fi repararea exciziei bazei, repararea exciziei nucleotidelor și repararea nepotrivirii, demonstrând rolul său crucial în păstrarea stabilității genomului.
Uzura telomerilor
Telomerii sunt secțiuni de secvențe de nucleotide repetitive (TTAGGG la om) care conțin informații neesențiale, situate la ambele capete ale fiecărui cromozom și care protejează împotriva degradării și fuziunii sale cu alți cromozomi. Acest lucru asigură că nu se pierde nicio informație genetică și controlează numărul de replicări celulare. O mică fracțiune de ADN telomeric (50-100 de perechi de baze în fibroblastele umane) se pierde în fiecare diviziune celulară din cauza problemei de replicare finală, ceea ce face ca telomerii să se scurteze treptat pe măsură ce înaintează în vârstă. Când telomerii ating o lungime extrem de scurtă, celulele o recunosc și își opresc mașinile de replicare, devenind senescente, ceea ce are loc după aproximativ 50 de diviziuni în majoritatea celulelor umane. Această limită ajută la prevenirea cancerului (limitează capacitatea de proliferare celulară), spre deosebire de replicarea necontrolată a celulelor canceroase. Telomeraza, care este oprită în majoritatea celulelor adulte, poate preveni scurtarea telomerilor și chiar poate restabili lungimea telomerilor. Telomerii pot suferi o scurtare din cauza stresului oxidativ, iar telomerii mai scurti au fost asociați cu risc crescut de cancer, boli cardiovasculare și mortalitate, în special la vârste mai mici. Fumatul, un factor de risc cardinal pentru boli cardiovasculare, cancer și mortalitate, accelerează uzura telomerilor. Dimpotrivă, unele studii, dar nu toate, au descoperit că activitatea fizică protejează împotriva uzurii telomerilor.
Magneziul influențează structura și integritatea cromatinei telomerice. Peste cincizeci la sută din telomeri se află în lamele nucleare, iar proteinele lor de legare la laminină depind de concentrațiile de magneziu. Magneziul este, de asemenea, implicat în reglarea telomerazei. Componenta catalitică a telomerazei este transcriptaza inversă a telomerazei (TERT); TERT își exercită efectele biologice prin interacțiunea cu ținta căii rapamicinei (mTOR), care este modulată de concentrația de magneziu. Magneziul protejează împotriva potențialului de regenerare musculară în declin legat de vârstă și a pierderii masei musculare prin activarea semnalizării mTOR. Mai mult, fluctuațiile circadiene mTOR sunt reglate de oscilațiile magneziului într-o manieră sensibilă la MgATP. Expresia (m)ARN-ului mesager TERT este modificată de ritmurile circadiene modificate care accelerează procesul de îmbătrânire, în timp ce fluctuațiile magneziului modulează ceasul celular.
Alterări epigenetice
Epigenetica se referă la modificări ale expresiei genomului fără modificarea secvenței ADN care modulează funcțiile celulare și tisulare. Fiecare celulă conține aceeași secvență de ADN, dar adăugarea de mărci epigenetice activează și oprește expresia anumitor gene, după cum o cere situația. Epigenomul poate fi modificat prin dietă, alți factori de stil de viață și produse farmaceutice. Mașina epigenetică complexă cuprinde mai multe molecule și mărci, inclusiv metilarea ADN-ului, scrierea și ștergerea acestor mărci, modificările histonelor, proteinele și enzimele care permit citirea mărcilor. Include, de asemenea, modele de expresie a ARN-ului necodificator (ARNnc) cu dimensiuni variind de la microARN (~22 nucleotide) la ARNnc lung (>200 nucleotide). Mai multe boli și îmbătrânirea în sine sunt asociate cu modele aberante de semne și molecule epigenetice. Cromatina compactă care se găsește de obicei în celulele de la indivizi tineri sănătoși acumulează daune cauzate de multiple insulte de-a lungul timpului odată cu îmbătrânirea, compromițând în cele din urmă integritatea genomică și funcționarea celulară. Pe măsură ce celulele sunt expuse la factorii de mediu pentru o perioadă lungă de timp, modificările epigenetice pot fi pierdute, adăugate inadecvat sau mutate. Mediul inflamator legat de vârstă cu diferite molecule inhibitoare eliberate din celulele rănite și stresate duce la acumularea de modificări epigenetice, schimbând în cele din urmă funcția celulară.
Magneziul a fost conectat cu epigenetica. Takaya și colab. a constatat că, la descendenții șobolanilor gestante cu deficit de magneziu, promotorii 11β-hidroxisteroid dehidrogenazei-2 (Hsd11b2) hepatice au prezentat o hipermetilare extinsă, contribuind la reglarea în jos a expresiei genelor. În acest studiu, o dietă cu conținut scăzut de magneziu a indus metilarea citozinelor specifice în genele glucocorticoidelor hepatice generând modificări metabolice la descendenții neonatali. Metilarea ADN-ului este legată de atenuarea genelor și de compactarea cromatinei. Într-un studiu pilot încrucișat cu adulți sănătoși supraponderali, profilurile de expresie a genelor au fost examinate după o suplimentare de 4 săptămâni cu magneziu, ceea ce a dus la o reglare în sus a 22 de gene și la o reglare în jos a 36 de gene cu ≥20% față de placebo; multe dintre genele implicate au fost legate de cai inflamatorii. Rezultatele lui Takaya et al. menționate mai sus susțin, cel puțin parțial, potențialele efecte epigenetice ale deficitului/suplimentării de magneziu asupra inflamației. Într-adevăr, deficiența genei Hsd11b1, a cărei regiune promotoare este hipometilată la șobolanii cu deficit de calciu și supraexprimarea genei Hsd11b2 sunt legate de îmbunătățiri ale caracteristicilor metabolice, inclusiv cele legate de diabet și hipertensiune arterială. S-a descoperit că chiar și perioadele scurte de privare de magneziu din dietă reduc în mod semnificativ telomeraza și reglează proteina 53 (p53) și sfingomielinaza din cardiomiocite, o chestiune care este legată de modificări genomice importante în timpul îmbătrânirii și este asociată cu geneza bolilor cardiovasculare.
Disfuncția mitocondrială
Mitocondriile sunt „centrala” celulară care produce cea mai mare parte a ATP-ului disponibil, care este principala sursă de energie pentru procesele celulare. Au propriul lor genom, care este susceptibil la deteriorare, fiind depozitat într-o locație pro-oxidare. Mitocondriile sunt nucleul pentru multiple cascade de semnalizare care conduc destinul celulei fie la supraviețuire, fie la moarte prin apoptoză. Sunt principalele surse de radicali liberi (specii reactive de oxigen, SRO) ca o consecință a metabolismului celular normal și a respirației aerobe, care, atunci când depășesc capacitatea antioxidantă celulară, au fost legate de îmbătrânire și de diferite boli asociate vârstei, inclusiv Alzheimer. și boala Parkinson, printre altele. De fapt, acumularea de mitocondrii disfuncționale este caracteristică îmbătrânirii, cu producție scăzută de ATP și generare crescută de ROS. Excesul de ROS dăunează tuturor moleculelor, de la proteine la ADN, provocându-le mutații și prin urmare, dereglându-le funcția. Mitocondriile disfuncționale produc mai puțin ATP, reducând aportul de energie și conducând, în timp, la inflamație cronică, stres oxidativ și leziuni celulare.
Dintre numeroasele funcții celulare ale magneziului, cea mai proeminentă este probabil legarea sa de ATP din complexul Mg-ATP. Peste o treime din magneziul celular este localizat în mitocondrii și este concentrat în special prin despicarea ARN-ului mitocondrial 2 (Mrs2), care formează un canal proteic de intrare a magneziului și este exprimat în membrana mitocondrială interioară. Diverse enzime ale ciclului acidului tricarboxilic (TCA) și lanțul de transport de electroni depind de magneziu, cuprinzând 2-oxoglutarat dehidrogenază (etapa de limitare a vitezei a ciclului TCA), fosfofructokinaza, hexokinaza, piruvat kinaza și câteva subunități ale lanțului de transport de electroni care acționează ca activatori direcţi ai Complexului V mitocondrial. Perturbarea homeostaziei mitocondriale a magneziului reduce producția de ATP, modifică potențialul membranei mitocondriale și intensifică stresul oxidativ. Diverse investigații au evaluat concentrația de magneziu ca un regulator cheie al bioenergeticii mitocondriale, potențialul transmembranar și starea redox.
Diferențele de deplasare chimică ale rezonanțelor grupurilor α- și β-fosforil ale ATP în spectroscopia de rezonanță magnetică 31P depind de complexarea magneziului cu ATP și oferă o estimare indirectă a magneziului intracelular liber atunci când este combinată cu o măsurare simultană a pH-ului din spectrul 31P. Acest lucru a permis măsurători ale magneziului liber intracelular în relație cu hipertensiunea și diabetul, două dintre cele mai răspândite boli la bătrânețe (Figura 1).
Funcția mitocondrială alterată a fost legată de deficitul de magneziu prin mai multe mecanisme, cuprinzând modificări ale respirației cuplate, suprimarea sistemului de apărare antioxidantă (de exemplu, glutation, superoxid dismutază, catalază, vitamina E), creșterea producției mitocondriale de ROS, atenuarea semnalizării pro-supraviețuire , declanșarea supraîncărcării cu calciu prin intermediul uniporterului de calciu mitocondrial , îmbunătățirea canalului de potasiu mitocondrial sensibil la ATP , deschiderea porilor de tranziție a permeabilității mitocondriale și promovarea canalului anionic al membranei interioare. Aceste efecte duc la depolarizarea potențială a membranei mitocondriale. Dimpotrivă, suplimentarea cu magneziu îmbunătățește funcția mitocondrială prin suprimarea supraproducției de ROS, păstrând potențialul membranei mitocondriale, inhibând deschiderea porilor de tranziție a permeabilității mitocondriale și eliberând citocromul C, reducând acumularea de calciu mitocondrial, crescând expresia limfotică a proteinelor din familia celulelor B2 anti-apoptotice și, concomitent, scăderea expresiei proteinei X asociate cu Bcl-2 pro-apoptotic, reducerea apoptozei prin suprimarea factorului inductibil de hipoxie 1alfa și p38 proteinkinaza activată de mitogen/semnalizarea kinazei N-terminale c-Jun și prin reglarea în jos a autofagiei.
Reducerea magneziului celular perturbă homeostazia mitocondrială și prin modularea Mrs2, un transportor de magneziu care reglează fluxul de magneziu în și în afara mitocondriilor. Acest lucru influențează semnificativ disponibilitatea și vulnerabilitatea energiei celulare. Knockdown-ul experimental al Mrs2 declanșează pierderea complexului I al lanțului de transport de electroni, reduce nivelurile celulare și nucleare de ATP și face celulele mai susceptibile la stimuli apoptotici și inductori de stres oxidativ. Supraexprimarea in vitro a membrului 3 al familiei 41 de purtători soluți (SLC41A3), identificat ca primul sistem de eflux de magneziu mitocondrial la mamifere, s-a dovedit a fi legată de scăderea ATP celular. Activitatea excesivă a potențialului receptor tranzitoriu melastatin 7 (TRPM7), un alt transportator de magneziu, provoacă stres oxidativ și nitrozativ, în timp ce stresul oxidativ inhibă curentul TRPM7 în condiții patologice asociate cu epuizarea ATP intracelular. Într-un model de șoarece de progeria, o dietă suplimentată cu magneziu a crescut potențialul membranei mitocondriale și producția mitocondrială cuplată cu H+ de nicotinamidă adenină dinucleotidă fosfat hidrogen (NADPH) și ATP, inducând speranța de viață prelungită.
S-a demonstrat că la persoanele obeze nivelurile scăzute de magneziu sunt asociate cu deteriorarea stresului oxidativ prin scăderea activității enzimelor antioxidante, peroxidarea lipidelor, căile inflamatorii activate și disfuncția endotelială. O manifestare clinică clară a legăturii strânse dintre magneziu și funcția mitocondrială este legată de funcția musculară. Diverse investigații transversale au raportat asocierea puternică a hipomagnezemiei sau a aportului redus de magneziu cu scăderea masei și funcției musculare. Un studiu de intervenție în rândul femeilor cu vârsta peste 65 de ani a raportat îmbunătățiri ale scorurilor lor de performanță fizică după o suplimentare de magneziu de 12 săptămâni față de placebo. Un studiu anterior a raportat o scădere a absorbției de oxigen în timpul exercițiului submaximal indusă de restricția magneziului alimentar la femeile sănătoase. Legătura strânsă dintre magneziu și mușchi se datorează probabil sintezei mitocondriale a MgATP discutată mai sus. Această legătură a fost definită și pentru mușchiul neted vascular.
Pierderea proteostazei
Homeostazia proteinelor celulare este păstrată printr-o rețea de sistem multicompartimentar care coordonează sinteza, plierea, dezagregarea și degradarea proteinelor. Alterările proteostazei generează autofagie eșuată, pierderi de stabilitate și acumulare de proteine pliate greșit. Mai multe boli cronice legate de vârstă au fost legate de dereglarea proteostazei, inclusiv bolile neurodegenerative și cardiovasculare. Alzheimer și boala Parkinson au fost legate de acumularea de proteine prost pliate, desfăcute sau agregate.
Au fost raportate niveluri scăzute de magneziu în creier în tulburările neurologice, de exemplu, epilepsie, migrenă și boala Alzheimer și Parkinson. Mecanismele primare cele mai acceptate ale acestor stări patologice implică agregarea anormală a proteinei β amiloid extracelulare (Aβ), fosforilarea tau și neuroinflamația cu expresie crescută a factorului de necroză tumorală-α (TNF-α) și interleukinei (IL)-1β. Investigațiile experimentale au descoperit că magneziul a redus TNF-α și IL-1β și a scăzut acumularea creierului de precursori Ap. S-a demonstrat, de asemenea, că magneziul induce clearance-ul Aβ prin căile de degradare a proteazomalului și prin scăderea permeabilității barierei hematoencefalice.
Un rol fundamental în neurotransmisia excitatoare, neuro-excitotoxicitatea, neuroplasticitatea, memoria și ritmul circadian este jucat de receptorul N-metil-D-aspartat (NMDA). Magneziul inhibă receptorii NMDA, iar concentrațiile reduse de magneziu extracelular depolarizează potențialul membranei, producând o excitabilitate crescută.
Proteina de legare a elementului de răspuns la cAMP intracelular (CREB) reglează expresia genei cheie în neuronii dopaminergici. Un studiu recent a constatat că creșterea extracelulară a magneziului a îmbunătățit activarea CREB prin semnalizarea receptorului NMDA atât în neuronii de cultură de șobolan, cât și în feliile de creier, probabil independent de calciul extracelular.
Dereglarea detecției nutrienților
Teoria soma de eliminare afirmă că îmbătrânirea rezultă dintr-un compromis evolutiv între resursele esențiale pentru creștere, reproducere și întreținerea țesuturilor. Astfel, sistemele care detectează și interpretează accesibilitatea resurselor vitale celulare, adică energie și nutrienți sau „sistemele de detectare a nutrienților” sunt cruciale pentru reglarea răspunsurilor și proceselor fiziologice care susțin creșterea, reproducerea și îmbătrânirea. Dezvoltarea bolilor cronice legate de vârstă a fost atribuită, cel puțin parțial, modificărilor diferitelor căi de detectare a nutrienților, cum ar fi factorul de creștere 1 asemănător insulinei/insulină (IIS), protein kinaza activată de 5′ AMP (AMPK). ), mTOR și sirtuine. Calea IIS, fundamentală pentru homeostazia glucozei, a fost prima cale de detectare a nutrienților care a fost descrisă. O cale IIS reglată în jos duce la activarea proteinelor Forkhead Box O (FOXO), care au fost legate de longevitate prin creșterea sensibilității la insulină, modularea opririi ciclului celular, îmbunătățirea biogenezei mitocondriale, suprimarea inflamației și promovarea unei schimbări a substratului metabolic de la glucoză la oxidarea lipidelor. Aceste evenimente au fost asociate cu un risc scăzut de boli legate de vârstă, inclusiv cancer, boli neurodegenerative și diabet. Studiile experimentale pe drojdie, viermi, muște și șoareci au descoperit că reglarea genetică a activității mTOR-Complex1 (mTORC1) promovează îmbătrânirea sănătoasă. Căile mTOR kinazei detectează concentrații mari de aminoacizi; AMPK și sirtuinele simt deficitul de nutrienți, în timp ce căile IIS și mTOR simt abundența de nutrienți. Reglarea AMPK și sirtuinelor promovează o durată de viață crescută prin inactivarea mTOR-C1 și stimularea receptorului gamma coactivator (PGC)-1α activat de proliferatorul peroxizomului.
Dovezile acumulate au legat deficitele de magneziu cu modificări ale sensibilității la insulină și diabet zaharat de tip 2 (T2D). Mai multe anomalii ale magneziului extracelular și intracelular au fost asociate cu T2D. Concentrații scăzute de magneziu intracelular și/sau niveluri scăzute de magneziu plasmatic ionizat au fost detectate la persoanele cu T2D, în ciuda concentrațiilor normale de magneziu seric total. Mecanismele care ajută la explicarea epuizării de magneziu observată în T2D includ o dietă săracă în alimente care conțin magneziu (Figura 3) și pierderea urinară crescută de magneziu.
Două meta-analize ale studiilor prospective au descoperit că aportul de magneziu a fost invers asociat cu incidentul T2D. De asemenea, într-un studiu de urmărire de 10 ani, hipomagnezemia a fost asociată cu afectarea toleranței la glucoză. În schimb, un aport mai mare de magneziu a fost asociat cu o sensibilitate crescută la insulină și cu 30% scădere a riscului de incident T2D față de un aport scăzut de magneziu. Rezultate similare au fost raportate în studiul de dezvoltare a riscului arterei coronariene la adulți tineri (CARDIA) în timpul unei urmăriri de 20 de ani. Un alt studiu a constatat că hiperglicemia și hiperinsulinemia au contribuit la epuizarea magneziului, probabil prin excreția urinară excesivă de magneziu și transportul alterat al magneziului. Pe baza acestor dovezi, suplimentarea cu săruri de magneziu a fost propusă ca un adjuvant non-farmacologic, sigur și ieftin pentru controlul metabolic și prevenirea T2D. Într-o revizuire sistematică și o meta-analiză care cuprinde 25 de studii randomizate controlate (RCT) (12 dintre participanții cu diabet și 6 dintre cei cu risc crescut de T2D), am constatat că suplimentarea cu magneziu a redus glicemia plasmatică a jeun la persoanele cu T2D față de placebo și a îmbunătățit semnificativ glicemia a jeun și încărcarea de glucoză orală după 2 ore la participanții cu risc crescut de diabet. Participantii la suplimentarea cu magneziu au aratat markeri imbunatatiti de sensibilitate la insulina. Într-o analiză generală care urmărește să delimiteze și să evalueze rezultatele asupra sănătății asociate cu aportul și suplimentarea de magneziu, am validat recent asocierea unui aport crescut de magneziu cu un risc scăzut de T2D.
În diferite studii epidemiologice, magneziul alimentar scăzut a fost asociat cu un risc crescut de sindrom metabolic, intoleranță la glucoză și T2D. La femeile sănătoase, un aport mai mare de magneziu a fost asociat cu un nivel mai scăzut de insulină a jeun. Aportul total de magneziu alimentar a fost invers asociat cu răspunsurile la insulină în timpul testelor orale de toleranță la glucoză. Aceste rezultate sunt plauzibile deoarece nivelurile scăzute de magneziu intracelular perturbă activarea tuturor kinazelor în semnalizarea insulinei (Figura 6) și cresc stresul oxidativ, generând rezistența la insulină și condițiile asociate acesteia: sindromul metabolic, intoleranța la glucoză și T2D.
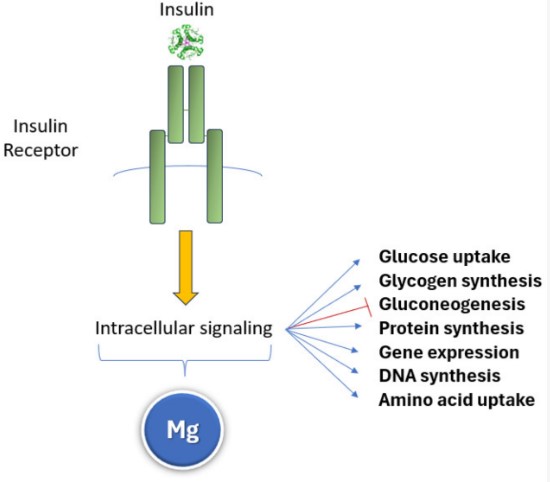
Figura 6. Magneziul influențează toate căile intracelulare de semnalizare a insulinei ca un cofactor al sistemelor enzimatice implicate; prin urmare, modulează efectele asupra metabolismului glucozei și sintezei proteinelor și ADN-ului.
Au fost raportate mai multe tulburări metabolice la animalele experimentale în vârstă, inclusiv intoleranța la glucoză, rezistența la insulină, fosforilarea oxidativă afectată, biosinteza mitocondrială redusă și scăderea oxidării acizilor grași. Oile care suferă de privare de magneziu au prezentat o absorbție redusă de glucoză mediată de insulină, iar suplimentarea cu magneziu a amânat debutul bolii într-un model experimental de diabet. Magneziul are un impact asupra căilor metabolice prin funcția sa de cofactor al sistemelor enzimatice fundamentale din mitocondrii, unde complexul Mg-ATP reglează enzimele glicolitice. Magneziul este implicat în activarea dehidrogenazelor mitocondriale, inclusiv a enzimelor cheie limitatoare ale ciclului TCA, cum ar fi complexul de piruvat dehidrogenază, izocitrat dehidrogenază și complexul 2-oxoglutarat dehidrogenază. În plus, magneziul acționează ca un al doilea mesager care reglează secreția de insulină, deoarece influențează toate căile de semnalizare intracelulară a insulinei (Figura 6). S-a demonstrat că restricția calorică (CR) prelungește durata de viață și previne declinul legat de vârstă prin modificarea condițiilor metabolice în modelele experimentale. Abraham şi colab. a constatat că magneziul a mediat efectele pozitive ale CR prin supresorii R-loops (hibrizi ARN-ADN), în timp ce suplimentarea cu magneziu a avut un efect protector împotriva acreției de R-bucle, care promovează de obicei instabilitatea genomică și o scurtare a duratei de viață.
Senescența celulară
Senescența cuprinde răspunsuri la stresul celular și leziunile care implică oprirea irevocabilă a ciclului celular ca urmare a leziunilor nereparabile ADN și a fenotipului secretor asociat senescenței (SASP), care implică eliberarea de citokine inflamatorii cu acțiuni autocrine, paracrine și endocrine. Alte semne distinctive ale îmbătrânirii, inclusiv disfuncția autofagiei/mitofagiei, disfuncția mitocondrială asociată senescenței, reprogramarea epigenetică și semnalizarea modificată a nutrienților și a stresului au fost legate de senescența celulară, adesea legate de acumularea de leziuni non-telomerice ADN și de biomarkeri relativi. În timpul îmbătrânirii, numărul de celule senescente crește, crescând riscul de boli asociate cu vârsta. La animalele de experiment, durata de sănătate a fost extinsă prin uciderea celulelor senescente cu tratamente farmacologice și genetice. De asemenea, tratamentul cu senolitice (cuprinzând componente alimentare) reduce numărul de celule senescente și amână sau previne îmbătrânirea organismului.
Unele modificări celulare care au loc în timpul senescenței sunt analoge cu cele cauzate de deficitul de magneziu, cuprinzând protecție redusă împotriva daunelor de stres oxidativ, creșterea culturii, progresia ciclului celular, viabilitatea celulară și șansele crescute de exprimare a protooncogenelor și a factorilor de transcripție. În culturile de fibroblaste umane primare sărăcite de magneziu, Killilea și colab. a constatat că capacitatea de replicare a fost mai mică și că expresia biomarkerilor asociați cu senescența, cum ar fi activitatea galactozidazei, p16INK4a, p21WAF1 și uzura telomerilor, a fost crescută, în paralel cu o durată de viață scăzută. Un alt studiu asupra celulelor endoteliale cultivate a constatat că expunerea pe termen scurt la medii cu conținut scăzut de magneziu a promovat caracteristici asociate în mod obișnuit cu senescența endotelială: celulele au devenit mărite, alungite și vacuolate, au exprimat activitatea β-galactozidazei asociată senescenței și a supraexprimat IL-1α, considerată un marker al senescenței endoteliale. În schimb, suplimentarea cu magneziu într-un model de șoarece de îmbătrânire prematură a îmbunătățit funcția mitocondrială, a prevenit stresul oxidativ al țesuturilor și a îmbunătățit durata de viață.
Epuizarea celulelor stem
Celulele stem mențin țesuturile umane datorită capacității lor de auto-reînnoire și capacității de a se diferenția în celule progenitoare, generând diversitatea celulară a diferitelor țesuturi. Funcțiile lor cheie se deteriorează din cauza factorilor extrinseci și intrinseci care promovează îmbătrânirea și bolile legate de vârstă. De exemplu, reducerea potențialului de regenerare al celulelor hematopoietice, legată de vârstă, poate duce la scăderea producției de celule imune adaptative (imunosenescență), care este asociată cu un risc crescut de anemie și afecțiuni maligne mieloide. Imunosenescența se manifestă adesea ca acumulare subclinica de factori proinflamatori și „inflamație”.
Adulții în vârstă prezintă trăsături de imunosenescență cu severitate variabilă, inclusiv scăderea numărului total și capacitatea de proliferare a celulelor stem hematopoietice. Prezența și severitatea fragilității sunt legate de severitatea imunocompetenței. În general, persoanele în vârstă au un grad ușor de imunosupresie din cauza imunosenescenței, adăugat la multimorbiditatea asociată vârstei, declinul organelor, malnutriția, insuficiența funcțională, fragilitatea, sindroamele geriatrice și polifarmacoterapie. Combinația tuturor acestor factori poate ajuta la explicarea susceptibilității crescute la infecții cu prognostic mai rău, inclusiv COVID-19, la dezvoltarea neoplasmelor, a autoimunității și la o capacitate redusă de vindecare a leziunilor cutanate la bătrânețe.
Mai multe investigații susțin rolul magneziului în răspunsul imunitar. Magneziul este un cofactor pentru sinteza imunoglobulinelor (Ig), aderența celulelor imune, convertaza C3, legarea limfocitelor IgM, citoliza dependentă de anticorpi, aderența celulelor T helper-B și răspunsul macrofagelor la limfokine. Magneziul reduce expresia și secreția moleculelor proinflamatorii, cum ar fi substanța P, prin controlul activității factorului nuclear kappa-amplificator al lanțului ușor al celulelor B activate (NF-kB) în condiții normale de magneziu și declanșează o activare crescută a NF- kB și producția de citokine în concentrații suboptime de magneziu. Magneziul modifică, de asemenea, imunitatea dobândită prin reglarea dezvoltării și proliferării limfocitelor. Majoritatea acestor cercetări au fost efectuate pe animale de experiment hrănite cu diete sărace în magneziu. Aceste animale au prezentat un număr crescut și o funcție alterată a celulelor polimorfonucleare, care au fost asociate cu o fagocitoză crescută. Proliferarea și funcția mastocitelor sunt, de asemenea, perturbate de deficitul de magneziu și ar putea fi implicate în fibroza hepatică și steatoza. Apoptoza celulelor B indusă de Fas uman este un proces dependent de magneziu. Alte studii confirmă că animalele experimentale cu deficiență de magneziu prezintă răspunsuri imune specifice scăzute, răspunsuri imunitare exacerbate la stres și inflamație crescută.
În mod interesant, semnificația fundamentală a magneziului în imunitate a fost dezvăluită după caracterizarea XMEN (imunodeficiență legată de X cu defect de magneziu, infecție cu virus Epstein-Barr și neoplazie), o imunodeficiență primară datorată unei deficiențe genetice a transportorului MAGT1, ceea ce a sugerat că magneziul ar putea funcționa ca un al doilea mesager în semnalizarea imună celulară.
Chiar dacă magneziul are un rol crucial în replicarea celulară, precum și în sinteza ADN și ARN, influența homeostaziei alterate a magneziului intra și extracelular asupra țesutului hematopoietic nu este studiată pe larg. Celulele stem mezenchimale osoase (MSC) se pot diferenția în diferite tulpini, de exemplu, osteoblaste și adipocite. Adipocitele sunt regulatori negativi ai hematopoiezei, în timp ce osteoblastele sunt promotori ai acesteia. Concentrațiile mari de magneziu au fost asociate cu creșterea osteoblastogenezei; astfel, deficiența de magneziu, cel puțin parțial, pare a fi dăunătoare sănătății oaselor.
Deficiența de magneziu crește transcripția markerilor de multipotență și a factorilor de transcripție specifici țesuturilor în MSC-uri derivate din țesut adipos uman expuse la un amestec de molecule naturale, adică acizii hialuronic, butiric și retinoizi, care reglează diferențierea. Astfel, lipsa de magneziu poate genera condiții stresante care modulează plasticitatea celulelor stem și potențialul de diferențiere.
Comunicarea intercelulară alterată
Comunicarea dintre celule este esențială pentru coordonarea funcționării celulelor la toate nivelurile (organe, țesuturi, întregul corp) și cuprinde factori solubili, inclusiv citokine, chemokine, neurotransmițători și factori de creștere, recunoscuți de receptorii specifici de la suprafața celulei. Joncțiunile intercelulare contribuie la semnalizarea intracelulară prin schimburi de ioni și molecule de reglare, care sunt cruciale pentru proliferarea, diferențierea și apoptoza celulară. Îmbătrânirea este asociată cu modificări semnificative în comunicarea dintre celule prin căi neuronale, endocrine și neuroendocrine. Inflamația este unul dintre cele mai amplu studiate și relevante evenimente de comunicare intercelulară și se modifică odată cu îmbătrânirea. După cum sa menționat, o trăsătură semnificativă a îmbătrânirii este o inflamație sistemică cronică, de grad scăzut, prevalentă – inflamația – care este legată și predictivă de fragilitate, boli neurodegenerative și risc de mortalitate. Inflamația poate avea mai multe cauze, inclusiv creșterea producției de radicali liberi, creșterea secreției de citokine și adipokine proinflamatorii, activarea îmbunătățită a căii NF-κB și modificări ale microbiomului intestinal și permeabilității intestinale. În propunerea originală, inflamația a fost inclusă ca parte a semnului distinctiv „comunicarea intercelulară alterată”; cu toate acestea, este acum considerată un alt semn distinctiv al îmbătrânirii datorită implicării sale în procesul de îmbătrânire și a rolului său care stă la baza altor semne distinctive, cum ar fi senescența celulară, epuizarea celulelor stem și microbiota intestinală modificată.
Magneziul și sistemele sale de transport sunt modulatori cheie ai comunicării diferitelor căi de semnalizare intracelulară. Receptorul NMDA participă la neurotransmisia excitatoare, neuro-excitotoxicitatea, neuroplasticitatea, memoria și ritmul circadian, toate acestea fiind modificate de vârstă. Magneziul blochează canalul ionic al receptorului NMDA și previne activarea excesivă a acestuia. O reducere a magneziului extracelular depolarizează potențialul membranei, ducând la hiperexcitabilitate. Transportorul de magneziu TRPM7 acționează ca o kinază; au fost definite diferite substraturi kinazei, inclusiv lanțul greu al miozinei IIA, anexina-1 și calpaina, validând rolul TRPM7 în multiple funcții celulare, cuprinzând dilatarea și contracția vasculară, creșterea, apoptoza, migrarea, răspunsurile antiinflamatorii și aderența celulară. Influxul de magneziu prin TRPM7 contribuie la activarea căii de semnalizare fosfoinozitid 3-kinaze (PI3K)/Akt/mTOR în limfocitele B tumorale și produce tranziții metabolice repaus/proliferative. Deoarece TRPM7 este exprimat pe scară largă, s-a sugerat că TRPM7 poate avea un impact asupra tranzițiilor metabolice legate de proliferarea celulară rapidă și malignitatea în multe țesuturi. În plus, supraexprimarea SLC41A1, un schimbător Na+/Magneziu care permite efluxul de magneziu, a atenuat remarcabil fosforilarea kinazelor implicate în evenimentele celulare anti-apoptotice și prin urmare, pro-supraviețuire.
Autofagie compromisă
Modificări ale autofagiei sunt observate în numeroase condiții de îmbătrânire, inclusiv imunosenescență și neurodegenerare. S-a demonstrat că activarea proeminentă a autofagiei crește durata de viață a șoarecelui. În plus, autofagia a fost legată de îmbunătățirea răspunsului imun la vaccinare la oamenii în vârstă, prin depășirea imunosenescenței. În propunerea originală a semnelor distinctive ale îmbătrânirii, autofagia a fost luată în considerare împreună cu semnul distinctiv „proteostază alterată”. Propunerea actualizată include autofagia ca un alt semn distinctiv, datorită rolului său relevant în reglementarea altor semne distinctive, cum ar fi repararea ADN-ului și detectarea/metabolismul nutrienților.
Magneziul este esențial pentru procesele celulare principale, cuprinzând metabolismul energetic, proliferarea și apoptoza. Unele mecanisme prin care magneziul modulează proliferarea celulară includ inhibitorii ciclului celular p53 și p27 și alți modulatori negativi ai proliferării celulare (de exemplu, Jumonji și numblike). Cu toate acestea, dovezile pentru rolul magneziului în apoptoza celulară rămân incerte. În unele modele experimentale, privarea de magneziu a declanșat moartea celulelor prin apoptoză, în timp ce restricția magneziului alimentar a accelerat apoptoza. Cu toate acestea, nivelurile intracelulare de magneziu liber au fost crescute în celulele supuse apoptozei, constituind un eveniment inițial în timpul procesului de apoptoză. Endonucleazele care depind de calciu și magneziu au fost implicate în rupturile ADN-ului în timpul apoptozei. Magneziul poate funcționa ca „al doilea mesager” pentru fazele din aval în apoptoză. Lipsa de magneziu crește tendința de deteriorare oxidativă, permițând modificări ale integrității și funcției membranei.
Disbioza
În ultimele decenii, progresele în cercetarea asupra microbiotei/microbiomului intestinal au pus în evidență importanța acesteia în sănătatea umană. Evoluțiile recente ale metodelor de secvențiere de generație următoare au permis cercetătorilor să investigheze modificările microbiomului care apar în timpul îmbătrânirii și poate, vor ajuta la elucidarea influenței lor asupra fiziologiei gazdei. Potrivit investigațiilor recente, microbiomii intestinali se dovedesc a fi din ce în ce mai unici la fiecare individ în timpul îmbătrânirii, un proces care începe la vârsta adultă mijlocie până târziu. Wilmanski şi colab. a evaluat trei cohorte independente, inclusiv > 9000 de participanți și a constatat că unicitatea compoziției microbiomului a fost asociată puternic și pozitiv cu markerii metabolici cunoscuți ai microbiomului implicați în inflamație, reglare imună, îmbătrânire și longevitate. Participanții sănătoși cu vârsta peste 80 de ani au prezentat o schimbare microbiană susținută către o compoziție unică care a fost absentă la cei mai puțin sănătoși. La participanții cu vârsta > 85 de ani, menținerea unei abundențe relativ ridicate de Bacteroides și o unicitate scăzută a microbiomului intestinal au fost asociate cu o supraviețuire redusă semnificativ în timpul unei urmăriri de 4 ani. Modificările populațiilor microbiene și dialogul încrucișat de-a lungul axei intestin-creier reglează nocicepția inflamatorie, răspunsurile inflamatorii și homeostazia imună, care împreună cu pierderea integrității structurale a intestinului și a altor bariere asociate cu vârsta (de exemplu, bariera hematoencefalică) poate oferi progrese cheie în bolile asociate inflamației legate de vârstă.
Deși până acum există puține studii care explorează relația dintre magneziu și compoziția microbiotei, unele cercetări sugerează că microbiota intestinală ar putea fi un intermediar, legând aportul de magneziu de unele afecțiuni legate de vârstă. În modelele experimentale de artrită reumatoidă (AR), Laragione și colab. a arătat că o dietă bogată în magneziu a redus semnificativ expresia IL-6, IL-1β și TNFα în paralel cu scăderea leziunilor articulare și a severității artritei. În plus, animalele care au primit o dietă bogată în magneziu au avut un număr mai mare de celule T producătoare de IL-10 și celule T reglatoare Foxp3+ (Treg). Transplantul de material fecal de la șoareci cu dietă bogată în magneziu a reprodus fenotipurile observate la șoarecii tratați cu dietă (severitate redusă a artritei și profiluri imunitare modificate). Analizele microbiomului intestinal cu secvențierea ADNr 16S au arătat modificări specifice dietei, cuprinzând niveluri reduse de Prevotella asociată cu RA în grupul cu dietă bogată în magneziu și niveluri crescute de Bacteroides și alte bacterii asociate cu producția crescută de acizi grași cu lanț scurt. Studii similare viitoare ar putea fi efectuate pe alte boli autoimune și inflamatorii.
Hipomagnezemia este un efect secundar raportat frecvent al inhibitorilor pompei de protoni (IPP), un tratament de primă linie pentru tulburările legate de acidul gastric. Microbiomul intestinal poate contribui la dezvoltarea hipomagnezemiei induse de PPI, deoarece utilizarea PPI afectează compoziția microbiomului intestinal prin creșterea pH-ului luminal, modificând absorbția intestinală a magneziului. Un studiu realizat într-un model experimental a constatat că leziunile intestinale și hepatice induse de metotrexat au fost atenuate semnificativ folosind un tratament cu izoglicirrizinat de magneziu, care a remodelat, de asemenea, compoziția microbiană intestinală și a inhibat translocarea bacteriilor în ficat. Del Chierico et al. a evaluat dacă efectele pozitive ale suplimentelor de magneziu ar putea fi mediate de microbiota intestinală într-un model murin de colită. Suplimentarea alimentară cu magneziu a crescut populația de bacterii legate de sănătatea intestinală, homeostazia metabolică și a redus bacteriile asociate cu inflamația și bolile umane asociate, cum ar fi boala inflamatorie intestinală. Un studiu experimental la porci înțărcați a arătat că suplimentarea alimentară cu potasiu-magneziu a redus citokinele inflamatorii din mucoasa jejunală, un fenomen care a fost parțial legat de modificările compoziției microbiotei colonice.
Microbiota intestinală, precum și magneziul, au fost legate de afecțiuni mentale, inclusiv depresie și tulburări de anxietate. Trei studii experimentale au arătat că magneziul are un impact semnificativ pozitiv asupra microbiotei intestinale și a manifestărilor mentale. Într-un studiu, șoarecii care au urmat o dietă săracă în magneziu timp de 6 săptămâni au experimentat o schimbare semnificativă a microbiotei intestinale și un comportament crescut de anxietate. Într-un alt studiu, aceiași cercetători au raportat că șoarecii expuși la o dietă cu deficit de magneziu timp de 6 săptămâni au experimentat un comportament depresiv crescut și modificări ale microbiotei intestinale, au demonstrat o relație între modificarea microbiotei intestinale și schimbarea comportamentelor depresive. Într-un al treilea studiu, Pachikian și colab. au arătat că șoarecii hrăniți cu o dietă cu deficit de magneziu timp de până la 21 de zile au avut concentrații reduse de bifidobacterii, independent de orice alte modificări ale aportului de nutrienți, comparativ cu șoarecii care au fost hrăniți cu o dietă saturată cu magneziu. Șoarecii hrăniți cu o dietă cu conținut scăzut de magneziu au avut, de asemenea, un conținut de ARNm mai mic de factori care controlează funcția barierei intestinale în ileon (zonula occludens-1, occludină, proglucagon) și un conținut de ARNm de 2 ori mai mare în ficat și/sau intestin de TNF -α, IL-6, proteina omoloagă a proteinei care leagă CCAAT/amplificator și factorul de transcripție activator 4, reflectând stresul inflamator și celular.
Chiar dacă dovezile de până acum provin în principal din studii pe animale, constatările sunt interesante și relevante. Deși sunt disponibile studii pe oameni, este totuși înțelept și necesar să se evite deficitul de magneziu prin promovarea consumului de alimente cu conținut ridicat de magneziu (Figura 3).
Inflamaţia
Am menționat deja că inflamația cronică de grad scăzut, sau inflamația, legată de vârstă, este implicată într-o gamă largă de boli cronice. Îmbătrânirea se corelează cu nivelurile sanguine ridicate ale mediatorilor inflamatori, cum ar fi IL-1, IL-6, proteina C reactivă (CRP), interferonul (IFN)α și alte câteva. Datorită importanței sale primordiale care mediază numeroase afecțiuni și căi modificate, în propunerea actualizată a semnelor distinctive ale îmbătrânirii, inflamația a fost inclusă ca una independentă.
Studiile in vitro au arătat că concentrațiile scăzute de magneziu inițiază o producție și eliberare excesivă de IL-1β și TNF-α, activează celulele fagocitare, deschid canalele de calciu, activează receptorul NMDA și semnalizarea NF-κB și stimulează sinteza oxidului nitric și alți markeri inflamatori. S-a demonstrat că, creșterea producției de ROS și homeostazia alterată a calciului declanșată de nivelurile scăzute de magneziu afectează și mai mult funcția mitocondrială, crescând eliberarea markerilor inflamatori. În plus, deficitul de magneziu crește adezivitatea și agregarea trombocitelor și inhibă migrarea și creșterea celulelor endoteliale, putând perturba structura și funcția microvasculară. Concentrațiile adecvate de magneziu inhibă producția de ROS și degranularea mastocitelor, protejează celulele epiteliale și reduc deteriorarea oxidativă și inflamatorie a celulelor și a vaselor de sânge. Concentrația de magneziu este redusă în țesuturile inflamate acut prin activarea axei IL-33/ST2, confirmând importanța magneziului în căile inflamatorii.
În modelele experimentale, privarea de magneziu a condus la creșterea parametrilor inflamatori, inclusiv TNF-α, IL-6, IL-1-β, inhibitorul de activator al plasminogenului-1 și moleculele de adeziune a celulelor vasculare; creșterea producției hepatice și a secreției de proteine de fază acută (adică fibrinogen, α2-macroblobulină, complement); si a crescut numarul de celule inflamatorii circulante . Nivelurile scăzute de magneziu au fost, de asemenea, legate de disfuncția endotelială, care a fost legată și de eliberarea de mediatori inflamatori. În schimb, s-a constatat că suplimentarea cu sulfat de magneziu facilitează efectele antiinflamatorii la macrofagele murine prin reglarea redusă a mediatorilor inflamatori induși de endotoxină și NF-κB, împreună cu inhibarea canalelor ionice de tip L și activarea PI3K. Magneziul are efecte de blocare a canalelor de calciu care duc la suprimarea în aval a IL-6, NF-kB și CRP. Figura 7 ilustrează mai multe căi de semnalizare prin care deficiența de magneziu induce inflamația.
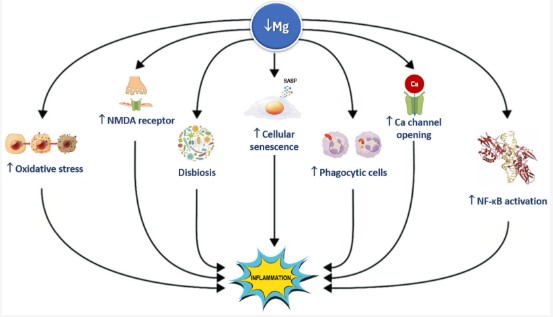
Figura 7. Deficiența de magneziu induce inflamație prin mai multe căi de semnalizare. NF-kB: factor nuclear kappa-amplificator de lanț ușor al celulelor B activate; NMDA: N-metil-D-aspartat; și SASP: fenotip secretor asociat senescenței.
În studiile epidemiologice, concentrațiile scăzute de magneziu seric și un aport scăzut de magneziu din dietă au fost asociate cu inflamație sistemică de grad scăzut. Alte studii au confirmat o asociere inversă a aportului de magneziu și a magneziului seric cu markerii inflamatori. Una dintre cele mai relevante contribuții vine din Studiul de sănătate a asistentelor, în care aportul de magneziu a fost invers asociat cu concentrațiile serice de CRP și legat de prezența sindromului metabolic. De asemenea, King și colab. folosind date de la 70% din populația din 1999-2002 din Sondajul național de sănătate și nutriție (NHANES) care nu a luat suplimente, a constatat că aportul de magneziu sub RDA a fost asociat semnificativ cu CRP crescut. Rezultatele unei mari cohorte finlandeze au coroborat din nou asocierea inversă a unui aport scăzut de magneziu alimentar cu nivelurile serice de CRP.
O meta-analiză anterioară care a inclus opt RCT a arătat că, după suplimentarea cu magneziu, concentrațiile serice de CRP au fost reduse, independent de durata și doza suplimentării cu magneziu. Am efectuat recent o meta-analiză actualizată care include 17 RCT și am constatat că suplimentarea cu magneziu a redus semnificativ diferiți markeri inflamatori umani, în special concentrațiile de oxid nitric și CRP.
Observații
Magneziul este un cation esențial în corpul uman deoarece reglează numeroase procese fiziologice și patologice. Deficitul de magneziu este foarte frecvent la adulții în vârstă. Inflamația cronică de grad scăzut (inflamația) este asociată în mod recurent cu o serie de boli cronice legate de îmbătrânire și cu procesul de îmbătrânire în sine. Deoarece insuficiența magneziului a fost asociată cu o producție excesivă de markeri inflamatori și ROS, am emis anterior ipoteza că o insuficiență cronică de magneziu poate fi unul dintre intermediarii relației dintre inflamație și bolile legate de vârstă. După cum se arată în această revizuire, există dovezi că magneziul este legat de toate semnele distinctive ale îmbătrânirii (Figura 5). Un echilibru optim de magneziu pe parcursul vieții poate ajuta la prevenirea inflamației și a consecințelor aferente acesteia. Cu toate acestea, deși este prudent să păstrați un echilibru adecvat de magneziu printr-o dietă cu suficiente alimente bogate în magneziu (Figura 3) și/sau suplimente atunci când este indicat, este esențial să nu pierdeți din vedere faptul că procesul de îmbătrânire este complex și că corectarea doar a unuia dintre multiplii determinanți poate să nu aibă niciun efect pe termen lung. Cu toate acestea, prezenta revizuire a intenționat să clarifice posibilele mecanisme care pot explica relația strânsă a magneziului cu semnele distinctive ale îmbătrânirii, fără a pretinde că acest cation este singurul sau cel mai important determinant al acestui proces multivariat.
Cum se abordează clinic magneziul la bătrânețe? În primul rând, este esențial să ne asigurăm că seniorii au o dietă adecvată în componentele sale și care include alimente bogate în magneziu (Figura 3). Dacă, din orice motiv, persoana are dificultăți în a urma acest tip de dietă, trebuie luată în considerare suplimentarea cu săruri de magneziu, în special la pacienții afectați de boli sau afecțiuni care sunt asociate mai frecvent cu hipomagnezemie (Tabelul 1 și Tabelul 2). În aceste cazuri, este recomandabil să se măsoare concentrația seric de magneziu a pacientului, care este singura metodă clinică disponibilă pe scară largă, știind că nivelurile sub intervalul normal vor dezvălui doar o depleție severă de magneziu, deoarece cantitatea din ser este mult mai mică decât magneziul intracelular. conținut (Figura 1). Din acest motiv, valorile care tind să fie scăzute, chiar și cele menționate de laborator ca fiind normale, ar trebui considerate inadecvate. De asemenea, este necesar să se ia în considerare polifarmacia; prin urmare, un aport adecvat de alimente bogate în magneziu ar trebui recomandat în primul rând, luând în considerare suplimentarea doar pentru persoanele care nu pot urma o astfel de dietă. Este important de luat în considerare faptul că suplimentarea cu magneziu poate provoca diaree atunci când este administrată în doze mari; prin urmare, este necesară o titrare adecvată a dozei. În plus, evaluarea funcției renale înainte de suplimentare este importantă, în timp ce suplimentarea cu magneziu la pacienții cu insuficiență renală trebuie efectuată cu prudență.
În ultimele decenii, s-au înregistrat progrese semnificative în cercetarea îmbătrânirii, dar o teorie unificată a îmbătrânirii, care poate explica pe deplin un proces atât de complex, lipsește încă de înțeles. Studiul semnelor distinctive ale îmbătrânirii ca evenimente izolate poate ajuta cercetătorii să definească mai bine mecanismele care stau la baza procesului complex de îmbătrânire. Cu toate acestea, aceste mecanisme pot interacționa între ele. De exemplu, starea proinflamatoare rezultă din disfuncția mitocondrială și senescența celulară, printre altele (Figura 7). Posibilele efecte sinergice ale acestor interacțiuni nu sunt simple întrebări de cercetare, de abordat. Cu toate acestea, un factor cu efecte multiple asupra diferitelor semne distinctive ale îmbătrânirii, cum ar fi magneziul, ne poate ajuta să înțelegem legăturile strânse dintre ele și posibil să ne permită să sugerăm că astfel de interacțiuni au efecte de întărire unul asupra celuilalt.
Posibilitatea ca menținerea unui echilibru adecvat de magneziu pe parcursul unei vieți să devină o strategie ieftină și sigură care contribuie la îmbătrânirea sănătoasă este o ipoteză intrigantă, care trebuie explorată în continuare de studiile viitoare bine concepute.
By. Bitanu-Alexandru Sebastian-Alin
Referințe :
1. Beard, J.R.; Officer, A.; de Carvalho, I.A.; Sadana, R.; Pot, A.M.; Michel, J.P.; Lloyd-Sherlock, P.; Epping-Jordan, J.E.; Peeters,
G.M.E.E.; Mahanani, W.R.; et al. The World report on ageing and health: A policy framework for healthy ageing. Lancet 2016, 387,
2145–2154. [CrossRef] [PubMed]
2. Foreman, K.J.; Marquez, N.; Dolgert, A.; Fukutaki, K.; Fullman, N.; McGaughey, M.; Pletcher, M.A.; Smith, A.E.; Tang, K.; Yuan,
C.-W.; et al. Forecasting life expectancy, years of life lost, and all-cause and cause-specific mortality for 250 causes of death:
Reference and alternative scenarios for 2016-40 for 195 countries and territories. Lancet 2018, 392, 2052–2090. [CrossRef] [PubMed]
3. Kuo, P.-L.; Schrack, J.A.; Levine, M.E.; Shardell, M.D.; Simonsick, E.M.; Chia, C.W.; Moore, A.Z.; Tanaka, T.; An, Y.; Karikkineth,
A.; et al. Longitudinal phenotypic aging metrics in the Baltimore Longitudinal Study of Aging. Nat. Aging 2022, 2, 635–643.
[CrossRef] [PubMed]
4. Fabbri, E.; Zoli, M.; Gonzalez-Freire, M.; Salive, M.E.; Studenski, S.A.; Ferrucci, L. Aging and Multimorbidity: New Tasks,
Priorities, and Frontiers for Integrated Gerontological and Clinical Research. J. Am. Med. Dir. Assoc. 2015, 16, 640–647. [CrossRef]
[PubMed]
5. Caspi, R.; Altman, T.; Dreher, K.; Fulcher, C.A.; Subhraveti, P.; Keseler, I.M.; Kothari, A.; Krummenacker, M.; Latendresse, M.;
Mueller, L.A.; et al. The MetaCyc database of metabolic pathways and enzymes and the BioCyc collection of pathway/genome
databases. Nucleic Acids Res. 2012, 40, D742–D753. [CrossRef] [PubMed]
6. Saris, N.-E.L.; Mervaala, E.; Karppanen, H.; Khawaja, J.A.; Lewenstam, A. Magnesium: An update on physiological, clinical and
analytical aspects. Clin. Chim. Acta 2000, 294, 1–26. [CrossRef]
7. Barbagallo, M.; Gupta, R.K.; Dominguez, L.J.; Resnick, L.M. Cellular ionic alterations with age: Relation to hypertension and
diabetes. J. Am. Geriatr. Soc. 2000, 48, 1111–1116. [CrossRef]
8. Barbagallo, M.; Veronese, N.; Dominguez, L.J. Magnesium in Aging, Health and Diseases. Nutrients 2021, 13, 463. [CrossRef]
9. Lopez-Otin, C.; Blasco, M.A.; Partridge, L.; Serrano, M.; Kroemer, G. The hallmarks of aging. Cell 2013, 153, 1194–1217. [CrossRef]
10. López-Otín, C.; Blasco, M.A.; Partridge, L.; Serrano, M.; Kroemer, G. Hallmarks of aging: An expanding universe. Cell 2023, 186,
243–278. [CrossRef]
11. Schmauck-Medina, T.; Molière, A.; Lautrup, S.; Zhang, J.; Chlopicki, S.; Madsen, H.B.; Cao, S.; Soendenbroe, C.; Mansell, E.;
Vestergaard, M.B.; et al. New hallmarks of ageing: A 2022 Copenhagen ageing meeting summary. Aging 2022, 14, 6829–6839.
[CrossRef]
12. Barbagallo, M.; Veronese, N.; Dominguez, L.J. Magnesium in Type 2 Diabetes Mellitus, Obesity, and Metabolic Syndrome.
Nutrients 2022, 14, 714. [CrossRef]
13. Grober, U.; Schmidt, J.; Kisters, K. Magnesium in Prevention and Therapy. Nutrients 2015, 7, 8199–8226. [CrossRef]
14. Barbagallo, M.; Dominguez, L.J.; Galioto, A.; Ferlisi, A.; Cani, C.;Malfa, L.; Pineo, A.; Busardo’, A.; Paolisso, G. Role of magnesium
in insulin action, diabetes and cardio-metabolic syndrome X. Mol. Asp. Med. 2003, 24, 39–52. [CrossRef]
15. Gupta, R.; Benovic, J.; Rose, Z. The determination of the free magnesium level in the human red blood cell by 31P NMR. J. Biol.
Chem. 1978, 253, 6172–6176. [CrossRef] [PubMed]
16. Pan, M.-R.; Li, K.; Lin, S.-Y.; Hung, W.-C. Connecting the Dots: From DNA Damage and Repair to Aging. Int. J. Mol. Sci. 2016, 17,
685. [CrossRef]
17. Ford, E.S.; Mokdad, A.H. Dietary magnesium intake in a national sample of US adults. J. Nutr. 2003, 133, 2879–2882. [CrossRef]
[PubMed]
18. Resnick, L.M.; Gupta, R.K.; Laragh, J.H. Intracellular free magnesium in erythrocytes of essential hypertension: Relation to blood
pressure and serum divalent cations. Proc. Natl. Acad. Sci. USA 1984, 81, 6511–6515. [CrossRef] [PubMed]
19. Resnick, L.M.; Gupta, R.K.; Laragh, J.H.; Alderman, M.H.; Altura, B.M. Intracellular and extracellular magnesium depletion in
Type 2 (non-insulin-dependent) diabetes mellitus. Diabetologia 1993, 36, 767–770. [CrossRef] [PubMed]
20. Mathers, J.C. Impact of nutrition on the ageing process. Br. J. Nutr. 2015, 113, S18–S22. [CrossRef] [PubMed]
21. Aguilera, A.; Gómez-González, B. Genome instability: A mechanistic view of its causes and consequences. Nat. Rev. Genet. 2008,
9, 204–217. [CrossRef] [PubMed]
22. Jackson, S.P.; Bartek, J. The DNA-damage response in human biology and disease. Nature 2009, 461, 1071–1078. [CrossRef]
[PubMed]
23. Hoeijmakers, J.H. DNA damage, aging, and cancer. N. Engl. J. Med. 2009, 361, 1475–1485. [CrossRef] [PubMed]
24. Laconi, E.; Marongiu, F.; DeGregori, J. Cancer as a disease of old age: Changing mutational and microenvironmental landscapes.
Br. J. Cancer 2020, 122, 943–952. [CrossRef]
25. Chiu, T.K.; Dickerson, R.E. 1 A crystal structures of B-DNA reveal sequence-specific binding and groove-specific bending of DNA
by magnesium and calcium. J. Mol. Biol. 2000, 301, 915–945. [CrossRef]
26. Sirover, M.A.; Loeb, L.A. Metal activation of DNA synthesis. Biochem. Biophys. Res. Commun. 1976, 70, 812–817. [CrossRef]
27. Ohyama, T. New Aspects of Magnesium Function: A Key Regulator in Nucleosome Self-Assembly, Chromatin Folding and Phase
Separation. Int. J. Mol. Sci. 2019, 20, 4232. [CrossRef]
28. Price, M.A.; Tullius, T.D. Using hydroxyl radical to probe DNA structure. Methods Enzymol. 1992, 212, 194–219.
29. SantaLucia, J., Jr.; Hicks, D. The thermodynamics of DNA structural motifs. Annu. Rev. Biophys. Biomol. Struct. 2004, 33, 415–440.
[CrossRef]
Nutrients 2024, 16, 496 20 of 28
30. Bui, V.; Nguyen, T. DNA aggregation induced by Mg2+ ions under different conditions. J. Mol. Recognit. 2018, 31, e2721.
[CrossRef]
31. Anastassopoulou, J.; Theophanides, T. Magnesium-DNA interactions and the possible relation of magnesium to carcinogenesis.
Irradiation and free radicals. Crit. Rev. Oncol. Hematol. 2002, 42, 79–91. [CrossRef] [PubMed]
32. Kielar, C.; Xin, Y.; Shen, B.; Kostiainen, M.A.; Grundmeier, G.; Linko, V.; Keller, A. On the Stability of DNA Origami Nanostructures
in Low-Magnesium Buffers. Angew. Chem. Int. Ed Engl. 2018, 57, 9470–9474. [CrossRef] [PubMed]
33. Calsou, P.; Salles, B. Properties of damage-dependent DNA incision by nucleotide excision repair in human cell-free extracts.
Nucleic Acids Res. 1994, 22, 4937–4942. [CrossRef] [PubMed]
34. Ban, C.; Junop, M.; Yang,W. Transformation of MutL by ATP binding and hydrolysis: A switch in DNA mismatch repair. Cell
1999, 97, 85–97. [CrossRef]
35. Hartwig, A. Role of magnesium in genomic stability. Mutat. Res. Fundam. Mol. Mech. Mutagen. 2001, 475, 113–121. [CrossRef]
36. Blackburn, E.H.; Epel, E.S.; Lin, J. Human telomere biology: A contributory and interactive factor in aging, disease risks, and
protection. Science 2015, 350, 1193–1198. [CrossRef]
37. Saretzki, G. Telomeres, Telomerase and Ageing. Subcell. Biochem. 2018, 90, 221–308.
38. Herrmann, M.; Pusceddu, I.; Marz, W.; Herrmann, W. Telomere biology and age-related diseases. CCLM 2018, 56, 1210–1222.
[CrossRef]
39. von Zglinicki, T. Oxidative stress shortens telomeres. Trends Biochem. Sci. 2002, 27, 339–344. [CrossRef]
40. Yadav, S.; Maurya, P.K. Correlation Between Telomere Length and Biomarkers of Oxidative Stress in Human Aging. Rejuvenation
Res. 2022, 25, 25–29. [CrossRef]
41. Calado, R.T.; Young, N.S. Telomere diseases. N. Engl. J. Med. 2009, 361, 2353–2365. [CrossRef]
42. Boonekamp, J.J.; Simons, M.J.P.; Hemerik, L.; Verhulst, S. Telomere length behaves as biomarker of somatic redundancy rather
than biological age. Aging Cell 2013, 12, 330–332. [CrossRef]
43. Astuti, Y.; Wardhana, A.; Watkins, J.; Wulaningsih, W. Cigarette smoking and telomere length: A systematic review of 84 studies
and meta-analysis. Environ. Res. 2017, 158, 480–489. [CrossRef]
44. Arsenis, N.C.; You, T.; Ogawa, E.F.; Tinsley, G.M.; Zuo, L. Physical activity and telomere length: Impact of aging and potential
mechanisms of action. Oncotarget 2017, 8, 45008–45019. [CrossRef]
45. Ganesh, S.; Qin, Z.; Spagnol, S.T.; Biegler, M.T.; Coffey, K.A.; Kalinowski, A.; Buehler, M.J.; Dahl, K.N. The tail domain of lamin B1
is more strongly modulated by divalent cations than lamin A. Nucleus 2015, 6, 203–211. [CrossRef]
46. Zvereva, M.I.; Shcherbakova, D.M.; Dontsova, O.A. Telomerase: Structure, functions, and activity regulation. Biochemistry 2010,
75, 1563–1583. [CrossRef] [PubMed]
47. Zhou, J.; Ding, D.; Wang, M.; Cong, Y.-S. Telomerase reverse transcriptase in the regulation of gene expression. BMB Rep. 2014, 47,
8–14. [CrossRef] [PubMed]
48. Liu, Y.;Wang, Q.; Zhang, Z.; Fu, R.; Zhou, T.; Long, C.; He, T.; Yang, D.; Li, Z.; Peng, S. Magnesium supplementation enhances
mTOR signalling to facilitate myogenic differentiation and improve aged muscle performance. Bone 2021, 146, 115886. [CrossRef]
[PubMed]
49. Feeney, K.A.; Hansen, L.L.; Putker, M.; Olivares-Yanez, C.; Day, J.; Eades, L.J.; Larrondo, L.F.; Hoyle, N.P.; O’neill, J.S.; van Ooijen,
G. Daily magnesium fluxes regulate cellular timekeeping and energy balance. Nature 2016, 532, 375–379. [CrossRef] [PubMed]
50. Chen,W.-D.;Wen, M.-S.; Shie, S.-S.; Lo, Y.-L.;Wo, H.-T.;Wang, C.-C.; Hsieh, I.-C.; Lee, T.-H.;Wang, C.-Y. The circadian rhythm
controls telomeres and telomerase activity. Biochem. Biophys. Res. Commun. 2014, 451, 408–414. [CrossRef]
51. Pal, S.; Tyler, J.K. Epigenetics and aging. Sci. Adv. 2016, 2, e1600584. [CrossRef] [PubMed]
52. Yu, M.; Hazelton, W.D.; Luebeck, G.E.; Grady, W.M. Epigenetic Aging: More Than Just a Clock When it Comes to Cancer. Cancer
Res. 2020, 80, 367–374. [CrossRef] [PubMed]
53. Feinberg, A.P.; Levchenko, A. Epigenetics as a mediator of plasticity in cancer. Science 2023, 379, eaaw3835. [CrossRef] [PubMed]
54. Cora, D.; Re, A.; Caselle, M.; Bussolino, F. MicroRNA-mediated regulatory circuits: Outlook and perspectives. Phys. Biol. 2017, 14,
045001. [CrossRef] [PubMed]
55. Takaya, J.; Iharada, A.; Okihana, H.; Kaneko, K. Magnesium deficiency in pregnant rats alters methylation of specific cytosines in
the hepatic hydroxysteroid dehydrogenase-2 promoter of the offspring. Epigenetics 2011, 6, 573–578. [CrossRef] [PubMed]
56. Newell-Price, J.; Clark, A.J.; King, P. DNA methylation and silencing of gene expression. Trends Endocrinol. Metab. 2000, 11,
142–148. [CrossRef]
57. Chacko, S.A.; Sul, J.; Song, Y.; Li, X.; LeBlanc, J.; You, Y.; Butch, A.; Liu, S. Magnesium supplementation, metabolic and
inflammatory markers, and global genomic and proteomic profiling: A randomized, double-blind, controlled, crossover trial in
overweight individuals. Am. J. Clin. Nutr. 2011, 93, 463–473. [CrossRef]
58. Takaya, J.; Iharada, A.; Okihana, H.; Kaneko, K. A calcium-deficient diet in pregnant, nursing rats induces hypomethylation of
specific cytosines in the 11beta-hydroxysteroid dehydrogenase-1 promoter in pup liver. Nutr. Res. 2013, 33, 961–970. [CrossRef]
59. Hruby, A.; McKeown, N.M.; Song, Y.; Djoussé, L. Dietary magnesium and genetic interactions in diabetes and related risk factors:
A brief overview of current knowledge. Nutrients 2013, 5, 4990–5011. [CrossRef] [PubMed]
60. Shah, N.C.; Shah, G.J.; Li, Z.; Jiang, X.C.; Altura, B.T.; Altura, B.M. Short-term magnesium deficiency downregulates telomerase,
up-regulates neutral sphingomyelinase and induces oxidative DNA damage in cardiovascular tissues: Relevance to atherogenesis,
cardiovascular diseases and aging. Int. J. Clin. Exp. Med. 2014, 7, 497–514. [PubMed]
Nutrients 2024, 16, 496 21 of 28
61. McBride, H.M.; Neuspiel, M.; Wasiak, S. Mitochondria: More than just a powerhouse. Curr. Biol. 2006, 16, R551–R560. [CrossRef]
62. Hekimi, S.; Lapointe, J.; Wen, Y. Taking a “good” look at free radicals in the aging process. Trends Cell Biol. 2011, 21, 569–576.
[CrossRef] [PubMed]
63. Park, J.-S.; Davis, R.L.; Sue, C.M. Mitochondrial Dysfunction in Parkinson’s Disease: New Mechanistic Insights and Therapeutic
Perspectives. Curr. Neurol. Neurosci. Rep. 2018, 18, 21. [CrossRef] [PubMed]
64. Birnbaum, J.H.; Wanner, D.; Gietl, A.F.; Saake, A.; Kundig, T.M.; Hock, C.; Nitsch, R.M.; Tackenberg, C. Oxidative stress and
altered mitochondrial protein expression in the absence of amyloid-beta and tau pathology in iPSC-derived neurons from
sporadic Alzheimer’s disease pa-tients. Stem Cell Res. 2018, 27, 121–130. [CrossRef] [PubMed]
65. Whitehall, J.C.; Greaves, L.C. Aberrant mitochondrial function in ageing and cancer. Biogerontology 2020, 21, 445–459. [CrossRef]
[PubMed]
66. Romani, A.; Marfella, C.; Scarpa, A. Cell magnesium transport and homeostasis: Role of intracellular compartments. Miner.
Electrolyte Metab. 1993, 19, 282–289. [PubMed]
67. Zsurka, G.; Gregá ˇ n, J.; Schweyen, R.J. The human mitochondrial Mrs2 protein functionally substitutes for its yeast homologue, a
candidate magnesium transporter. Genomics 2001, 72, 158–168. [CrossRef] [PubMed]
68. Garfinkel, L.; Garfinkel, D. Magnesium regulation of the glycolytic pathway and the enzymes involved. Magnesium 1985, 4, 60–72.
[PubMed]
69. Soulimane, T.; Buse, G. Integral cytochrome-c oxidase. Preparation and progress towards a three-dimensional crystallization. Eur.
J. Biochem. 1995, 227, 588–595. [CrossRef]
70. Yamanaka, R.; Tabata, S.; Shindo, Y.; Hotta, K.; Suzuki, K.; Soga, T.; Oka, K. Mitochondrial Mg2+ homeostasis decides cellular
energy metabolism and vulnerability to stress. Sci. Rep. 2016, 6, 30027. [CrossRef]
71. Pilchova, I.; Klacanova, K.; Tatarkova, Z.; Kaplan, P.; Racay, P. The Involvement of Mg2+ in Regulation of Cellular and Mitochondrial
Functions. Oxidative Med. Cell. Longev. 2017, 2017, 6797460. [CrossRef] [PubMed]
72. Resnick, L.M.; Barbagallo, M.; Dominguez, L.J.; Veniero, J.M.; Nicholson, J.P.; Gupta, R.K. Relation of cellular potassium to other
mineral ions in hypertension and diabetes. Hypertension 2001, 38 Pt 2, 709–712. [CrossRef]
73. Dominguez, L.J.; Veronese, N.; Barbagallo, M. Magnesium and Hypertension in Old Age. Nutrients 2020, 13, 139. [CrossRef]
[PubMed]
74. Gout, E.; Rebeille, F.; Douce, R.; Bligny, R. Interplay of Mg2+, ADP, and ATP in the cytosol and mitochondria: Unravelling the role
of Mg2+ in cell respiration. Proc. Natl. Acad. Sci. USA 2014, 111, E4560–E4567. [CrossRef]
75. Panov, A.; Scarpa, A. Mg2+ control of respiration in isolated rat liver mitochondria. Biochemistry. Biochemistry 1996, 35,
12849–12856. [CrossRef]
76. Rodríguez-Zavala, J.S.; Moreno-Sánchez, R. Modulation of oxidative phosphorylation by Mg2+ in rat heart mitochondria. J. Biol.
Chem. 1998, 273, 7850–7855. [CrossRef] [PubMed]
77. Morais, J.B.; Severo, J.S.; Santos, L.R.; de Sousa Melo, S.R.; de Oliveira Santos, R.; de Oliveira, A.R.; Cruz, K.J.C.; Marreiro, D.D.N.
Role of Magnesium in Oxidative Stress in Individuals with Obesity. Biol. Trace Elem. Res. 2017, 176, 20–26. [CrossRef]
78. Calviello, G.; Ricci, P.; Lauro, L.; Palozza, P.; Cittadini, A. Mg deficiency induces mineral content changes and oxidative stress in
rats. Biochem. Mol. Biol. Int. 1994, 32, 903–911.
79. Shah, N.C.; Liu, J.-P.; Iqbal, J.; Hussain, M.; Jiang, X.-C.; Li, Z.; Li, Y.; Zheng, T.; Li,W.; Sica, A.C.; et al. Mg deficiency results in
modulation of serum lipids, glutathione, and NO synthase isozyme activation in cardiovascular tissues: Relevance to de novo
synthesis of ceramide, serum Mg and atherogenesis. Int. J. Clin. Exp. Med. 2011, 4, 103–118.
80. Kumar, B.P.; Shivakumar, K. Depressed antioxidant defense in rat heart in experimental magnesium deficiency implications for
the pathogenesis of myocardial lesions. Biol. Trace Element Res. 1997, 60, 139–144. [CrossRef]
81. Liu, M.; Dudley, S.C., Jr. Magnesium, Oxidative Stress, Inflammation, and Cardiovascular Disease. Antioxidants 2020, 9, 907.
[CrossRef]
82. Liu, M.; Jeong, E.-M.; Liu, H.; Xie, A.; So, E.Y.; Shi, G.; Jeong, G.E.; Zhou, A.; Dudley, S.C. Magnesium supplementation improves
diabetic mitochondrial and cardiac diastolic function. J. Clin. Investig. 2019, 4, e123182. [CrossRef] [PubMed]
83. Liu, M.; Liu, H.; Feng, F.; Xie, A.; Kang, G.; Zhao, Y.; Hou, C.R.; Zhou, X.; Dudley, S.C., Jr. Magnesium Deficiency Causes a
Reversible, Metabolic, Diastolic Cardiomyopathy. J. Am. Heart Assoc. 2021, 10, e020205. [CrossRef]
84. Kramer, J.H.; Mišík, V.;Weglicki,W.B. Magnesium-deficiency potentiates free radical production associated with postischemic
injury to rat hearts: Vitamin E affords protection. Free Radic. Biol. Med. 1994, 16, 713–723. [CrossRef]
85. Chen, Y.;Wei, X.; Yan, P.; Han, Y.; Sun, S.;Wu, K.; Fan, D. Human mitochondrial Mrs2 protein promotes multidrug resistance
in gastric cancer cells by regulating p27, cyclin D1 expression and cytochrome C release. Cancer Biol. Ther. 2009, 8, 607–614.
[CrossRef]
86. Salvi, M.; Bozac, A.; Toninello, A. Gliotoxin induces Mg2+ efflux from intact brain mitochondria. Neurochem. Int. 2004, 45, 759–764.
[CrossRef]
87. Sponder, G.; Abdulhanan, N.; Frohlich, N.; Mastrototaro, L.; Aschenbach, J.R.; Rontgen, M.; Pilchova, I.; Cibulka, M.; Racay, P.;
Kolisek, M. Overexpression of Na(+)/Mg2+exchanger SLC41A1 attenuates pro-survival signaling. Oncotarget 2018, 9, 5084–5104.
[CrossRef] [PubMed]
88. Racay, P. Effect of magnesium on calcium-induced depolarisation of mitochondrial transmembrane potential. Cell Biol. Int. 2008,
32, 136–145. [CrossRef] [PubMed]
Nutrients 2024, 16, 496 22 of 28
89. Blomeyer, C.A.; Bazil, J.N.; Stowe, D.F.; Dash, R.K.; Camara, A.K.S. Mg2+ differentially regulates two modes of mitochondrial
Ca2+ uptake in isolated cardiac mitochondria: Implications for mitochondrial Ca2+ sequestration. J. Bioenerg. Biomembr. 2016, 48,
175–188. [CrossRef]
90. Bednarczyk, P.; Dolowy, K.; Szewczyk, A. Matrix Mg2+ regulates mitochondrial ATP-dependent potassium channel from heart.
FEBS Lett. 2005, 579, 1625–1632. [CrossRef]
91. Zoratti, M.; Szabo, I. The mitochondrial permeability transition. Biochim. Biophys Acta. 1995, 1241, 139–176. [CrossRef]
92. Beavis, A.D.; Powers, M.F. On the regulation of the mitochondrial inner membrane anion channel by magnesium and protons. J.
Biol. Chem. 1989, 264, 17148–17155. [CrossRef] [PubMed]
93. Sharikabad, M.N.; Ostbye, K.M.; Brors, O. Increased [Mg2+]o reduces Ca2+ influx and disruption of mitochondrial membrane
potential during reoxygenation. Am. J. Physiol. Heart Circ. Physiol. 2001, 281, H2113–H2123. [CrossRef] [PubMed]
94. Huang, C.Y.; Hsieh, Y.L.; Ju, D.T.; Lin, C.C.; Kuo, C.H.; Liou, Y.F.; Ho, T.-J.; Tsai, C.-H.; Tsai, F.-J.; Lin, J.-Y. Attenuation of
Magnesium Sulfate on CoCl(2)-Induced Cell Death by Activating ERK1/2/MAPK and Inhibiting HIF-1alpha via Mitochondrial
Apoptotic Signaling Suppression in a Neuronal Cell Line. Chin. J. Physiol. 2015, 58, 244–253. [CrossRef] [PubMed]
95. Gorgoglione, V.; Laraspata, D.; La Piana, G.; Marzulli, D.; Lofrumento, N.E. Protective effect of magnesium and potassium ions
on the permeability of the external mitochondrial membrane. Arch. Biochem. Biophys. 2007, 461, 13–23. [CrossRef]
96. La Piana, G.; Gorgoglione, V.; Laraspata, D.; Marzulli, D.; Lofrumento, N.E. Effect of magnesium ions on the activity of the
cytosolic NADH/cytochrome c electron transport system. FEBS J. 2008, 275, 6168–6179. [CrossRef]
97. Seo, Y.-W.; Na Shin, J.; Ko, K.H.; Cha, J.H.; Park, J.Y.; Lee, B.R.; Yun, C.-W.; Kim, Y.M.; Seol, D.-W.; Kim, D.-W.; et al. The molecular
mechanism of Noxa-induced mitochondrial dysfunction in p53-mediated cell death. J. Biol. Chem. 2003, 278, 48292–48299.
[CrossRef]
98. Ferrari, R.; Albertini, A.; Curello, S.; Ceconi, C.; Dilisa, F.; Raddino, R.; Visioli, O. Myocardial recovery during post-ischaemic
reperfusion: Effects of nifedipine, calcium and magnesium. J. Mol. Cell. Cardiol. 1986, 18, 487–498. [CrossRef]
99. Boelens, A.D.; Pradhan, R.K.; Blomeyer, C.A.; Camara, A.K.S.; Dash, R.K.; Stowe, D.F. Extra-matrix Mg2+ limits Ca2+ uptake and
modulates Ca2+ uptake–independent respiration and redox state in cardiac isolated mitochondria. J. Bioenerg. Biomembr. 2013, 45,
203–218. [CrossRef]
100. Li, Y.;Wang, J.; Yue, J.;Wang, Y.; Yang, C.; Cui, Q. High magnesium prevents matrix vesicle-mediated mineralization in human
bone marrow-derived mesenchymal stem cells via mitochondrial pathway and autophagy. Cell Biol. Int. 2018, 42, 205–215.
[CrossRef]
101. Mastrototaro, L.; Smorodchenko, A.; Aschenbach, J.R.; Kolisek, M.; Sponder, G. Solute carrier 41A3 encodes for a mitochondrial
Mg2+efflux system. Sci. Rep. 2016, 6, 27999. [CrossRef]
102. Su, L.-T.; Chen, H.-C.; González-Pagán, O.; Overton, J.D.; Xie, J.; Yue, L.; Runnels, L.W. TRPM7 activates m-calpain by stressdependent
stimulation of p38 MAPK and c-Jun N-terminal kinase. J. Mol. Biol. 2010, 396, 858–869. [CrossRef]
103. Inoue, H.; Murayama, T.; Tashiro, M.; Sakurai, T.; Konishi, M. Mg2+- and ATP-dependent inhibition of transient receptor potential
melastatin 7 by oxidative stress. Free. Radic. Biol. Med. 2014, 72, 257–266. [CrossRef]
104. Villa-Bellosta, R. Dietary magnesium supplementation improves lifespan in a mouse model of progeria. EMBO Mol. Med. 2020,
12, e12423. [CrossRef]
105. Dominguez, L.J.; Barbagallo, M.; Lauretani, F.; Bandinelli, S.; Bos, A.; Corsi, A.M.; Simonsick, E.M.; Ferrucci, L. Magnesium and
muscle performance in older persons: The InCHIANTI study. Am. J. Clin. Nutr. 2006, 84, 419–426. [CrossRef] [PubMed]
106. Welch, A.A.; Kelaiditi, E.; Jennings, A.; Steves, C.J.; Spector, T.D.; MacGregor, A. Dietary Magnesium Is Positively Associated
With Skeletal Muscle Power and Indices of Muscle Mass and May Attenuate the Association Between Circulating C-Reactive
Protein and Muscle Mass in Women. J. Bone Miner. Res. 2016, 31, 317–325. [CrossRef]
107. Hayhoe, R.P.; Lentjes, M.A.; Mulligan, A.A.; Luben, R.N.; Khaw, K.-T.;Welch, A.A. Cross-sectional associations of dietary and
circulating magnesium with skeletal muscle mass in the EPIC-Norfolk cohort. Clin. Nutr. 2019, 38, 317–323. [CrossRef] [PubMed]
108. Verlaan, S.; Aspray, T.J.; Bauer, J.M.; Cederholm, T.; Hemsworth, J.; Hill, T.R.; McPhee, J.S.; Piasecki, M.; Seal, C.; Sieber, C.C.; et al.
Nutritional status, body composition, and quality of life in community-dwelling sarcopenic and non-sarcopenic older adults: A
case-control study. Clin. Nutr. 2017, 36, 267–274. [CrossRef] [PubMed]
109. Veronese, N.; Berton, L.; Carraro, S.; Bolzetta, F.; De Rui, M.; Perissinotto, E.; Toffanello, E.D.; Bano, G.; Pizzato, S.; Miotto, F.; et al.
Effect of oral magnesium supplementation on physical performance in healthy elderly women involved in a weekly exercise
program: A randomized controlled trial. Am. J. Clin. Nutr. 2014, 100, 974–981. [CrossRef]
110. Lukaski, H.C.; Nielsen, F.H. Dietary magnesium depletion affects metabolic responses during submaximal exercise in postmenopausal
women. J. Nutr. 2002, 132, 930–935. [CrossRef]
111. Cameron, D.; Welch, A.A.; Adelnia, F.; Bergeron, C.M.; Reiter, D.A.; Dominguez, L.J.; Brennan, N.A.; Fishbein, K.W.; Spencer,
R.G.; Ferrucci, L. Age and Muscle Function Are More Closely Associated With Intracellular Magnesium, as Assessed by 31P
Magnetic Resonance Spectroscopy, Than With Serum Magnesium. Front. Physiol. 2019, 10, 1454. [CrossRef]
112. van Dronkelaar, C.; van Velzen, A.; Abdelrazek, M.; van der Steen, A.;Weijs, P.J.M.; Tieland, M. Minerals and Sarcopenia; The
Role of Calcium, Iron, Magnesium, Phosphorus, Potassium, Selenium, Sodium, and Zinc on Muscle Mass, Muscle Strength, and
Physical Performance in Older Adults: A Systematic Review. J. Am. Med. Dir. Assoc. 2018, 19, 6–11.e3. [CrossRef]
113. Labbadia, J.; Morimoto, R.I. The biology of proteostasis in aging and disease. Annu. Rev. Biochem. 2015, 84, 435–464. [CrossRef]
Nutrients 2024, 16, 496 23 of 28
114. Yerbury, J.J.; Ooi, L.; Dillin, A.; Saunders, D.N.; Hatters, D.M.; Beart, P.M.; Cashman, N.R.;Wilson, M.R.; Ecroyd, H.Walking the
tightrope: Proteostasis and neurodegenerative disease. J. Neurochem. 2016, 137, 489–505. [CrossRef]
115. Henning, R.H.; Brundel, B.J.J.M. Proteostasis in cardiac health and disease. Nat. Rev. Cardiol. 2017, 14, 637–653. [CrossRef]
116. Dugger, B.N.; Dickson, D.W. Pathology of Neurodegenerative Diseases. Cold Spring Harb. Perspect. Biol. 2017, 9, a028035.
[CrossRef]
117. Veronese, N.; Zurlo, A.; Solmi, M.; Luchini, C.; Trevisan, C.; Bano, G.; Manzato, E.; Sergi, G.; Rylander, R. Magnesium Status in
Alzheimer’s Disease: A Systematic Review. Am. J. Alzheimers Dis. Other Demen. 2016, 31, 208–213. [CrossRef] [PubMed]
118. Yu, J.; Sun, M.; Chen, Z.; Lu, J.; Liu, Y.; Zhou, L.; Xu, X.; Fan, D.; Chui, D. Magnesium modulates amyloid-beta protein precursor
trafficking and processing. J. Alzheimers Dis. 2010, 20, 1091–1106. [CrossRef] [PubMed]
119. Yu, X.; Guan, P.P.; Zhu, D.; Liang, Y.Y.; Wang, T.; Wang, Z.Y.; Wang, P. Magnesium Ions Inhibit the Expression of Tumor Necrosis
Factor alpha and the Activity of gamma-Secretase in a beta-Amyloid Protein-Dependent Mechanism in APP/PS1 Transgenic
Mice. Front. Mol. Neurosci. 2018, 11, 172. [CrossRef] [PubMed]
120. Zhu, D.; Su, Y.; Fu, B.; Xu, H. Magnesium Reduces Blood-Brain Barrier Permeability and Regulates Amyloid-beta Transcytosis.
Mol. Neurobiol. 2018, 55, 7118–7131. [CrossRef] [PubMed]
121. Hansen, K.B.; Yi, F.; Perszyk, R.E.; Furukawa, H.; Wollmuth, L.P.; Gibb, A.J.; Traynelis, S.F. Structure, function, and allosteric
modulation of NMDA receptors. J. Gen. Physiol. 2018, 150, 1081–1105. [CrossRef]
122. Nechifor, M. Magnesium in addiction—A general view. Magnes. Res. 2018, 31, 90–98. [CrossRef]
123. Hou, H.; Wang, L.; Fu, T.; Papasergi, M.; Yule, D.I.; Xia, H. Magnesium Acts as a Second Messenger in the Regulation of NMDA
Re-ceptor-Mediated CREB Signaling in Neurons. Mol. Neurobiol. 2020, 57, 2539–2550. [CrossRef]
124. Templeman, N.M.; Murphy, C.T. Regulation of reproduction and longevity by nutrient-sensing pathways. J. Cell Biol. 2018, 217,
93–106. [CrossRef] [PubMed]
125. de Lucia, C.; Murphy, T.; Steves, C.J.; Dobson, R.J.B.; Proitsi, P.; Thuret, S. Lifestyle mediates the role of nutrient-sensing pathways
in cognitive aging: Cellular and epidemiological evidence. Commun. Biol. 2020, 3, 157. [CrossRef] [PubMed]
126. Kenyon, C.; Chang, J.; Gensch, E.; Rudner, A.; Tabtiang, R. A C. elegans mutant that lives twice as long as wild type. Nature 1993,
366, 461–464. [CrossRef] [PubMed]
127. Puig, O.; Tjian, R. Transcriptional feedback control of insulin receptor by dFOXO/FOXO1. Minerva Anestesiol. 2005, 19, 2435–2446.
[CrossRef] [PubMed]
128. van der Horst, A.; Burgering, B.M. Stressing the role of FoxO proteins in lifespan and disease. Nat. Rev. Mol. Cell Biol. 2007, 8,
440–450. [CrossRef] [PubMed]
129. van Heemst, D. Insulin, IGF-1 and longevity. Aging Dis. 2010, 1, 147–157. [PubMed]
130. Calnan, D.R.; Brunet, A. The FoxO code. Oncogene 2008, 27, 2276–2288. [CrossRef] [PubMed]
131. Johnson, S.C.; Rabinovitch, P.S.; Kaeberlein, M. mTOR is a key modulator of ageing and age-related disease. Nature 2013, 493,
338–345. [CrossRef]
132. Alers, S.; Loffler, A.S.;Wesselborg, S.; Stork, B. Role of AMPK-mTOR-Ulk1/2 in the regulation of autophagy: Cross talk, shortcuts,
and feedbacks. Mol. Cell Biol. 2012, 32, 2–11. [CrossRef] [PubMed]
133. Rodgers, J.T.; Lerin, C.; Haas, W.; Gygi, S.P.; Spiegelman, B.M.; Puigserver, P. Nutrient control of glucose homeostasis through a
complex of PGC-1α and SIRT1. Nature 2005, 434, 113–118. [CrossRef] [PubMed]
134. Barbagallo, M.; Dominguez, L.J. Magnesium metabolism in type 2 diabetes mellitus, metabolic syndrome and insulin resistance.
Arch. Biochem. Biophys. 2007, 458, 40–47. [CrossRef] [PubMed]
135. Barbagallo, M.; Dominguez, L.J. Magnesium and type 2 diabetes. World J. Diabetes 2015, 6, 1152–1157. [CrossRef] [PubMed]
136. Mather, H.M.; Levin, G.E. Magnesium status in diabetes. Lancet 1979, 1, 924. [CrossRef] [PubMed]
137. Schnack, C.; Bauer, I.; Pregant, P.; Hopmeier, P.; Schernthaner, G. Hypomagnesaemia in Type 2 (non-insulin-dependent) diabetes
mellitus is not corrected by improvement of long-term metabolic control. Diabetologia 1992, 35, 77–79. [CrossRef] [PubMed]
138. Barbagallo, M.; Di Bella, G.; Brucato, V.; D’angelo, D.; Damiani, P.; Monteverde, A.; Belvedere, M.; Dominguez, L.J. Serum ionized
magnesium in diabetic older persons. Metabolism 2014, 63, 502–509. [CrossRef] [PubMed]
139. Walti, M.K.; Zimmermann, M.B.; Walczyk, T.; Spinas, G.A.; Hurrell, R.F. Measurement of magnesium absorption and retention in
type 2 diabetic patients with the use of stable isotopes. Am. J. Clin. Nutr. 2003, 78, 448–453. [CrossRef]
140. Larsson, S.C.; Wolk, A. Magnesium intake and risk of type 2 diabetes: A meta-analysis. J. Intern. Med. 2007, 262, 208–214.
[CrossRef]
141. Dong, J.Y.; Xun, P.; He, K.; Qin, L.Q. Magnesium intake and risk of type 2 diabetes: Meta-analysis of prospective cohort studies.
Diabetes Care 2011, 34, 2116–2122. [CrossRef]
142. Guerrero-Romero, F.; Rascón-Pacheco, R.A.; Rodríguez-Morán, M.; De La Pena, J.E.; Wacher, N. Hypomagnesaemia and risk for
metabolic glucose disorders: A 10-year follow-up study. Eur. J. Clin. Investig. 2008, 38, 389–396. [CrossRef] [PubMed]
143. Ma, B.; Lawson, A.B.; Liese, A.D.; Bell, R.A.; Mayer-Davis, E.J. Dairy, magnesium, and calcium intake in relation to insulin
sensitivity: Approaches to modeling a dose-dependent association. Am. J. Epidemiol. 2006, 164, 449–458. [CrossRef]
144. Song, Y.; Manson, J.E.; Buring, J.E.; Liu, S. Dietary magnesium intake in relation to plasma insulin levels and risk of type 2
diabetes in women. Diabetes Care 2004, 27, 59–65. [CrossRef]
145. Lopez-Ridaura, R.; Willett, W.C.; Rimm, E.B.; Liu, S.; Stampfer, M.J.; Manson, J.E.; Hu, F.B. Magnesium intake and risk of type 2
diabetes in men and women. Diabetes Care 2004, 27, 134–140. [CrossRef]
Nutrients 2024, 16, 496 24 of 28
146. Kim, D.J.; Xun, P.; Liu, K.; Loria, C.; Yokota, K.; Jr, D.R.J.; He, K. Magnesium intake in relation to systemic inflammation, insulin
resistance, and the incidence of diabetes. Diabetes Care 2010, 33, 2604–2610. [CrossRef] [PubMed]
147. McNAIR, P.; Christensen, M.S.; Christiansen, C.; Madsbad, S.; Transbol, I. Renal hypomagnesaemia in human diabetes mellitus:
Its relation to glucose homeostasis. Eur. J. Clin. Investig. 1982, 12, 81–85. [CrossRef]
148. Djurhuus, M.; Skott, P.; Hother-Nielsen, O.; Klitgaard, N.; Beck-Nielsen, H. Insulin increases renal magnesium excretion: A
possible cause of magnesium depletion in hyperinsulinaemic states. Diabet. Med. 1995, 12, 664–669. [CrossRef]
149. Veronese, N.; Dominguez, L.J.; Pizzol, D.; Demurtas, J.; Smith, L.; Barbagallo, M. Oral Magnesium Supplementation for Treating
Glucose Metabolism Parameters in People with or at Risk of Diabetes: A Systematic Review and Meta-Analysis of Double-Blind
Ran-domized Controlled Trials. Nutrients 2021, 13, 4074. [CrossRef]
150. Veronese, N.; Demurtas, J.; Pesolillo, G.; Celotto, S.; Barnini, T.; Calusi, G.; Caruso, M.G.; Notarnicola, M.; Reddavide, R.; Stubbs,
B.; et al. Magnesium and health outcomes: An umbrella review of systematic reviews and meta-analyses of observational and
intervention studies. Eur. J. Nutr. 2020, 59, 263–272. [CrossRef]
151. He, K.; Liu, K.; Daviglus, M.L.; Morris, S.J.; Loria, C.M.; Van Horn, L.; Jacobs, D.R.; Savage, P.J. Magnesium intake and incidence
of metabolic syndrome among young adults. Circulation 2006, 113, 1675–1682. [CrossRef]
152. Fung, T.T.; Manson, J.E.; Solomon, C.G.; Liu, S.;Willett,W.C.; Hu, F.B. The association between magnesium intake and fasting
insulin concentration in healthy middle-aged women. J. Am. Coll. Nutr. 2003, 22, 533–538. [CrossRef]
153. Humphries, S.; Kushner, H.; Falkner, B. Low dietary magnesium is associated with insulin resistance in a sample of young,
nondiabetic Black Americans. Am. J. Hypertens. 1999, 12 Pt 1, 747–756. [CrossRef] [PubMed]
154. Houtkooper, R.H.; Argmann, C.; Houten, S.M.; Cantó, C.; Jeninga, E.H.; Andreux, P.A.; Thomas, C.; Doenlen, R.; Schoonjans, K.;
Auwerx, J. The metabolic footprint of aging in mice. Sci. Rep. 2011, 1, 134. [CrossRef] [PubMed]
155. Matsunobu, S.; Terashima, Y.; Senshu, T.; Sano, H.; Itoh, H. Insulin secretion and glucose uptake in hypomagnesemic sheep fed a
low magnesium, high potassium diet. J. Nutr. Biochem. 1990, 1, 167–171. [CrossRef] [PubMed]
156. Balon, T.W.; Gu, J.L.; Tokuyama, Y.; Jasman, A.P.; Nadler, J.L. Magnesium supplementation reduces development of diabetes in a
rat model of spontaneous NIDDM. Am. J. Physiol. Metab. 1995, 269, E745–E752. [CrossRef] [PubMed]
157. Thomas, A.P.; Diggle, T.; Denton, R.M. Sensitivity of pyruvate dehydrogenase phosphate phosphatase to magnesium ions. Similar
effects of spermine and insulin. Biochem. J. 1986, 238, 83–91. [CrossRef] [PubMed]
158. Tretter, L.; Adam-Vizi, V. Alpha-ketoglutarate dehydrogenase: A target and generator of oxidative stress. Philos. Trans. R. Soc. B
Biol. Sci. 2005, 360, 2335–2345. [CrossRef]
159. McLain, A.L.; Szweda, P.A.; Szweda, L.I. alpha-Ketoglutarate dehydrogenase: A mitochondrial redox sensor. Free Radic. Res.
2011, 45, 29–36. [CrossRef]
160. Mooren, F.C. Magnesium and disturbances in carbohydrate metabolism. Diabetes Obes. Metab. 2015, 17, 813–823. [CrossRef]
161. Rodríguez-Morán, M.; Guerrero-Romero, F. Insulin secretion is decreased in non-diabetic individuals with hypomagnesaemia.
Diabetes/Metab. Res. Rev. 2011, 27, 590–596. [CrossRef] [PubMed]
162. Kamran, M.; Kharazmi, F.; Malekzadeh, K.; Talebi, A.; Khosravi, F.; Soltani, N. Effect of Long-term Administration of Oral
Magnesium Sulfate and Insulin to Reduce Streptozotocin-Induced Hyperglycemia in Rats: The Role of Akt2 and IRS1 Gene
Expressions. Biol. Trace Element Res. 2019, 190, 396–404. [CrossRef]
163. Le Couteur, D.G.; Simpson, S.J. 90th Anniversary Commentary: Caloric Restriction Effects on Aging. J. Nutr. 2018, 148, 1656–1659.
[CrossRef] [PubMed]
164. Abraham, K.J.; Chan, J.N.; Salvi, J.S.; Ho, B.; Hall, A.; Vidya, E.; Guo, R.; Killackey, S.A.; Liu, N.; Lee, J.E.; et al. Intersection of
calorie restriction and magnesium in the suppression of genome-destabilizing RNA–DNA hybrids. Nucleic Acids Res. 2016, 44,
8870–8884. [CrossRef]
165. Collado, M.; Blasco, M.A.; Serrano, M. Cellular senescence in cancer and aging. Cell 2007, 130, 223–233. [CrossRef]
166. Tchkonia, T.; Zhu, Y.; van Deursen, J.; Campisi, J.; Kirkland, J.L. Cellular senescence and the senescent secretory phenotype:
Therapeutic opportunities. J. Clin. Investig. 2013, 123, 966–972. [CrossRef]
167. Song, S.; Lam, E.W.-F.; Tchkonia, T.; Kirkland, J.L.; Sun, Y. Senescent Cells: Emerging Targets for Human Aging and Age-Related
Diseases. Trends Biochem. Sci. 2020, 45, 578–592. [CrossRef] [PubMed]
168. Baker, D.J.; Childs, B.G.; Durik, M.;Wijers, M.E.; Sieben, C.J.; Zhong, J.; Saltness, R.A.; Jeganathan, K.B.; Verzosa, G.C.; Pezeshki,
A.; et al. Naturally occurring p16Ink4a-positive cells shorten healthy lifespan. Nature 2016, 530, 184–189. [CrossRef]
169. Xu, M.; Pirtskhalava, T.; Farr, J.N.;Weigand, B.M.; Palmer, A.K.;Weivoda, M.M.; Inman, C.L.; Ogrodnik, M.B.; Hachfeld, C.M.;
Fraser, D.G.; et al. Senolytics improve physical function and increase lifespan in old age. Nat. Med. 2018, 24, 1246–1256. [CrossRef]
170. Blackburn, E.H. Telomere states and cell fates. Nature 2000, 408, 53–56. [CrossRef]
171. Sgambato, A.;Wolf, F.I.; Faraglia, B.; Cittadini, A. Magnesium depletion causes growth inhibition, reduced expression of cyclin
D1, and increased expression of P27Kip1 in normal but not in transformed mammary epithelial cells. J. Cell. Physiol. 1999, 180,
245–254. [CrossRef]
172. Killilea, D.W.; Ames, B.N. Magnesium deficiency accelerates cellular senescence in cultured human fibroblasts. Proc. Natl. Acad.
Sci. USA 2008, 105, 5768–5773. [CrossRef] [PubMed]
173. Ferrè, S.; Mazur, A.; Maier, J.A.M. Low-magnesium induces senescent features in cultured human endothelial cells. Magnes. Res.
2007, 20, 66–71. [PubMed]
Nutrients 2024, 16, 496 25 of 28
174. Mihaylova, M.M.; Sabatini, D.M.; Yilmaz, H. Dietary and metabolic control of stem cell function in physiology and cancer. Cell
Stem Cell 2014, 14, 292–305. [CrossRef] [PubMed]
175. Gruver, A.; Hudson, L.; Sempowski, G. Immunosenescence of ageing. J. Pathol. 2007, 211, 144–156. [CrossRef] [PubMed]
176. Fulop, T.; Larbi, A.; Dupuis, G.; Le Page, A.; Frost, E.H.; Cohen, A.A.;Witkowski, J.M.; Franceschi, C. Immunosenescence and
Inflamm-Aging as Two Sides of the Same Coin: Friends or Foes? Front. Immunol. 2017, 8, 1960. [CrossRef] [PubMed]
177. Elias, R.; Hartshorn, K.; Rahma, O.; Lin, N.; Snyder-Cappione, J.E. Aging, immune senescence, and immunotherapy: A
comprehensive review. Semin. Oncol. 2018, 45, 187–200. [CrossRef]
178. Tannou, T.; Koeberle, S.; Manckoundia, P.; Aubry, R. Multifactorial immunodeficiency in frail elderly patients: Contributing
factors and management. Med. Mal. Infect. 2019, 49, 167–172. [CrossRef]
179. Dominguez, L.J.; Veronese, N.; Guerrero-Romero, F.; Barbagallo, M. Magnesium in Infectious Diseases in Older People. Nutrients
2021, 13, 180. [CrossRef]
180. Tam, M.; Gómez, S.; González-Gross, M.; Marcos, A. Possible roles of magnesium on the immune system. Eur. J. Clin. Nutr. 2003,
57, 1193–1197. [CrossRef]
181. Galland, L. Magnesium and immune function: An overview. Magnesium 1988, 7, 290–299.
182. Sugimoto, J.; Romani, A.M.; Valentin-Torres, A.M.; Luciano, A.A.; Kitchen, C.M.R.; Funderburg, N.; Mesiano, S.; Bernstein, H.B.
Magnesium decreases inflammatory cytokine production: A novel innate immunomodulatory mechanism. J. Immunol. 2012, 188,
6338–6346. [CrossRef]
183. Feske, S.; Skolnik, E.Y.; Prakriya, M. Ion channels and transporters in lymphocyte function and immunity. Nat. Rev. Immunol.
2012, 12, 532–547. [CrossRef]
184. Bussière, F.; Tridon, A.; Zimowska, W.; Mazur, A.; Rayssiguier, Y. Increase in complement component C3 is an early response to
experimental magnesium deficiency in rats. Life Sci. 2003, 73, 499–507. [CrossRef]
185. Kraeuter, S.L.; Schwartz, R. Blood and mast cell histamine levels in magnesium-deficient rats. J. Nutr. 1980, 110, 851–858.
[CrossRef]
186. Takemoto, S.; Yamamoto, A.; Tomonaga, S.; Funaba, M.; Matsui, T. Magnesium deficiency induces the emergence of mast cells in
the liver of rats. J. Nutr. Sci. Vitaminol. 2013, 59, 560–563. [CrossRef]
187. Chien, M.M.; Zahradka, K.E.; Newell, M.K.; Freed, J. HFas-induced B cell apoptosis requires an increase in free cytosolic
magnesium as an early event. J. Biol. Chem. 1999, 274, 7059–7066. [CrossRef] [PubMed]
188. Malpuech-Brugere, C.; Nowacki, W.; Daveau, M.; Gueux, E.; Linard, C.; Rock, E.; Lebreton, J.-P.; Mazur, A.; Rayssiguier, Y.
Inflammatory response following acute mag-nesium deficiency in the rat. Biochim. Biophys. Acta. 2000, 1501, 91–98. [CrossRef]
189. Petrault, I.; Zimowska, W.; Mathieu, J.; Bayle, D.; Rock, E.; Favier, A.; Rayssiguier, Y.; Mazur, A. Changes in gene expression in rat
thymocytes identified by cDNA array support the occurrence of oxidative stress in early magnesium deficiency. Biochim. Biophys.
Acta (BBA) Mol. Basis Dis. 2002, 1586, 92–98. [CrossRef]
190. Zimowska, W.; Girardeau, J.P.; Kuryszko, J.; Bayle, D.; Rayssiguier, Y.; Mazur, A. Morphological and immune response alterations
in the intestinal mucosa of the mouse after short periods on a low-magnesium diet. Br. J. Nutr. 2002, 88, 515–522. [CrossRef]
[PubMed]
191. Li, F.-Y.; Chaigne-Delalande, B.; Kanellopoulou, C.; Davis, J.C.; Matthews, H.F.; Douek, D.C.; Cohen, J.I.; Uzel, G.; Su, H.C.;
Lenardo, M.J. Second messenger role for Mg2+ revealed by human T-cell immunodeficiency. Nature 2011, 475, 471–476. [CrossRef]
192. Li, F.-Y.; Chaigne-Delalande, B.; Su, H.; Uzel, G.; Matthews, H.; Lenardo, M.J. XMEN disease: A new primary immunodeficiency
affecting Mg2+ regulation of immunity against Epstein-Barr virus. Blood 2014, 123, 2148–2152. [CrossRef]
193. Chaigne-Delalande, B.; Li, F.-Y.; O’connor, G.M.; Lukacs, M.J.; Jiang, P.; Zheng, L.; Shatzer, A.; Biancalana, M.; Pittaluga, S.;
Matthews, H.F.; et al. Mg2+ regulates cytotoxic functions of NK and CD8 T cells in chronic EBV infection through NKG2D. Science
2013, 341, 186–191. [CrossRef] [PubMed]
194. Lima, F.D.S.; Fock, R.A. A Review of the Action of Magnesium on Several Processes Involved in the Modulation of Hematopoiesis.
Int. J. Mol. Sci. 2020, 21, 7084. [CrossRef]
195. Naveiras, O.; Nardi, V.; Wenzel, P.L.; Hauschka, P.V.; Fahey, F.; Daley, G.Q. Bone-marrow adipocytes as negative regulators of the
haematopoietic microenvironment. Nature 2009, 460, 259–263. [CrossRef] [PubMed]
196. Sugimura, R.; Li, L. Shifting in balance between osteogenesis and adipogenesis substantially influences hematopoiesis. J. Mol.
Cell Biol. 2010, 2, 61–62. [CrossRef]
197. Rude, R.K.; Gruber, H.E. Magnesium deficiency and osteoporosis: Animal and human observations. J. Nutr. Biochem. 2004, 15,
710–716. [CrossRef] [PubMed]
198. Castiglioni, S.; Cazzaniga, A.; Albisetti,W.; Maier, J.A.M. Magnesium and osteoporosis: Current state of knowledge and future
research directions. Nutrients 2013, 5, 3022–3033. [CrossRef]
199. Sargenti, A.; Castiglioni, S.; Olivi, E.; Bianchi, F.; Cazzaniga, A.; Farruggia, G.; Cappadone, C.; Merolle, L.; Malucelli, E.; Ventura,
C.; et al. Magnesium Deprivation Potentiates Human Mesenchymal Stem Cell Transcriptional Remodeling. Int. J. Mol. Sci. 2018,
19, 1410. [CrossRef]
200. Mittelbrunn, M.; Sánchez-Madrid, F. Intercellular communication: Diverse structures for exchange of genetic information. Nat.
Rev. Mol. Cell Biol. 2012, 13, 328–335. [CrossRef]
Nutrients 2024, 16, 496 26 of 28
201. Franceschi, C.; Bonafe, M.; Valensin, S.; Olivieri, F.; De Luca, M.; Ottaviani, E.; De Benedictis, G. Inflamm-aging: An evolutionary
perspective on immunosenescence. Ann. N. Y. Acad. Sci. 2000, 908, 244–254. [CrossRef] [PubMed]
202. Cohen, H.J.; Pieper, C.F.; Harris, T.; Rao, K.M.; Currie, M.S. The association of plasma IL-6 levels with functional disability in
commu-nity-dwelling elderly. J. Gerontol. A Biol. Sci. Med. Sci. 1997, 52, M201–M208. [CrossRef] [PubMed]
203. Franceschi, C.; Campisi, J. Chronic inflammation (inflammaging) and its potential contribution to age-associated diseases. J.
Gerontol. A Ser. Biol. Sci. Med. Sci. 2014, 69 (Suppl. S1), S4–S9. [CrossRef] [PubMed]
204. Rosano, C.; Marsland, A.L.; Gianaros, P.J. Maintaining brain health by monitoring inflammatory processes: A mechanism to
promote successful aging. Aging Dis. 2012, 3, 16–33. [PubMed]
205. Harris, T.B.; Ferrucci, L.; Tracy, R.P.; Corti, M.C.; Wacholder, S.; Ettinger, W.H., Jr.; Heimovitz, H.; Cohen, H.J.; Wallace, R.
Associations of elevated Interleukin-6 and C-Reactive protein levels with mortality in the elderly. Am. J. Med. 1999, 106, 506–512.
[CrossRef] [PubMed]
206. Michaud, M.; Balardy, L.; Moulis, G.; Gaudin, C.; Peyrot, C.; Vellas, B.; Vellas, B.; Cesari, M.; Nourhashemi, F. Proinflammatory
cytokines, aging, and age-related diseases. J. Am. Med. Dir. Assoc. 2013, 14, 877–882. [CrossRef] [PubMed]
207. Szarcvel Szic, K.; Declerck, K.; Vidakovic, M.; Vanden Berghe, W. From inflammaging to healthy aging by dietary lifestyle choices:
Is epigenetics the key to personalized nutrition? Clin. Epigenetics 2015, 7, 33. [CrossRef] [PubMed]
208. Xia, S.; Zhang, X.; Zheng, S.; Khanabdali, R.; Kalionis, B.;Wu, J.;Wan,W.; Tai, X. An Update on Inflamm-Aging: Mechanisms,
Prevention, and Treatment. J. Immunol. Res. 2016, 2016, 8426874. [CrossRef]
209. Fransen, F.; Van Beek, A.A.; Borghuis, T.; El Aidy, S.; Hugenholtz, F.; van der Gaast–de Jongh, C.; Savelkoul, H.F.J.; De Jonge, M.I.;
Boekschoten, M.V.; Smidt, H.; et al. Aged Gut Microbiota Contributes to Systemical Inflammaging after Transfer to Germ-Free
Mice. Front. Immunol. 2017, 8, 1385. [CrossRef]
210. Leonardi, G.C.; Accardi, G.; Monastero, R.; Nicoletti, F.; Libra, M. Ageing: From inflammation to cancer. Immun. Ageing 2018, 15,
1. [CrossRef]
211. Shapiro, H.A.; Thaiss, C.; Levy, M.; Elinav, E. The cross talk between microbiota and the immune system: Metabolites take center
stage. Curr. Opin. Immunol. 2014, 30, 54–62. [CrossRef]
212. Yogi, A.; Callera, G.E.; Antunes, T.T.; Tostes, R.C.; Touyz, R.M. Transient receptor potential melastatin 7 (TRPM7) cation channels,
magnesium and the vascular system in hypertension. Circ. J. 2011, 75, 237–245. [CrossRef]
213. Schlingmann, K.P.; Waldegger, S.; Konrad, M.; Chubanov, V.; Gudermann, T. TRPM6 and TRPM7—Gatekeepers of human
magnesium metabolism. Biochim. Biophys. Acta (BBA) Mol. Basis Dis. 2007, 1772, 813–821. [CrossRef] [PubMed]
214. Trzeciakiewicz, A.; Opolski, A.; Mazur, A. TRPM7: A protein responsible for magnesium homeostasis in a cell. Adv. Hyg. Exp.
Med. 2005, 59, 496–502.
215. Sahni, J.; Tamura, R.; Sweet, I.R.; Scharenberg, A.M. TRPM7 regulates quiescent/proliferative metabolic transitions in lymphocytes.
Cell Cycle 2010, 9, 3565–3574. [CrossRef] [PubMed]
216. Wong, S.Q.; Kumar, A.V.; Mills, J.; Lapierre, L.R. Autophagy in aging and longevity. Hum. Genet. 2020, 139, 277–290. [CrossRef]
[PubMed]
217. Aman, Y.; Schmauck-Medina, T.; Hansen, M.; Morimoto, R.I.; Simon, A.K.; Bjedov, I.; Palikaras, K.; Simonsen, A.; Johansen, T.;
Tavernarakis, N.; et al. Autophagy in healthy aging and disease. Nat. Aging 2021, 1, 634–650. [CrossRef] [PubMed]
218. Fernández, Á.F.; Sebti, S.; Wei, Y.; Zou, Z.; Shi, M.; McMillan, K.L.; He, C.; Ting, T.; Liu, Y.; Chiang, W.-C.; et al. Disruption of the
beclin 1–BCL2 autophagy regulatory complex promotes longevity in mice. Nature 2018, 558, 136–140. [CrossRef]
219. Alsaleh, G.; Panse, I.; Swadling, L.; Zhang, H.; Richter, F.C.; Meyer, A.; Lord, J.; Barnes, E.; Klenerman, P.; Green, C.; et al.
Autophagy in T cells from aged donors is maintained by spermidine and correlates with function and vaccine responses. Elife
2020, 9, e57950. [CrossRef]
220. Kaushik, S.; Cuervo, A.M. The coming of age of chaperone-mediated autophagy. Nat. Rev. Mol. Cell Biol. 2018, 19, 365–381.
[CrossRef]
221. Wolf, F.I.; Trapani, V. Cell (patho)physiology of magnesium. Clin. Sci. 2008, 114, 27–35. [CrossRef] [PubMed]
222. Ikari, A.; Sawada, H.; Sanada, A.; Tonegawa, C.; Yamazaki, Y.; Sugatani, J. Magnesium deficiency suppresses cell cycle progression
mediated by increase in transcriptional activity of p21(Cip1) and p27(Kip1) in renal epithelial NRK-52E cells. J. Cell. Biochem.
2011, 112, 3563–3572. [CrossRef] [PubMed]
223. Martin, H.; Richert, L.; Berthelot, A. Magnesium deficiency induces apoptosis in primary cultures of rat hepatocytes. J. Nutr. 2003,
133, 2505–2511. [CrossRef] [PubMed]
224. Feng, H.; Guo, L.; Gao, H.; Li, X.-A. Deficiency of calcium and magnesium induces apoptosis via scavenger receptor BI. Life Sci.
2011, 88, 606–612. [CrossRef]
225. Krzywoszyn´ ska, K.; Witkowska, D.; S´wia˛tek-Kozłowska, J.; Szebesczyk, A.; Kozłowski, H. General Aspects of Metal Ions as
Signaling Agents in Health and Disease. Biomolecules 2020, 10, 1417. [CrossRef]
226. Giannakis, C.; Forbes, I.J.; Zalewski, P.D. Ca2+ Mg2+-dependent nuclease: Tissue distribution, relationship to inter-nucleosomal
DNA fragmentation and inhibition by Zn2+. Biochem. Biophys. Res. Commun. 1991, 181, 915–920. [CrossRef]
227. Wilmanski, T.; Diener, C.; Rappaport, N.; Patwardhan, S.; Wiedrick, J.; Lapidus, J.; Earls, J.C.; Zimmer, A.; Glusman, G.; Robinson,
M.; et al. Gut microbiome pattern reflects healthy ageing and predicts survival in humans. Nat. Metab. 2021, 3, 274–286. [CrossRef]
228. Agirman, G.; Yu, K.B.; Hsiao, E.Y. Signaling inflammation across the gut-brain axis. Science 2021, 374, 1087–1092. [CrossRef]
Nutrients 2024, 16, 496 27 of 28
229. Laragione, T.; Harris, C.; Azizgolshani, N.; Beeton, C.; Bongers, G.; Gulko, P.S. Magnesium increases numbers of Foxp3+ Treg
cells and reduces arthritis severity and joint damage in an IL-10-dependent manner mediated by the intestinal microbiome.
EBioMedicine 2023, 92, 104603. [CrossRef] [PubMed]
230. Gommers, L.M.M.; Hoenderop, J.G.J.; de Baaij, J.H.F. Mechanisms of proton pump inhibitor-induced hypomagnesemia. Acta
Physiol. 2022, 235, e13846. [CrossRef] [PubMed]
231. Xia, Y.; Shi, H.; Qian, C.; Han, H.; Lu, K.; Tao, R.; Gu, R.; Zhao, Y.; Wei, Z.; Lu, Y.; et al. Modulation of Gut Microbiota by
Magnesium Isoglycyrrhizinate Mediates En-hancement of Intestinal Barrier Function and Amelioration of Methotrexate-Induced
Liver Injury. Front Immunol. 2022, 13, 874878. [CrossRef]
232. Del Chierico, F.; Trapani, V.; Petito, V.; Reddel, S.; Pietropaolo, G.; Graziani, C.; Masi, L.; Gasbarrini, A.; Putignani, L.; Scaldaferri,
F.; et al. Dietary Magnesium Alleviates Experimental Murine Colitis through Modulation of Gut Microbiota. Nutrients 2021, 13,
4188. [CrossRef]
233. Cao, S.; Huang, K.; Wen, X.; Gao, J.; Cui, B.; Yao, K.; Zhan, X.; Hu, S.; Wu, Q.; Xiao, H.; et al. Dietary supplementation with
potassium-magnesium sulfate modulates the antioxidant capacity, immunity, and gut microbiota in weaned piglets. Front.
Microbiol. 2022, 13, 961989. [CrossRef]
234. Jorgensen, B.P.; Winther, G.; Kihl, P.; Nielsen, D.S.; Wegener, G.; Hansen, A.K.; Sorensen, D.B. Dietary magnesium deficiency
affects gut microbiota and anxiety-like behaviour in C57BL/6N mice. Acta Neuropsychiatr. 2015, 27, 307–311. [CrossRef] [PubMed]
235. Winther, G.; Jorgensen, B.M.P.; Elfving, B.; Nielsen, D.S.; Kihl, P.; Lund, S.; Sorensen, D.B.; Wegener, G. Dietary magnesium
deficiency alters gut microbiota and leads to depressive-like behaviour. Acta Neuropsychiatr. 2015, 27, 168–176. [CrossRef]
[PubMed]
236. Pachikian, B.D.; Neyrinck, A.M.; Deldicque, L.; De Backer, F.C.; Catry, E.; Dewulf, E.M.; Sohet, F.M.; Bindels, L.B.; Everard, A.;
Francaux, M.; et al. Changes in intestinal bifidobacteria levels are associated with the inflammatory response in magnesiumdeficient
mice. J. Nutr. 2010, 140, 509–514. [CrossRef] [PubMed]
237. Ferrucci, L.; Fabbri, E. Inflammageing: Chronic inflammation in ageing, cardiovascular disease, and frailty. Nat. Rev. Cardiol.
2018, 15, 505–522. [CrossRef] [PubMed]
238. Kolisek, M.; Touyz, R.M.; Romani, A.; Barbagallo, M. Magnesium and Other Biometals in Oxidative Medicine and Redox Biology.
Oxidative Med. Cell. Longev. 2017, 2017, 7428796. [CrossRef] [PubMed]
239. Maier, J.A.; Castiglioni, S.; Locatelli, L.; Zocchi, M.; Mazur, A. Magnesium and inflammation: Advances and perspectives. Semin.
Cell Dev. Biol. 2021, 115, 37–44. [CrossRef]
240. Mazur, A.; Maier, J.A.; Rock, E.; Gueux, E.; Nowacki,W.; Rayssiguier, Y. Magnesium and the inflammatory response: Potential
physiopathological implications. Arch. Biochem. Biophys. 2007, 458, 48–56. [CrossRef]
241. Kramer, J.H.; Mak, I.T.; Phillips, T.M.; Weglicki, W.B. Dietary magnesium intake influences circulating pro-inflammatory
neuropeptide levels and loss of myocardial tolerance to postischemic stress. Exp. Biol. Med. 2003, 228, 665–673. [CrossRef]
[PubMed]
242. Maier, J.A.; Malpuech-Brugere, C.; Zimowska, W.; Rayssiguier, Y.; Mazur, A. Low magnesium promotes endothelial cell
dysfunction: Implications for atherosclerosis, inflammation and thrombosis. Biochim. Biophys Acta. 2004, 1689, 13–21. [CrossRef]
[PubMed]
243. Locatelli, L.; Fedele, G.; Castiglioni, S.; Maier, J.A. Magnesium Deficiency Induces Lipid Accumulation in Vascular Endothelial
Cells via Oxidative Stress-The Potential Contribution of EDF-1 and PPARgamma. Int. J. Mol. Sci. 2021, 22, 1050. [CrossRef]
[PubMed]
244. Stankovic, M.S.; Janjetovic, K.; Velimirovic, M.; Milenkovic, M.; Stojkovic, T.; Puskas, N.; Zaletel, I.; De Luka, S.R.; Jankovic, S.;
Stefanovic, S.; et al. Effects of IL-33/ST2 pathway in acute inflammation on tissue damage, antioxidative parameters, magnesium
concentration and cytokines profile. Exp. Mol. Pathol. 2016, 101, 31–37. [CrossRef] [PubMed]
245. Su, N.-Y.; Peng, T.-C.; Tsai, P.-S.; Huang, C.-J. Phosphoinositide 3-kinase/Akt pathway is involved in mediating the antiinflammation
effects of magnesium sulfate. J. Surg. Res. 2013, 185, 726–732. [CrossRef]
246. Lin, C.Y.; Tsai, P.S.; Hung, Y.C.; Huang, C.J. L-type calcium channels are involved in mediating the anti-inflammatory effects of
magnesium sulphate. Br. J. Anaesth. 2010, 104, 44–51. [CrossRef] [PubMed]
247. King, D.E.; Mainous, A.G., 3rd; Geesey, M.E.;Woolson, R.F. Dietary magnesium and C-reactive protein levels. J. Am. Coll. Nutr.
2005, 24, 166–171. [CrossRef]
248. Song, Y.; Li, T.Y.; van Dam, R.M.; Manson, J.E.; Hu, F.B. Magnesium intake and plasma concentrations of markers of systemic
in-flammation and endothelial dysfunction in women. Am. J. Clin. Nutr. 2007, 85, 1068–1074. [CrossRef]
249. Guerrero-Romero, F.; Bermudez-Pena, C.; Rodríguez-Morán, M. Severe hypomagnesemia and low-grade inflammation in
metabolic syndrome. Magnes. Res. 2011, 24, 45–53. [CrossRef]
250. Song, Y.; Ridker, P.M.; Manson, J.E.; Cook, N.R.; Buring, J.E.; Liu, S. Magnesium intake, C-reactive protein, and the prevalence of
met-abolic syndrome in middle-aged and older U.S. women. Diabetes Care 2005, 28, 1438–1444. [CrossRef]
251. Mazidi, M.; Kengne, A.P.; Mikhailidis, D.P.; Cicero, A.F.; Banach, M. Effects of selected dietary constituents on high-sensitivity
C-reactive protein levels in U.S. adults. Ann. Med. 2018, 50, 1–6. [CrossRef]
252. Konstari, S.; Sares-Jaske, L.; Heliovaara, M.; Rissanen, H.; Knekt, P.; Arokoski, J.; Sundvall, J.; Karppinen, J. Dietary magnesium
intake, serum high sensitivity C-reactive protein and the risk of incident knee osteoarthritis leading to hospitalization-A cohort
study of 4,953 Finns. PLoS ONE 2019, 14, e0214064. [CrossRef] [PubMed]
Nutrients 2024, 16, 496 28 of 28
253. Mazidi, M.; Rezaie, P.; Banach, M. Effect of magnesium supplements on serum C-reactive protein: A systematic review and
me-ta-analysis. Arch. Med. Sci. 2018, 14, 707–716. [CrossRef] [PubMed]
254. Veronese, N.; Pizzol, D.; Smith, L.; Dominguez, L.J.; Barbagallo, M. Effect of Magnesium Supplementation on Inflammatory
Param-eters: A Meta-Analysis of Randomized Controlled Trials. Nutrients 2022, 14, 679. [CrossRef] [PubMed]