Efectul sincronizarii proteinelor asupra forței musculare și a hipertrofiei
Sincronizarea proteinelor este o strategie alimentară populară concepută pentru a optimiza răspunsul adaptativ la exerciții fizice. Strategia implică consumul de proteine în și în jurul unei sesiuni de antrenament, de a facilita repararea și remodelarea musculară și prin urmare, de a îmbunătăți adaptările legate de forță și hipertrofie după exercițiu. În ciuda aparentei de plauzibilitate biologică a strategiei, totuși, eficacitatea sincronizarii proteinelor în studiile de antrenament cronic a fost hotărât mixt. Prin urmare, scopul acestei lucrări a fost de a efectua o metaregresie pe mai multe niveluri a studiilor controlate randomizate pentru a determina dacă sincronizarea proteinelor este o strategie viabilă pentru îmbunătățirea adaptărilor musculare post-exercitiu. Analiza fortei a cuprins 478 de subiecți și 96 de ES, încadrați în 41 de grupuri de tratament sau de control și 20 de studii. Analiza hipertrofiei a cuprins 525 de subiecți și 132 de ES, cu 47 de grupuri de tratament sau de control și 23 de studii. O analiză comună simplă a sincronizarii proteinelor fără controlul covariatelor a arătat un efect mic până la moderat asupra hipertrofiei musculare, fără niciun efect semnificativ asupra forței musculare. Cu toate acestea, în modelul complet de meta-regresie care controlează toate covariatele, nu s-au găsit diferențe semnificative între tratament și controlul forței sau hipertrofie. Modelul redus nu a fost semnificativ diferit de modelul complet pentru forța sau hipertrofie. În ceea ce privește hipertrofia, aportul total de proteine a fost cel mai puternic predictor al magnitudinii ES. Aceste rezultate resping credința obișnuită că momentul aportului de proteine în și în jurul unei sesiuni de antrenament este esențial pentru adaptările musculare și indică faptul că consumul de proteine adecvate în combinație cu exercițiile de rezistență este factorul cheie pentru maximizarea acumularii de proteine musculare.
Este în general acceptat că proteinele ar trebui consumate chiar înainte și/sau imediat după o sesiune de antrenament pentru a profita la maximum de o fereastră anabolică limitată. Susținătorii strategiei susțin că, atunci când este executat corespunzător, aportul precis de proteine în perioada pre-antrenament poate stimula creșterea masei musculare fără grăsimi. Unii cercetători au susținut chiar ideea că momentul aportului alimentar poate avea un efect pozitiv mai mare asupra compoziției corpului decât consumul absolut zilnic de nutrienți.
O serie de studii susțin superioritatea sincronizarii proteinelor pentru stimularea creșterii sintezei acute a proteinelor în urma antrenamentului de rezistență în comparație cu placebo. Proteina este considerată a fi nutrientul critic necesar pentru optimizarea sintezei proteinelor după exercițiu. Aminoacizii esențiali, în special, sunt considerați responsabili în primul rând pentru îmbunătățirea acestui răspuns, cu o contribuție mică sau deloc observată din furnizarea de aminoacizi neesențiali. Borsheim și colab. a constatat că o doză de 6 g de aminoacizi esențiali (EAA) consumată imediat după exercițiu a produs o creștere de aproximativ două ori a echilibrului proteic net în comparație cu o doză comparabilă care conține un amestec aproximativ egal de aminoacizi esențiali și neesențiali, indicând o doză – relație de răspuns până la 6 g EAA. Cu toate acestea, creșterea aportului de EAA dincolo de această cantitate nu s-a dovedit a crește semnificativ sinteza proteinelor după exercițiu. Există dovezi limitate că carbohidrații au un efect aditiv asupra îmbunătățirii sintezei proteinelor musculare după exercițiu atunci când sunt combinați cu ingestia de aminoacizi, majoritatea studiilor nereușind să demonstreze un astfel de beneficiu.
În ciuda aparentei de plauzibilitate biologică a strategiei, eficacitatea sincronizarii proteinelor în studiile de antrenament cronic a fost hotărât mixt. În timp ce unele studii au arătat că consumul de proteine în perioada pre-antrenament favorizează creșterea forței musculare și/sau hipertrofia, altele nu au făcut-o. Într-o revizuire a literaturii, Aragon și Schoenfeld au concluzionat că există o lipsă de dovezi care să susțină o „fereastră de oportunitate anabolică” îngustă, prin care proteinele trebuie consumate în imediata apropiere a antrenamentului pentru a maximiza adaptările musculare. Cu toate acestea, aceste concluzii au fost cel puțin parțial o reflectare a problemelor metodologice din cercetarea actuală. O problemă în special este că studiile de până în prezent au folosit eșantion de dimensiuni mici. Astfel, este posibil ca concluziile nule să poată fi atribuite faptului că aceste studii sunt insuficiente, rezultând o eroare de tip II. În plus, diferiți factori de confuzie, inclusiv cantitatea de suplimente cu EAA, potrivirea aportului de proteine, statutul de antrenament și variațiile de vârstă și sex între studii fac dificilă tragerea de concluzii definitive pe această temă.
Astfel, prin creșterea puterii statistice și controlul variabilelor de confuzie, o meta-analiză poate ajuta la clarificarea dacă sincronizarea proteinei conferă beneficii potențiale în adaptările mușchilor scheletici post-exercițiu.
O meta-analiză recentă a Cermak și colab. a constatat că suplimentarea cu proteine, atunci când este combinată cu antrenament de rezistență, sporește creșterea forței și a masei musculare atât la adulții tineri, cât și la cei în vârstă. Cu toate acestea, această analiză nu a investigat în mod specific sincronizarea proteinei în sine. Mai degrabă, criteriile de includere au cuprins toate studiile de antrenament de rezistență în care cel puțin un grup a consumat un supliment de proteine sau a modificat o dietă, mai bogată în proteine. Prin urmare, scopul acestei lucrări este de a efectua o meta-analiză pentru a determina dacă sincronizarea proteinei în apropierea sesiunii de antrenament de rezistență este o strategie viabilă pentru îmbunătățirea adaptărilor musculare.
Metodologie/ Criterii de includere
Doar studiile randomizate controlate sau studiile randomizate încrucișate care implică sincronizarea proteinelor au fost luate în considerare pentru includere. Timpul pentru proteine a fost definit aici ca un studiu în care cel puțin un grup de tratament a consumat minimum 6 g de aminoacizi esențiali (EAA) ≤ 1 oră înainte și/sau post-exercițiu de rezistență și cel puțin un grup de control nu a consumat proteine < 2 ore înainte și/sau după exercițiul de rezistență. Protocoalele de antrenament de rezistență trebuiau să se întindă pe cel puțin 6 săptămâni și să măsoare direct forța musculară dinamică și/sau hipertrofia ca o variabilă de rezultat primară. Nu au existat restricții privind vârsta, sexul, statutul de antrenament sau potrivirea aportului de proteine, dar aceste variabile au fost controlate prin analiza de subgrup folosind meta-regresia.
Strategia de căutare
Pentru a efectua această revizuire, au fost efectuate căutări în literatura de specialitate în bazele de date PubMed și Google Scholar pentru toate perioadele de timp până în martie 2019. Au fost utilizate combinații ale următoarelor cuvinte cheie ca termeni de căutare: „nutrient timing”; „suplimente de proteine”; „suplimente nutriționale”; „supliment proteic”; „supliment nutritional”; „exercițiu de rezistență”; „antrenament de rezistenta”; „antrenamentul de forță”. În conformitate cu metodele prezentate de Greenhalgh și Peacock, listele de referințe ale articolelor preluate în căutare au fost apoi verificate pentru orice articole suplimentare care au avut relevanță pentru subiect. Rezumatele de la conferințe, recenzii și disertații/teze nepublicate au fost excluse din analiză. Un total de 34 de studii au fost identificate ca potențial relevante pentru această revizuire. Pentru a reduce potențialul selecției, fiecare dintre aceste studii a fost examinat în mod independent de doi dintre investigatori (BJS și AAA) și s-a luat o decizie reciprocă cu privire la îndeplinirea sau nu a criteriilor de includere de bază. Calitatea studiului a fost apoi evaluată cu scala PEDro, care s-a dovedit a fi o măsură validă a calității metodologice a RCT-urilor și are o fiabilitate acceptabilă între evaluatori.
Doar acele studii cu scor ≥5 pe scala PEDro – o valoare considerată a fi de calitate moderată până la înaltă – au fost acceptate pentru analiză. Orice dezacorduri între examinatori au fost soluționate prin consens și/sau consultare cu cel de-al treilea investigator. Pre-screeningul inițial a dezvăluit 29 de studii potențiale care au investigat sincronizarea nutrienților în ceea ce privește adaptările musculare. Dintre aceste studii, 3 nu au îndeplinit criteriile pentru un aport suficient de proteine suplimentare, iar într-un altul timpul de consum a fost în afara intervalului definit după antrenament. Astfel, un total de 25 de studii au fost considerate în cele din urmă potrivite pentru includere. Două dintre studii au fost ulterior excluse deoarece nu conțineau date suficiente pentru calcularea mărimii efectului și încercările de a obține aceste informații de la autori au fost eșuate, lăsând un total de 23 de studii adecvate pentru analiză. Scorul mediu PEDro al acestor studii a fost de 8,7, indicând un nivel general ridicat de calitate metodologică.
Codificarea studiilor
Studiile au fost citite și codificate individual de doi dintre investigatori (BJS și AAA) pentru următoarele variabile: Informații descriptive ale subiecților pe grupe, inclusiv sex, masa corporală, statutul de antrenament (subiecții antrenați au fost definiți ca cei cu experiență de cel puțin un an de antrenament cu rezistență), vârsta și vârsta subiectului stratificat (clasificat fie ca tineri [18–49 de ani] sau vârstnici [50+ ani]; dacă aportul zilnic total de proteine între grupuri a fost sau nu corelat; dacă studiul a fost un RCT sau un design încrucișat; numărul de subiecți din fiecare grup (clasificat ca fiind simplu, dublu sau neorb) tipul de măsurare a hipertrofiei (RMN, CT, ecografie, biopsie etc.) și regiunea/mușchiul corpului măsurat; măsurarea masei corporale slabe (adică DXA, cântărire hidrostatică, etc.), dacă este cazul, și exercițiile de forță utilizate pentru testare, dacă este cazul, codarea a fost verificată încrucișată și orice discrepanță a fost rezolvată de comun acord. Pentru a evalua deviația potențială a codificatorului, 5 studii au fost selectate aleatoriu pentru recodificare, așa cum este descris de Cooper și colab. Acordul pe caz a fost determinat prin împărțirea numărului de variabile codificate la fel la numărul total de variabile. Acceptarea a necesitat un acord mediu de 0,90.
Calculul mărimii efectului
Pentru fiecare rezultat de putere sau hipertrofie 1-RM, a fost calculată o mărime a efectului (ES) ca modificare pretest-posttest, împărțită la abaterea standard pretest (SD). Varianta de eșantionare pentru fiecare ES a fost estimată conform lui Morris și DeShon. Calculul varianței de eșantionare a necesitat o estimare a populației ES și corelația pretest-posttest pentru fiecare ES individual. ES populației a fost estimată prin calcularea ES medie pentru toate studiile și grupurile de tratament. Corelația pretest-posttest a fost calculată folosind următoarea formulă:
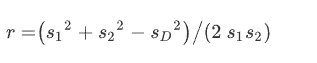
Unde s1 și s2 sunt SD pentru mediile pre- și, respectiv, posttest, iar sD este SD-ul scorurilor diferențelor. Acolo unde s2 nu a fost raportat, s1 a fost folosit în locul său. Acolo unde DS nu a fost raportată, a fost estimată folosind următoarea formulă:
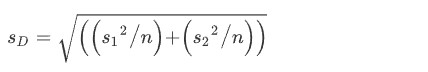
Analize statistice
Meta-analizele au fost efectuate folosind modele ierarhice liniare mixte, modelând variația dintre studii ca efect aleatoriu, variația dintre grupurile de tratament și de control ca efect aleator în studii și predictorii la nivel de grup ca efecte fixe. S-au presupus că variațiile în interiorul grupului sunt cunoscute. Observațiile au fost ponderate cu inversul varianței de eșantionare. A fost creat un model de interceptare, estimând ES medie ponderată pentru toate studiile și grupurile de tratament. În al doilea rând, a fost creat un model de bază care a inclus doar clasa grupului (tratament sau control) ca predictor. Apoi a fost creat un model complet cu următorii predictori: clasa grupului (tratament sau control), dacă grupurile au fost sau nu potrivite cu proteine, statutul de antrenament (experimentat sau începător), orbire (dublu, singur sau deloc), sex (masculin, feminin sau mixt), vârsta (tânăr sau bătrân), masa corporală în kg și durata studiului în săptămâni. Modelul complet a fost apoi redus prin eliminarea câte un predictor la un moment dat, începând cu cel mai nesemnificativ predictor. Modelul final a reprezentat modelul redus cu cel mai scăzut criteriu de corectare a informațiilor Akaike (AICC) și care nu a fost semnificativ diferit (P > 0,05) de modelul complet în comparație folosind un test al raportului de probabilitate (LRT). Parametrii modelului au fost estimați prin metoda probabilității maxime restricționate (REML); o excepție a fost în timpul procesului de reducere a modelului, în care parametrii au fost estimați prin metoda probabilității maxime (ML), deoarece LRT-urile nu pot fi utilizate pentru a compara modele cu estimările REML.
Numitorul df pentru testele statistice și CI au fost calculate conform Berkey și colab.. Variabila de clasificare tratament/control nu a fost eliminată în timpul procesului de reducere a modelului.
Au fost efectuate analize separate pentru forță și hipertrofie. ES pentru ambele modificări ale zonei transversale (CSA) și FFM au fost reunite în analiza hipertrofiei. Cu toate acestea, deoarece exercițiul de rezistență este asociat cu acumularea de țesut non-muscular, au fost efectuate subanalize separate privind CSA și FFM. Deoarece efectul sincronizarii proteinelor ar putea interacționa cu dacă grupurile de tratament și de control au fost potrivite pentru aportul total de proteine, a fost creat un model suplimentar care a inclus un termen de interacțiune între variabila de clasificare tratament/control și variabila de potrivire a proteinei. De asemenea, deoarece efectul sincronizarii proteinelor poate varia în funcție de experiența de antrenament, a fost creat un model care a inclus un termen de interacțiune între variabila de clasificare tratament/control și variabila de status de antrenament. Ajustarea pentru comparații multiple post-hoc a fost efectuată folosind o procedură bazată pe simulare. Toate analizele au fost efectuate folosind SAS Enterprise Guide Versiunea 4.2 (Cary, NC). Efectele au fost considerate semnificative la P ≤ 0,05. Datele sunt raportate ca medii (±SE) și IC 95%.
Rezultate
Caracteristicile studiului
Analiza fortei a cuprins 478 de subiecți și 96 de ES, încadrați în 41 de grupuri de tratament sau de control și 20 de studii. Forța medie ponderată ES în toate studiile și grupurile a fost de 1,39 ± 0,24 (IC: 0,88, 1,90). Analiza hipertrofiei a cuprins 525 de subiecți și 132 de ES, cu 47 de grupuri de tratament sau de control și 23 de studii. Media ponderată a hipertrofiei ES în toate studiile și grupurile a fost 0,47 ± 0,08 (IC: 0,31, 0,63).
Model de bază
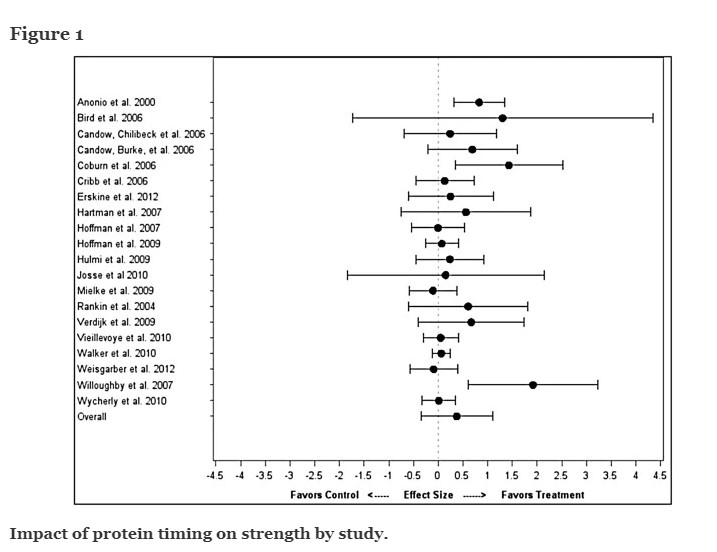
Nu a existat nicio diferență semnificativă între tratament și control pentru forță (diferență = 0,38 ± 0,36; IC: -0,34, 1,10; P = 0,30). Diferența medie de intensitate ES între tratament și control pentru fiecare studiu individual, împreună cu diferența medie ponderată globală din toate studiile, este prezentată în Figura 1. Pentru hipertrofie, ES medie a fost semnificativ mai mare în tratament în comparație cu controlul (diferență = = 0,24 ± 0,10 CI: 0,04, 0,44 P = 0,02). Diferența medie de hipertrofie ES între tratament și control pentru fiecare studiu individual, împreună cu diferența medie ponderată globală din toate studiile, este prezentată în Figura 2.
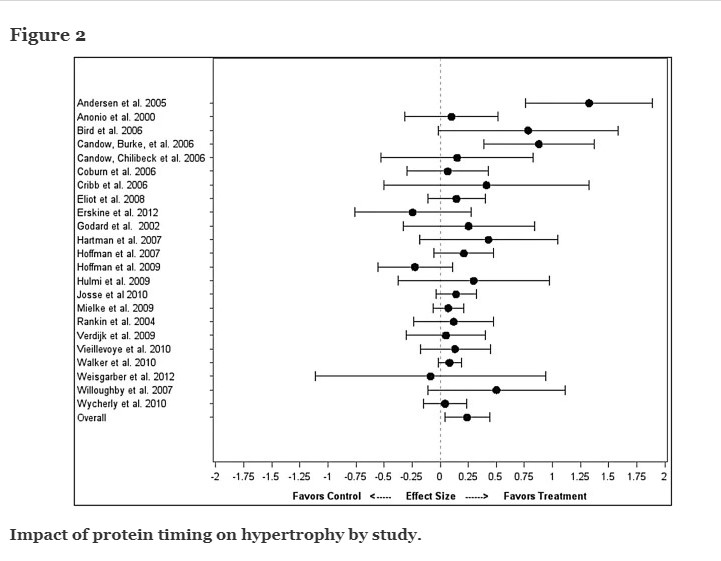
Model complet
În modelul complet de metaregresie care controlează toate covariatele, nu a existat nicio diferență semnificativă între tratament și control pentru forță (diferență = 0,28 ± 0,40; IC: -0,52, 1,07; P = 0,49) sau hipertrofie (diferență = 0,16 0,16 0,16 . IC: -0,07, 0,38 P = 0,18).
Model redus: rezistenta
După procedura de reducere a modelului, doar statutul de antrenament a rămas ca covariabila semnificativa. Modelul redus nu a fost semnificativ diferit de modelul complet (P = 0,73). În modelul redus, nu a existat nicio diferență semnificativă între tratament și control (diferență = 0,39 ± 0,36; IC: -0,34, 1,11; P = 0,29). ES mediu pentru control a fost 0,93 ± 0,31 (IC: 0,32, 1,54). ES mediu pentru tratament a fost 1,31 ± 0,30 (IC: 0,71, 1,92).
Model redus: hipertrofie
După procedura de reducere a modelului, aportul total de proteine, durata studiului au rămas ca covariabile semnificative. Modelul redus nu a fost semnificativ diferit de modelul complet (P = 0,87). În modelul redus, nu a existat nicio diferență semnificativă între tratament și control (diferență = 0,14 ± 0,11; CI: -0,07, 0,35; P = 0,20). ES mediu pentru control a fost 0,36 ± 0,09 (IC: 0,18, 0,53). ES mediu pentru tratament a fost 0,49 ± 0,08 (IC: 0,33, 0,66). Aportul total de proteine (în g/kg) a fost cel mai puternic predictor al magnitudinii ES (estimare = 0,41 ± 0,14; CI: 0,14, 0,69; P = 0,004).
Pentru a confirma faptul că aportul total de proteine a fost mediator variabil în relația dintre sincronizarea proteinei și hipertrofie, a fost creat un model cu doar aportul total de proteine ca covariabilă. Diferența dintre tratament și control nu a fost semnificativă (diferență = 0,14 ± 0,11; IC: -0,07, 0,35; P = 0,19). Aportul total de proteine a fost un predictor semnificativ al magnitudinii ES (estimare = 0,39 ± 0,15; CI: 0,08, 0,69; P = 0,01). Figura 3 arată ES-urile ajustate în funcție de aportul total de proteine pentru fiecare studiu, precum și efectul general al meta-regresiei cu doar aportul total de proteine ca covariabilă.
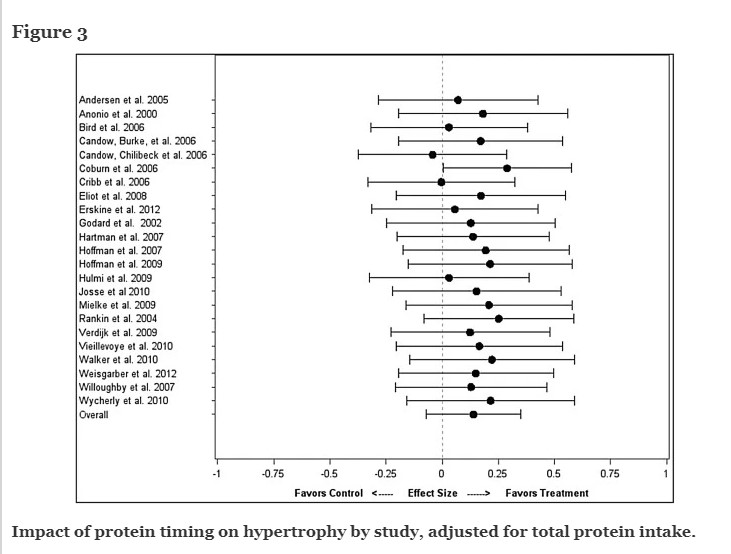
Interacțiuni
Pentru forță, interacțiunea dintre tratament și starea de antrenament a fost aproape semnificativă (P = 0,051), dar comparațiile post-hoc între tratament și control în cadrul fiecărei clasificări a stării de antrenament nu au fost semnificative (P = 0,47 ajustat pentru diferența în cadrul grupurilor neexperimentate și ajustat P = 0,99 pentru diferența în cadrul grupurilor cu experiență). Nu a existat nicio interacțiune semnificativă între tratament și dacă grupurile au fost potrivite cu proteine (P = 0,43). Pentru hipertrofie, nu a existat o interacțiune semnificativă între tratament și starea de antrenament (P = 0,63) sau tratament și potrivirea proteinelor (P = 0,59).
Subanalize de hipertrofie
Separarea analizei hipertrofiei în CSA sau FFM nu a modificat semnificativ rezultatele. Pentru FFM, nu a existat o diferență semnificativă între tratament și control (diferență = 0,08 ± 0,07; IC: -0,07, 0,24; P = 0,27). Aportul total de proteine a rămas un predictor puternic al magnitudinii ES (estimare = 0,39 ± 0,07; CI: 0,25, 0,53; P < 0,001). Pentru CSA, nu a existat o diferență semnificativă între tratament și control (diferență = 0,14 ± 0,16; IC: -0,17, 0,46; P = 0,37). Aportul total de proteine a fost din nou un predictor al magnitudinii ES (estimare = 0,55 ± 0,24; CI: 0,08, 1,20; P = 0,02).
Discuţie
Aceasta este prima meta-analiză care investighează în mod direct efectele sincronizarii proteinelor asupra forței și adaptărilor hipertrofice în urma protocoalelor de antrenament de rezistență pe termen lung. Studiul a produs câteva descoperiri noi. O analiză comună simplă a timpului proteinei fără controlul covariatelor a arătat un efect semnificativ asupra hipertrofiei musculare (ES = 0,24 ± 0,10) fără niciun efect semnificativ asupra forței musculare. În general, este acceptat că o mărime a efectului de 0,2 este mică, 0,5 este moderată și 0,8 și mai mult este mare, ceea ce indică faptul că efectul sincronizarii proteinelor asupra creșterii masei corporale slabe a fost mic spre moderat. Cu toate acestea, o analiză de regresie extinsă a constatat că orice efecte pozitive asociate cu sincronizarea proteinei asupra acumularii proteinelor musculare au dispărut după controlul covariatelor. Mai mult, sub-analiza a arătat discrepanțe în aportul total de proteine, au explicat majoritatea diferențelor hipertrofice observate în studiile de sincronizare. Atunci când sunt luate împreună, aceste rezultate ar părea să respingă credința comună că momentul aportului de proteine în perioada imediat pre- și post-antrenament este esențial pentru adaptările musculare.
Beneficiile hipertrofice percepute în studiile de sincronizare par să fie rezultatul unui consum crescut de proteine, spre deosebire de factori temporali. În modelul nostru redus, cantitatea de proteine consumată a fost asociată în mare măsură și semnificativ cu câștiguri hipertrofice. De fapt, modelul redus a arătat că aportul total de proteine a fost de departe cel mai important predictor al hipertrofiei ES, cu o creștere de ~ 0,2 a ES observată pentru fiecare creștere cu 0,5 g/kg a ingestiei de proteine. Deși există, fără îndoială, un prag superior pentru această corelație, aceste constatări subliniază importanța consumului de cantități mai mari de proteine atunci când scopul este de a maximiza creșterile masei musculare induse de efort. În schimb, aportul total de proteine nu a avut un impact asupra rezultatelor forței și în cele din urmă a fost luat în considerare în timpul procesului de reducere a procesului.
Doza dietetică recomandată (DZR) pentru proteine este de 0,8 g/kg/zi. Cu toate acestea, aceste valori se bazează pe nevoile indivizilor sedentari și sunt menite să reprezinte un nivel de aport necesar pentru a înlocui pierderile și prin urmare, a preveni deficiența; ele nu reflectă cerințele indivizilor cu antrenament dur care caută să crească masa slabă. Studiile arată de fapt că cei care participă la programe intensive de antrenament de rezistență au nevoie de mult mai multe proteine pentru a rămâne într-un echilibru de azot nenegativ. Pozițiile de la mai multe organisme științifice estimează că aceste cerințe sunt aproximativ duble față de RDA. Niveluri mai ridicate de consum de proteine par a fi deosebit de importante în primele etape ale antrenamentului intens de rezistență. Lemon et al. a arătat că culturiștii începători aveau nevoie de un aport de proteine de 1,6-1,7 g/kg/zi pentru a rămâne într-un echilibru de azot nenegativ. Nevoia crescută de proteine la subiecții începători a fost atribuită modificărilor ratei de sinteză a proteinelor musculare și nevoii de a menține o masă slabă mai mare decât utilizarea crescută a energiei. Există unele dovezi că necesarul de proteine scade de fapt ușor la aproximativ 1,4 g/kg/zi la persoanele bine antrenate din cauza unei eficiențe mai mari în utilizarea azotului alimentar, deși această ipoteză necesită un studiu suplimentar.
Aportul mediu de proteine pentru martori în studiile fără pereche a fost de 1,33 g/kg/zi, în timp ce aportul mediu pentru tratament a fost de 1,66 g/kg/zi. Deoarece o preponderență a acestor studii a implicat subiecți neantrenați, pare probabil că o majoritate a oricăror câștiguri în masa musculară s-ar fi datorat consumului mai mare de proteine de către grupul de tratament. Aceste constatări sunt în concordanță cu cele ale Cermak și colab. , care a descoperit că doar suplimentarea cu proteine a produs adaptări benefice atunci când este combinată cu antrenamentul de rezistență. Studiul lui Cermak et al. nu a evaluat, totuși, niciun efect în ceea ce privește momentul aportului, astfel încât rezultatele noastre sprijină în mod direct teoria conform căreia îndeplinirea cerințelor de proteine țintă este esențială în ceea ce privește acumularea de proteine musculare indusă de efort; aportul imediat de proteine din dietă înainte și/sau după antrenament ar părea, în cel mai bun caz, a fi o considerație minoră. Descoperirile susțin, de asemenea, recomandările anterioare conform cărora un consum de proteine de cel puțin 1,6 g/kg/zi este necesar pentru a maximiza acumularea de proteine musculare la persoanele implicate în programele de antrenament de rezistență.
Pentru studiile comparate, aportul de proteine a fost în medie de 1,91 g/kg/zi față de 1,81 g/kg/zi pentru tratament și respectiv, martori. Acest nivel de aport pentru ambele grupuri îndeplinește sau depășește liniile directoare sugerate, permițând o evaluare corectă a efectelor temporale. Cu toate acestea, doar 3 studii care au folosit aportul de proteine potrivite au îndeplinit criteriile de includere pentru această analiză. Interesant este că 2 din cele 3 nu au arătat niciun beneficiu din cronometrare. Mai mult, un alt studiu comparat a constatat de fapt creșteri semnificativ mai mari ale forței și masei corporale slabe de la o doză de proteine împărțită în timp (adică dimineața și seara) în comparație cu aceeași doză furnizată în timpul sesiunii de antrenament de rezistență. Cu toate acestea, acest studiu a trebuit să fie exclus din analiza noastră, deoarece nu avea date adecvate pentru a calcula un ES. Rezultatele sumare ale studiilor cu proteine corelate sugerează că momentul este de prisos, cu condiția ca proteinele adecvate să fie ingerate, deși numărul mic de studii limitează capacitatea de a trage concluzii ferme în acest sens.
Această meta-analiză a avut o serie de puncte forte. În primul rând, calitatea studiilor evaluate a fost ridicată, cu un scor mediu PEDro de 8,7. De asemenea, eșantionul a fost relativ mare (23 de studii cuprinzând 478 de subiecți pentru rezultatele de forță și 525 de subiecți pentru rezultatele hipertrofiei), oferind o putere statistică bună. În plus, au fost utilizate criterii stricte de includere/excludere pentru a reduce potențialul de părtinire. Combinați, acești factori oferă o bună încredere în capacitatea de a trage concluzii relevante din constatări.
Un alt punct forte a fost aderarea rigidă la practicile de codificare adecvate. Codarea a fost efectuată de doi dintre investigatori (BJS și AAA) și apoi verificată încrucișat între codori. Deviația codificatorului a fost apoi evaluată prin selecția aleatorie a studiilor pentru a asigura în continuare coerența datelor. În cele din urmă și important, studiul a beneficiat de utilizarea meta-regresiunii. Acest lucru a oferit capacitatea de a examina impactul variabilelor moderatoare asupra mărimii efectului și de a explica eterogenitatea dintre studii. Deși constatările inițiale au indicat un avantaj conferit de sincronizarea proteinelor, meta-regresia a arătat că rezultatele au fost confundate de discrepanțe în consum. Acest lucru a condus în cele din urmă la determinarea că aportul total de proteine, mai degrabă decât factorii temporali, a explicat orice beneficii percepute.
Există mai multe limitări ale acestei analize care ar trebui luate în considerare atunci când se trag concluzii bazate pe dovezi. În primul rând, momentul meselor în grupurile de control a variat semnificativ de la studiu la studiu. Unii au furnizat proteine imediat după 2 ore după antrenament, în timp ce alții au întârziat consumul cu multe ore. O revizuire recentă a lui Aragon și Schoenfeld a postulat că fereastra de oportunitate anabolică poate fi de până la 4-6 ore în jurul unei sesiuni de antrenament, în funcție de dimensiunea și compoziția mesei. Deoarece momentul aportului la controale au fost tratați în mod similar în această meta-analiză, este dificil de determinat dacă există o fereastră anabolică clară pentru consumul de proteine dincolo de care suferă adaptările musculare.
În al doilea rând, majoritatea studiilor au evaluat subiecți care nu aveau experiență în exercițiul de rezistență. Este bine stabilit că indivizii înalt pregătiți răspund diferit la cerințele antrenamentului de rezistență în comparație cu cei cărora le lipsește experiența de antrenament. În parte, acest lucru este atribuit unui „efect de plafon” prin care creșterea masei musculare devine progresiv mai dificilă pe măsură ce un cursant se apropie de potențialul său hipertrofic genetic. Există, de asemenea, dovezi care arată că exercițiul de rezistență reglat atenuează semnalizarea anabolică intracelulară la rozătoare și la oameni, diminuând probabil răspunsul hipertrofic. Subanaliza noastră nu a reușit să arate un efect de interacțiune între starea antrenamentului de rezistență și sincronizarea proteinelor fie pentru forță, fie pentru hipertrofie. Cu toate acestea, puterea statistică a fost scăzută deoarece doar 4 studii care au folosit subiecți instruiți au îndeplinit criteriile de includere. Cercetările viitoare ar trebui, prin urmare, să se concentreze pe determinarea efectelor sincronizarii proteinelor asupra adaptărilor musculare la cei cu cel puțin 1 an sau mai mult de experiență regulată, consecventă de antrenament de rezistență.
În al treilea rând, într-un efort de a menține dimensiunea eșantionului suficient de mare, am combinat datele CSA și FFM pentru a determina hipertrofia ES. FFM este frecvent utilizat ca un proxy pentru hipertrofie, deoarece se presupune, în general, că marea majoritate a câștigurilor în masă fără grăsimi din antrenamentul de rezistență sunt de natură miocelulară. Cu toate acestea, exercițiul de rezistență este asociat și cu acumularea de țesut non-muscular (adică os, țesut conjunctiv etc.). Pentru a ține seama de eventualele discrepanțe în această privință, am efectuat subanalize numai pe CSA și FFM, iar rezultatele în esență nu s-au schimbat. Pentru FFM, diferența dintre tratament și control nu a fost semnificativă (P = 0,27), cu o diferență ES de -0,08. Aportul de proteine a fost din nou foarte semnificativ, cu un impact ES de ~ 0,2 la fiecare 1 g/kg/zi. Pentru CSA, diferența dintre tratament și control nu a fost semnificativă (P = 0,37), cu o diferență ES de -0,14. Aportul de proteine a fost din nou semnificativ (P = 0,02) cu un impact ES de ~0,33 la fiecare 0,5 g/kg.
În cele din urmă și important, au existat puține studii de sincronizare care au încercat să egaleze aportul de proteine. După cum sa discutat anterior, rezultatele noastre arată că aportul total de proteine este puternic și pozitiv asociat cu câștigurile post-exercițiu în hipertrofia musculară. Studiile viitoare ar trebui să încerce să controleze această variabilă, astfel încât efectele reale ale calendarului, dacă există, să poată fi evaluate cu acuratețe.
Aplicații practice
În concluzie, dovezile actuale nu par să susțină afirmația că consumul imediat (≤ 1 oră) de proteine înainte și/sau după antrenament îmbunătățește în mod semnificativ adaptările legate de forță sau hipertrofie la exercițiile de rezistență. Rezultatele acestei meta-analize indică faptul că, dacă există de fapt o fereastră de oportunitate anabolizantă pre/post-antrenament, fereastra pentru consumul de proteine ar părea a fi mai mare de o oră înainte și după o sesiune de antrenament de rezistență. Orice efecte pozitive observate în studiile de sincronizare s-au dovedit a fi datorate unui aport crescut de proteine, mai degrabă decât aspectelor temporale ale consumului, dar lipsa unor studii potrivite face dificilă tragerea de concluzii ferme în acest sens. Faptul că consumul de proteine la subiecții fără suplimente a fost sub aportul recomandat în general pentru cei implicați în antrenamentul de rezistență, dă credință acestei descoperiri. Deoarece cauzalitatea nu poate fi extrasă direct din analiza noastră, totuși, trebuie să recunoaștem posibilitatea ca sincronizarea proteinei să fi fost de fapt responsabilă pentru producerea unui efect pozitiv și că creșterea asociată a aportului de proteine este pur și simplu coincidență. Cercetările viitoare ar trebui să urmărească controlul aportului de proteine, astfel încât valoarea reală în ceea ce privește sincronizarea nutrienților să poată fi evaluată în mod corespunzător. Ar trebui să se acorde o atenție deosebită efectuării acestor studii cu subiecți bine pregătiți pentru a determina mai bine dacă experiența antrenamentului de rezistență joacă un rol în răspuns.
By. Bitanu-Alexandru Sebastian-Alin
Referinte:
1.Phillips SM, Van Loon LJ: Dietary protein for athletes: from requirements to optimum adaptation. J Sports Sci. 2011, 29 ((Suppl 1)): S29-38.
2. Kerksick C, Harvey T, Stout J, Campbell B, Wilborn C, Kreider R: International society of sports nutrition position stand: nutrient timing. J Int Soc Sports Nutr. 2008 Oct 3, 5: 17-
3 .Lemon PW, Berardi JM, Noreen EE: The role of protein and amino acid supplements in the athlete’s diet: does type or timing of ingestion matter?. Curr Sports Med Rep. 2002 Aug, 1 (4): 214-221.
4 .Ivy J, Portman R: Nutrient timing: The future of sports nutrition. 2004, North Bergen, NJ: Basic Health Publications
5. Candow DG, Chilibeck PD: Timing of creatine or protein supplementation and resistance training in the elderly. Appl Physiol Nutr Metab. 2008 Feb, 33 (1): 184-190.
6. Tipton KD, Elliott TA, Cree MG, Wolf SE, Sanford AP, Wolfe RR: Ingestion of casein and whey proteins result in muscle anabolism after resistance exercise. Med Sci Sports Exerc. 2004 Dec, 36 (12): 2073-2081.
7. Rasmussen BB, Tipton KD, Miller SL, Wolf SE, Wolfe RR: An oral essential amino acid-carbohydrate supplement enhances muscle protein anabolism after resistance exercise. J Appl Physiol. 2000 Feb, 88 (2): 386-392.
8.Tipton KD, Elliott TA, Ferrando AA, Aarsland AA, Wolfe RR: Stimulation of muscle anabolism by resistance exercise and ingestion of leucine plus protein. Appl Physiol Nutr Metab. 2009 Apr, 34 (2): 151-161.
9.Tipton KD, Ferrando AA, Phillips SM, Doyle D, Wolfe RR: Postexercise net protein synthesis in human muscle from orally administered amino acids. Am J Physiol. 1999 Apr, 276 (4 Pt 1): E628-E634.
10.Borsheim E, Tipton KD, Wolf SE, Wolfe RR: Essential amino acids and muscle protein recovery from resistance exercise. Am J Physiol Endocrinol Metab. 2002 Oct, 283 (4): E648-E657.
11.Tipton KD, Gurkin BE, Matin S, Wolfe RR: Nonessential amino acids are not necessary to stimulate net muscle protein synthesis in healthy volunteers. J Nutr Biochem. 1999 Feb, 10 (2): 89-95.
12.Miller SL, Tipton KD, Chinkes DL, Wolf SE, Wolfe RR: Independent and combined effects of amino acids and glucose after resistance exercise. Med Sci Sports Exerc. 2003 Mar, 35 (3): 449-455.
13 .Koopman R, Beelen M, Stellingwerff T, Pennings B, Saris WH, Kies AK: Coingestion of carbohydrate with protein does not further augment postexercise muscle protein synthesis. Am J Physiol Endocrinol Metab. 2007 Sep, 293 (3): E833-E842.
14.Staples AW, Burd NA, West DW, Currie KD, Atherton PJ, Moore DR: Carbohydrate does not augment exercise-induced protein accretion versus protein alone. Med Sci Sports Exerc. 2011 Jul, 43 (7): 1154-1161.
15.Glynn EL, Fry CS, Timmerman KL, Drummond MJ, Volpi E, Rasmussen BB: Addition of carbohydrate or alanine to an essential amino acid mixture does not enhance human skeletal muscle protein anabolism. J Nutr. 2013 Mar, 143 (3): 307-314.
16.Cribb PJ, Hayes A: Effects of supplement timing and resistance exercise on skeletal muscle hypertrophy. Med Sci Sports Exerc. 2006 Nov, 38 (11): 1918-1925.
17.Willoughby DS, Stout JR, Wilborn CD: Effects of resistance training and protein plus amino acid supplementation on muscle anabolism, mass, and strength. Amino Acids. 2007, 32 (4): 467-477.
18.Hulmi JJ, Kovanen V, Selanne H, Kraemer WJ, Hakkinen K, Mero AA: Acute and long-term effects of resistance exercise with or without protein ingestion on muscle hypertrophy and gene expression. Amino Acids. 2009 Jul, 37 (2): 297-308.
19.Burk A, Timpmann S, Medijainen L, Vahi M, Oopik V: Time-divided ingestion pattern of casein-based protein supplement stimulates an increase in fat-free body mass during resistance training in young untrained men. Nutr Res. 2009 Jun, 29 (6): 405-413.
20.Hoffman JR, Ratamess NA, Tranchina CP, Rashti SL, Kang J, Faigenbaum AD: Effect of protein-supplement timing on strength, power, and body-composition changes in resistance-trained men. Int J Sport Nutr Exerc Metab. 2009 Apr, 19 (2): 172-185.
21.Verdijk LB, Jonkers RA, Gleeson BG, Beelen M, Meijer K, Savelberg HH: Protein supplementation before and after exercise does not further augment skeletal muscle hypertrophy after resistance training in elderly men. Am J Clin Nutr. 2009 Feb, 89
22.Wycherley TP, Noakes M, Clifton PM, Cleanthous X, Keogh JB, Brinkworth GD: Timing of protein ingestion relative to resistance exercise training does not influence body composition, energy expenditure, glycaemic control or cardiometabolic risk factors in a hypocaloric, high protein diet in patients with type 2 diabetes. Diab Obes Metab. 2010 Dec, 12 (12): 1097-1105.
23.Aragon AA, Schoenfeld BJ: Nutrient timing revisited: is there a post-exercise anabolic window?. J Int Soc Sports Nutr. 2013 Jan 29, 10 (1): 10-15. 5,2783
24.Cermak NM, Res PT, de Groot LC, Saris WH, van Loon LJ: Protein supplementation augments the adaptive response of skeletal muscle to resistance-type exercise training: a meta-analysis. Am J Clin Nutr. 2012 Dec, 96 (6): 1454-1464.
25.Greenhalgh T, Peacock R: Effectiveness and efficiency of search methods in systematic reviews of complex evidence: audit of primary sources. BMJ. 2005 Nov 5, 331 (7524): 1064-1065.
26.Elkins MR, Herbert RD, Moseley AM, Sherrington C, Maher C: Rating the quality of trials in systematic reviews of physical therapy interventions. Cardiopulm Phys Ther J. 2010 Sep, 21 (3): 20-26.
27.Moseley AM, Herbert RD, Sherrington C, Maher CG: Evidence for physiotherapy practice: a survey of the physiotherapy evidence database (PEDro). Aust J Physiother. 2002, 48 (1): 43-49.
28.Esmarck B, Andersen JL, Olsen S, Richter EA, Mizuno M, Kjaer M: Timing of postexercise protein intake is important for muscle hypertrophy with resistance training in elderly humans. J Physiol. 2001 Aug 15, 535 (Pt 1): 301-311.
29.Holm L, Olesen JL, Matsumoto K, Doi T, Mizuno M, Alsted TJ: Protein-containing nutrient supplementation following strength training enhances the effect on muscle mass, strength, and bone formation in postmenopausal women. J Appl Physiol. 2008 Jul, 105 (1): 274-281.
30.White KM, Bauer SJ, Hartz KK, Baldridge M: Changes in body composition with yogurt consumption during resistance training in women. Int J Sport Nutr Exerc Metab. 2009 Feb, 19 (1): 18-33.
31.Kerksick CM, Rasmussen CJ, Lancaster SL, Magu B, Smith P, Melton C: The effects of protein and amino acid supplementation on performance and training adaptations during ten weeks of resistance training. J Strength Cond Res. 2006 Aug, 20 (3): 643-653.
32.Bemben MG, Witten MS, Carter JM, Eliot KA, Knehans AW, Bemben DA: The effects of supplementation with creatine and protein on muscle strength following a traditional resistance training program in middle-aged and older men. J Nutr Health Aging. 2010 Feb, 14 (2): 155-159.
33.Antonio J, Sanders MS, Ehler LA, Uelmen J, Raether JB, Stout JR: Effects of exercise training and amino-acid supplementation on body composition and physical performance in untrained women. Nutrition. 2000 Nov-Dec, 16 (11-12): 1043-1046.
34.Godard MP, Williamson DL, Trappe SW: Oral amino-acid provision does not affect muscle strength or size gains in older men. Med Sci Sports Exerc. 2002 Jul, 34 (7): 1126-1131.
35.Rankin JW, Goldman LP, Puglisi MJ, Nickols-Richardson SM, Earthman CP, Gwazdauskas FC: Effect of post-exercise supplement consumption on adaptations to resistance training. J Am Coll Nutr. 2004 Aug, 23 (4): 322-330.
36.Andersen LL, Tufekovic G, Zebis MK, Crameri RM, Verlaan G, Kjaer M: The effect of resistance training combined with timed ingestion of protein on muscle fiber size and muscle strength. Metabolism. 2005 Feb, 54 (2): 151-156.
37.Bird SP, Tarpenning KM, Marino FE: Independent and combined effects of liquid carbohydrate/essential amino acid ingestion on hormonal and muscular adaptations following resistance training in untrained men. Eur J Appl Physiol. 2006 May, 97 (2): 225-238.
38.Coburn JW, Housh DJ, Housh TJ, Malek MH, Beck TW, Cramer JT: Effects of leucine and whey protein supplementation during eight weeks of unilateral resistance training. J Strength Cond Res. 2006 May, 20 (2): 284-291.
39.Candow DG, Burke NC, Smith-Palmer T, Burke DG: Effect of whey and soy protein supplementation combined with resistance training in young adults. Int J Sport Nutr Exerc Metab. 2006 Jun, 16 (3): 233-244.
40.Candow DG, Chilibeck PD, Facci M, Abeysekara S, Zello GA: Protein supplementation before and after resistance training in older men. Eur J Appl Physiol. 2006 Jul, 97 (5): 548-556.
41.Hartman JW, Tang JE, Wilkinson SB, Tarnopolsky MA, Lawrence RL, Fullerton AV: Consumption of fat-free fluid milk after resistance exercise promotes greater lean mass accretion than does consumption of soy or carbohydrate in young, novice, male weightlifters. Am J Clin Nutr. 2007 Aug, 86 (2): 373-381.
42.Hoffman JR, Ratamess NA, Kang J, Falvo MJ, Faigenbaum AD: Effects of protein supplementation on muscular performance and resting hormonal changes in college football players. J Sports Sci Med. 2007, 6: 85-92.
43.Eliot KA, Knehans AW, Bemben DA, Witten MS, Carter J, Bemben MG: The effects of creatine and whey protein supplementation on body composition in men aged 48 to 72 years during resistance training. J Nutr Health Aging. 2008 Mar, 12 (3): 208-212.
44.Mielke M, Housh TJ, Malek MH, Beck T, Schmidt RJ, Johnson GO: The effects of whey protein and leucine supplementation on strength, muscular endurance, and body composition during resistance training. J Exerc Physiol Online. 2009, 12: 39-50.
45.Josse AR, Tang JE, Tarnopolsky MA, Phillips SM: Body composition and strength changes in women with milk and resistance exercise. Med Sci Sports Exerc. 2010 Jun, 42 (6): 1122-1130.
46.Walker TB, Smith J, Herrera M, Lebegue B, Pinchak A, Fischer J: The influence of 8 weeks of whey-protein and leucine supplementation on physical and cognitive performance. Int J Sport Nutr Exerc Metab. 2010 Oct, 20 (5): 409-417.
47.Vieillevoye S, Poortmans JR, Duchateau J, Carpentier A: Effects of a combined essential amino acids/carbohydrate supplementation on muscle mass, architecture and maximal strength following heavy-load training. Eur J Appl Physiol. 2010 Oct, 110 (3): 479-488.
48.Erskine RM, Fletcher G, Hanson B, Folland JP: Whey protein does not enhance the adaptations to elbow flexor resistance training. Med Sci Sports Exerc. 2012 Sep, 44 (9): 1791-1800.
49.Weisgarber KD, Candow DG, Vogt ESM: Whey protein before and during resistance exercise has no effect on muscle mass and strength in untrained young adults. Int J Sport Nutr Exerc Metab. 2012 Jul, 4:
50.Cooper H, Hedges L, Valentine J: The handbook of research synthesis and meta-analysis. 2009, New York: Russell Sage Foundation, 2
51.Morris SB, DeShon RP: Combining effect size estimates in meta-analysis with repeated measures and independent-groups designs. Psychol Methods. 2002 Mar, 7 (1): 105-125.
52.Technical guide: Data analysis and interpretation [online]. [Internet].: National Center for Education Statistics. [updated 17 Dec. 2007,http://nces.ed.gov/programs/coe/guide/g3c.asp,
53.Hox JJ, de Leeuw ED, Hox JJ, de Leeuw ED: Multilevel models for meta-analysis. Reise SP, Duan N, editors. Multilevel modeling. Methodological advances, issues, and applications. Edited by: Duan N. 2003, Mahway, NJ: Lawrence Erlbaum Associates, 90-111.
54.Burnham KP, Anderson DR: Model selection and inference: A practical information-theoretic approach. 2002, New York: Springer-Verlag
55.Hurvich CM, Tsai CL: Regression and time series model selection in small samples. Biometrika. 1989, 76: 297-307.
56.Thompson SG, Sharp SJ: Explaining heterogeneity in meta-analysis: a comparison of methods. Stat Med. 1999 Oct 30, 18 (20): 2693-2708.
57.Berkey CS, Hoaglin DC, Mosteller F, Colditz GA: A random-effects regression model for meta-analysis. Stat Med. 1995 Feb 28, 14 (4): 395-411.
58.Edwards D, Berry JJ: The efficiency of simulation-based multiple comparisons. Biometrics. 1987 Dec, 43 (4): 913-928.
59.Campbell B, Kreider RB, Ziegenfuss T, La Bounty P, Roberts M, Burke D: International society of sports nutrition position stand: protein and exercise. J Int Soc Sports Nutr. 2007 Sep 26, 4: 8-
60.American College of Sports Medicine, American Dietetic Association, Dietitians of Canada: Joint position statement: Nutrition and athletic performance. american college of sports medicine, american dietetic association, and dietitians of canada. Med Sci Sports Exerc. 2000 Dec, 32 (12): 2130-2145.
61.Lemon PW, Tarnopolsky MA, MacDougall JD, Atkinson SA: Protein requirements and muscle mass/strength changes during intensive training in novice bodybuilders. J Appl Physiol. 1992 Aug, 73 (2): 767-775.
62.Lemon PW: Beyond the zone: protein needs of active individuals. J Am Coll Nutr. 2000 Oct, 19 (5 Suppl): 513S-521S.
63.Moore DR, Del Bel NC, Nizi KI, Hartman JW, Tang JE, Armstrong D: Resistance training reduces fasted- and fed-state leucine turnover and increases dietary nitrogen retention in previously untrained young men. J Nutr. 2007 Apr, 137 (4): 985-991.
64.van Houwelingen HC, Arends LR, Stijnen T: Advanced methods in meta-analysis: multivariate approach and meta-regression. Stat Med. 2002 Feb 28, 21 (4): 589-624.
65.Peterson MD, Rhea MR, Alvar BA: Applications of the dose-response for muscular strength development: a review of meta-analytic efficacy and reliability for designing training prescription. J Strength Cond Res. 2005 Nov, 19 (4): 950-958.
66.Ogasawara R, Kobayashi K, Tsutaki A, Lee K, Abe T, Fujita S: mTOR signaling response to resistance exercise is altered by chronic resistance training and detraining in skeletal muscle. J Appl Physiol. 2013 Jan, 31:
67.Coffey VG, Zhong Z, Shield A, Canny BJ, Chibalin AV, Zierath JR: Early signaling responses to divergent exercise stimuli in skeletal muscle from well-trained humans. FASEB J. 2006 Jan, 20 (1): 190-192.